4.1. Состав раствора из I компонентов характеризуется следующими концентрационными единицами (1 ≤ i ≤ I, Mi – мольные массы компонентов,ρ, ρ1, г/см3 – плотности раствора и чистого растворителя):
1) ni – число молей i- го компонента.
2) xi = ni /n – мольная или молярнаядоля, где 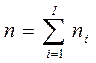
3) Моляльность m 2 – число молей растворенного вещества (компонента 2) в 1 кг растворителя с индексом 1
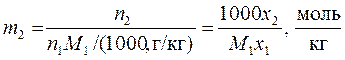 . Формула обратного пересчета моляльности в мольную долю
. Формула обратного пересчета моляльности в мольную долю 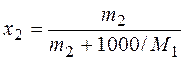 получается из 2).
получается из 2).
4) Объемная концентрация ci = ni /V, моль/м3 (CИ). Молярная концентрация или молярность С 2, (моль/л ≡ М) наиболее распространена в химической практике. Взаимосвязь молярности и моляльности для бинарного раствора осуществляется формулой:
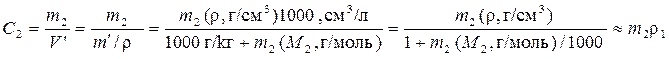 ,где V' и m' – объем и масса растворителя с растворенным веществом на 1 кг растворителя. Последнее равенство справедливо при малых m 2 , т.е. для разбавленных растворов. Для разбавленного водного раствора молярность С 2 и моляльность m 2 численно близкие величины (ρ1 ≈ 1 г/см3).
,где V' и m' – объем и масса растворителя с растворенным веществом на 1 кг растворителя. Последнее равенство справедливо при малых m 2 , т.е. для разбавленных растворов. Для разбавленного водного раствора молярность С 2 и моляльность m 2 численно близкие величины (ρ1 ≈ 1 г/см3).
5) Кроме молярности в химии используется еще одна разновидность объемной концентрации – нормальность, взаимосвязанная с понятием эквивалента и равная числу моль-эквивалентов в 1 литре раствора.
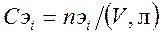 , (моль-экв/л º н.)
, (моль-экв/л º н.)
Химический эквивалент – это условная частица в целое число раз (z*) меньшая или равная соответствующей формульной единице вещества.Эк = 1/z*, где z* - эквивалентное число. (Ранее z*(Fe2(SO4)3) = 2*v = 6, Эк =1/6.)
Таким образом, веществу в количестве n молей соответствует nэ = z* n его моль-эквивалентов, а потому Сэ, н.= z* С, М.
Примеры, определяющие эквивалент вещества в химической реакции:
Al2(SO4)3+12KOH=2K3[Al(OH)6]+3K2SO4, Эк(Al2(SO4)3)=n1/n2 = 1/12, z*=12.
H2 SO4 + 2 KOH = K2 SO4 + 2H2O, Эк(H2 SO4) =1/2, z*= 2
H2 SO4 + KOH = KHSO4 + H2O, Эк(H2 SO4) = 1, z*=1,
(исходно z*– число атомов Н, замещаемых металлом или замещающих металл в реакции).
Напомним, мольная масса эквивалента Мэ = M ·Эк = M /z*.
 2015-05-26
2015-05-26 290
290







