Абсолютно нерастворимых веществ нет. Твердые вещества отличаются своей растворимостью. Очевидно, что труднорастворимый электролит легко образует насыщенный раствор. Рассмотрим равновесия, наблюдаемые в насыщенном растворе какого-нибудь труднорастворимого вещества, например, CaSO4. В этой системе осадок находится в равновесии с насыщенным раствором этого вещества:
СaSO4  Ca2+ + SO42–
Ca2+ + SO42–
осадок раствор
Константа равновесия для процесса растворения осадка имеет следующий вид:
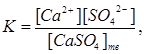
откуда K∙[CaSO4] тв = [Ca2+]∙[SO42-].
Концентрация твердого вещества есть величина постоянная:
[CaSO4] тв = const.
Учитывая это, K∙[CaSO4] тв как произведение двух постоянных величин также можно считать величиной постоянной, некоторой константой, характерной для данного вещества. Эту константу называют произведением растворимости. Её обозначают через ПР:
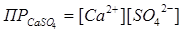 .
.
Для насыщенного раствора сульфата кальция произведение растворимости при 25оС найдено равным 3,72∙10-5 г-ион2/л2.
Таким образом, ПР – это произведение концентраций ионов малорастворимого сильного электролита, содержащихся в свободном виде в его насыщенном растворе. Величина ПР означает, что в насыщенном растворе труднорастворимого электролита произведение концентраций его ионов есть величина постоянная (при данной температуре).
Произведение растворимости характеризует растворимость электролитов. Растворимость численно равна 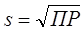 (для бинарных электролитов).
(для бинарных электролитов).
В общем случае для труднорастворимого электролита состава AnBm в растворе наблюдается равновесие:
AnBm = nAa++ mBb–.
Тогда
ПР = [Aa+]n [Вb–]m
Сравнивая значения произведений растворимости труднорастворимых солей, можно видеть, какая из них растворяется лучше (приложение, табл. 3).
Из величины ПР вытекает условие образования и растворения осадка:
1. Если [Aa+]n [Вb–]m = ПР, то осадок находится в равновесии с раствором.
2. Если [Aa+]n [Вb–]m > ПР, то осадок выпадает.
3. Если [Aa+]n [Вb–]m < ПР, то осадок растворяется.
Таким образом, если при той или иной химической реакции произведение концентраций участвующих в ней ионов станет больше произведения растворимости, то выпадает осадок труднорастворимого вещества. И обратно, если произведение концентраций ионов данного электролита в насыщенном его растворе в результате той или иной реакции становится меньше произведения растворимости для ионов этого электролита, то осадок переходит в раствор.
 2015-05-26
2015-05-26 1870
1870
