0,075 моль 0,225 моль 0,225 моль 0,15 моль 0,225 моль
Al2(SO4)3 + 3Me2S + 6H2O = 3Me2SO4 + 2Al(OH)3¯ + 3H2S
1 моль 3 моль 3 моль 2 моль 3 моль
342 г/моль (2х + 32)г/моль (2х + 96) г/моль 78 г/моль 34 г/моль
n(Al2(SO4)3) = (104,61мл × 1,22 г/мл × 0,2): 342 г/моль = 0,075 моль
m(р-ра) = 104,61 мл × 1,226 г/мл + 117г - 0,15 моль × 78 г/моль -
- 0,225 моль × 34 г/моль = 225,9 г
0,14143 = 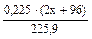 х = 23 Þ Na (натрий)
х = 23 Þ Na (натрий)
Решите:
· 26,68 мл 16%-го раствора хлорида железа (III) (r = 1,142 г/мл) полностью реагирует с 69,3 г 15%-го раствора карбоната щелочного металла. После отделения газа и осадка образуется 11,51%-ный раствор хлорида щелочного металла. Определите металл.
· Для реакции с 7,65 г оксида трехвалентного металла необходимо 74,66 мл 20 %-ного раствора соляной кислоты (r = 1,1 г/мл). Определите формулу оксида. Дайте характеристику его кислотно-основных свойств.
3. Смесь карбида и сульфида алюминия реагирует с 14%-ным раствором соляной кислоты с выделением 6,72 л смеси газов (н. у.), относительная плотность которой по гелию равна 6,7. Определите массовые доли карбида и сульфида алюминия в смеси, массовую долю хлорида алюминия в растворе. Какой объем 25%-ного раствора NaOH (r = 1,28 г/мл) вступит в реакцию со смесью карбида и сульфида алюминия?
 2015-06-14
2015-06-14 537
537








