1. Поверхность твердого тела, в отличие от поверхности жидкости, имеет сложный, неоднородный характер. Даже полированное зеркало имеет на поверхности выступы размерами до 3 * 10-7 см.
2. Адсорбция происходит не на всей поверхности, а лишь на активных центрах.
3. Адсорбция кинетически обратима – наряду с адсорбцией газа происходит его десорбция. Адсорбционное равновесие устанавливается очень быстро. Молекула газа статается адсорбированной, если она находится в поверхностном слое в течение определенного времени, называемого временем адсорбции т. Существуют методы, позволяющие экспериментально определить т. Так, для паров кадмия, адсорбированных на стекле, 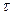 = 10-6-10-12 с в зависимости от температуры; для паров аргона на стекле
= 10-6-10-12 с в зависимости от температуры; для паров аргона на стекле 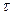 =3*10-5 с, при 90 К и
=3*10-5 с, при 90 К и 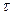 = 75 * 10-5 с при 78 К[3].
= 75 * 10-5 с при 78 К[3].
В зависимости от природы адсорбционных сил адсорбция газов и паров может быть физической и химической (см. параграф 2.5).
С повышением температуры физическая адсорбция уменьшается, так как возрастает интенсивность теплового движения молекул газа, стремящихся равномерно распределиться по всему объему системы. Это приводит к уменьшению времени адсорбции, а следовательно, к уменьшению количества адсорбированного вещества.
При хемосорбции молекулы адсорбата образуют с адсорбентом химические соединения. Хемосорбция может быть поверхностной (химическая реакция протекает только в пределах поверхностного слоя). Например, при адсорбции кислорода на поверхности алюминия происходит реакция:
4А1 + 3О2 = 2А12О3,
в результате которой алюминий покрывается прочной оксидной пленкой.
Хемосорбция может быть и объемной, когда слой вещества, образовавшегося в результате реакции на поверхности, не препятствует дальнейшему проникновению газа в объем твёрдого адсорбента, например:
СаО(тв) + СО2(г) = СаСО3(ТВ),
Хемосорбция, в отличие от физической адсорбции, является необратимой.
Обычно имеют место промежуточные случай, когда основная масса адсорбированного вещества связана с адсорбентом сравнительно слабо, а следы его связаны прочно и могут быть удалены лишь путем длительного прогревания и откачивания. Водород на никеле при низких температурах адсорбируется физически ввиду малой скорости химической реакции, но при повышений температуры начинает протекать адсорбция с заметной энергией активации по типу химических реакций.
4. Поверхность адсорбента часто бывает пористой. Наличие пор приводит к тому, что адсорбция сопровождается капиллярной конденсацией.
5. Наряду с адсорбцией, представляющей собой поверхностный процесс, может происходить поглощение газа или пара всем объемом твердого тела (например, поглощение водорода металлическим палладием или платиной). Это явление называется адсорбцией.
Адсорбцию газа на твердом адсорбенте количественно характеризуют величиной а:
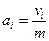 , моль/г,
, моль/г,
где vi – количество i-гo газа, адсорбированного на твердом адсорбенте; m – масса адсорбента.
Иногда вместо количества газа указывают его массу (m):
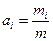 , г/г.
, г/г.
Часто количество газа выражают через его объем, приведенный к нормальным условиям:
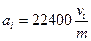 ,см3/г.
,см3/г.
Каким образом охарактеризована адсорбция, легко установить по размерности приведенной величины аi.
Величина адсорбции газа на твердом адсорбенте зависит от следующих факторов:
• температуры;
• концентрации (равновесного давления) пара или газа в поверхностном слое;
• в природы твердого тела;
• •природы газа.
 2015-06-05
2015-06-05 4033
4033
