| Кислота | Формула | Т. пл., оС | Растворимость, г в 100 мл воды, 20 °С | К1 · 105 при 25 оС | К2 · 105 при 25 оС |
| Щавелевая (этандиовая) | 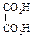
| 5,3 | |||
| Малоновая (пропандиовая) | 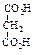
| 0,22 | |||
| Янтарная (бутандиовая) | 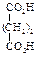
| 6,6 | 0,25 | ||
| Глутаровая (пентадиовая) | 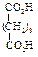
| 4,7 | 0,29 | ||
| Адипиновая (гександиовая) | 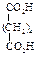
| 3,7 | 0,24 | ||
| Пимелиновая (гептандиовая) | 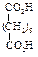
| 3,4 | 0,26 | ||
| Фталевая (о -бензолдикарбоновая) | 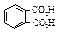
| 206-208 | 0,7 | 11220 | 0,3920 |
| Изофталевая (м -бензолдикарбоновая) | 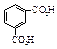
| 0,01 | 2420 | 2,520 | |
| Терефталевая (п -бензолдикарбоновая) | 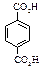
| (возг) | 0,002 | 2920 | 3,520 |
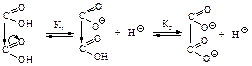
Влияние одной карбоксильной группы, проявляющей электроноакцепторный индукционный эффект, на другую в этом случае максимально. Сила кислот уменьшается с увеличением числа углеродных атомов между ними, т.к. влияние одной карбоксильной группы на другую ослабевает.
Вторая константа диссоциации (К2) меньше вследствие того, что отрыв второго протона от карбоксилат-иона оказывается более трудным, чем отрыв первого протона от нейтральной молекулы.
 2015-06-24
2015-06-24 486
486








