| Название, формула | Т пл., оС | Растворимость в 100 мл воды при 25 оС, г | К1·105 |
| Гликолевая НОСН2–СООН | Сильно растворима | ||
(±) Молочная
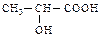
| ∞ | ||
(±) Яблочная
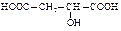
| |||
(±) Винная
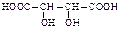
|
В зависимости от положения гидроксигруппы по отношению к карбоксильной группе дегидратация оксикислот происходит по-разному.
b-Оксикислоты отщепляют воду чрезвычайно легко при нагревании с кислотой, превращаясь в непредельные соединения.
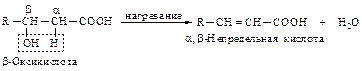
При нагревании a-оксикислот происходит реакция межмолекулярной этерификации – отщепление двух молекул воды от двух молекул кислоты, и образуется шестичленное кольцо – лактид.
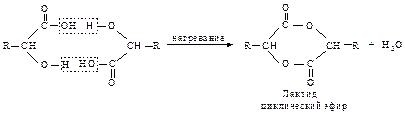
g- и d-Оксикислоты также при нагревании теряют воду и превращаются в циклические пяти- и шестичленный эфиры – лактоны (внутримолекулярная этерификация).
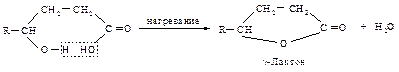
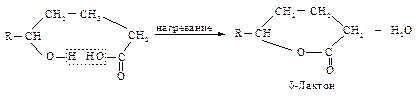
Методы синтеза оксикислот различны в зависимости от относительного расположения –ОН и –СООН-групп.
a-Оксикислоты получают гидролизом циангидринов.
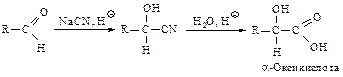
b- и g-Оксикислоты синтезируют из соответствующих b- и g-кето-эфиров гидрированием.
|
|
|
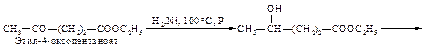
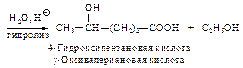
b-Оксикислоты получают также по реакции Реформатского. a-Бромэфир вводят в реакцию с цинком в абсолютном эфире, при этом образуется цинкорганическое соединение (I), которое затем присоединяется к карбонильному соединению.
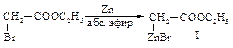
Цинкорганическое соединение (I) подобно магнийорганическому вступает в реакцию с кетоном (или альдегидом) с образованием третичного спирта, содержащего сложноэфирную группу (II), последующий гидролиз которого дает b-оксикислоту (III).
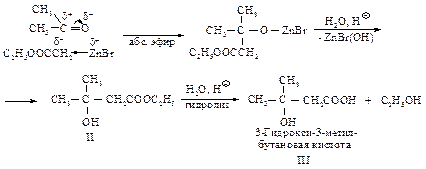
В этой реакции цинк используется вместо магния, так как цинкорганические соединения менее реакционноспособны, чем реактивы Гриньяра, и не реагируют со сложноэфирной группой.
Реакцию Реформатского можно использовать для синтеза карбоновых кислот более сложного строения. b-Оксикислоты легко теряют воду, превращаясь в a,b-непредельные карбоновые кислоты, которые могут быть превращены в насыщенные кислоты.
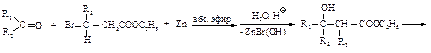

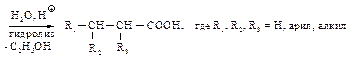
 2015-06-24
2015-06-24 1222
1222








