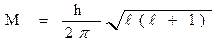| Радиус атома, R (нм) | • обычно в качестве радиуса атома принимают расстояние от ядра до главного максимума плотности внешних электронных орбиталей; • увеличение заряда ядра в периодах приводит к уменьшению атомного радиуса, а в главных и третьей побочной подгруппах – к увеличению. | |||
| Энергия ионизации Eи (эВ/атом, кДж/моль) | • энергия, необходимая для удаления электрона из атома, иона, радикала или молекулы в газовой фазе при Т = 0 К без передачи освобожденному атому кинетической энергии Чем легче атом отдает электрон, тем сильнее его восстановительные свойства. Восстановительная способность атомов с ростом заряда ядра в периодах уменьшается, в главных подгруппах, как правило, растет. • зависит от электронной конфигурации атома (иона) • полностью или наполовину заполненные подуровни обладают, как правило, повышенной устойчивостью | |||
| Энергия сродства к электрону, Eср (кДж/моль, эВ/атом,) | • энергия, выделяющаяся при присоединении электрона к нейтральному атому; чем больше Eср, тем сильнее выражены окислительные свойства элемента. Eср=0 у атомов с устойчивыми электронными конфигурациями s2, s2p6, d10 например: Mg, Ne, Сd (исключения: Be, Zn) | |||
| Электро-отрицатель-ность ЭО | • условная величина, характеризующая способность атома в химическом соединении смещать к себе общую электронную пару; • зависит от соотношения значений энергии ионизации (Eи) и сродства к электрону (Eср) | |||
| Квантовые числа | • параметры, характеризующие состояние электрона в атоме | |||
| Главное квантовое число n | • определяет основной запас энергии электрона, иными словами, степень его удаленности от ядра, или размер электронного облака (орбитали). •может принимать целочисленные значения от 1 до ∞ | |||
| Орбитальное (побочное, азимутальное) квантовое число l | • определяет орбитальный момент количества движения электрона
• характеризует форму электронного облака • может принимать все целочисленные значения от 0 до (n – 1) | |||
| Магнитное квантовое число ml | • определяет значение проекции орбитального момента количества движения электрона M на произвольно выделенную ось (например z): 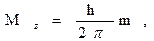 • характеризует пространственную ориентацию электронного облака. • может принимать все целочисленные значения от – l до + l • характеризует пространственную ориентацию электронного облака. • может принимать все целочисленные значения от – l до + l | |||
| Спиновое квантовое число s | • характеризует механический момент электрона, связанный с его собственным движением • может принимать значения +½ или – ½ | |||
| Формулы электронного строения атомов (электронные формулы) | • показывают распределение электронов в атоме по энергетическим уровням и подуровням +8O 1s2 2s22p4 | |||
| Порядок заполнения энергетических уровней электронами | • регулируется принципом наименьшей энергии, принципом запрета (Паули); | |||
| Принцип наименьшей энергии | • электроны в первую очередь располагаются в пределах электронного подуровня с наинизшей в данных условиях энергией | |||
| Принцип запрета Паули (1925г.) | • в атоме не может быть двух электронов в одинаковых квантовых состояниях, т.е. с одинаковыми значениями всех четырех квантовых чисел | |||
| Правило Гунда (Хунда) | • суммарное значение спина электронов в подуровне должно быть максимальным | |||
| Правила Клечковского | • Атомные орбитали заполняются в порядке: 1) Увеличения суммы значений главного и орбитального квантовых чисел n + l 2) При одинаковых значениях этой суммы – в порядке возрастания значений главного квантового числа – (n) | |||
| Электронные аналоги | • атомы, у которых валентные электроны расположены на орбиталях, описываемых одинаковой структурой внешних электронных слоев | |||
| Изобары | • атомы, имеющие одинаковые значения массового числа, но различные заряды ядер (атомные номера) 21 21 Ne и Na 10 11 | |||
| Изотопы | • разновидности атомов химического элемента, имеющих одинаковое число протонов, но различное число нейтронов в ядрах 21 20 Ne и Ne (11 и 10 нейтронов 10 10 соответственно) | |||
| Изотоны | • атомы, ядра которых содержат одинаковое число нейтронов 20 21 Ne и Na (по 10 нейтронов) 10 11 | |||
| Квантовая химия | • учение о строении и физико-химических свойствах молекул (ионов, радикалов, комплексов); включает учение о природе химической связи, валентности, электронной структуре молекул, электрических и магнитных свойствах молекул. | |||
| Основные положения квантовой химии (механики) | • дискретность (квантование) энергии • корпускулярно – волновой дуализм (двойственная природа микрочастиц – электрона, фотона и т.д.) • вероятностный характер законов микромира | |||
| Волновая функция ψ «пси» | • математическая функция, описывающая состояние электрона в атоме или молекуле | |||
| Принцип неопределенности Гейзенберга | •микрочастица (так же как и волна) не имеет одновременно точных значений координат и импульса (скорости) | |||
| Уравнение Шрёдингера | • основное уравнение квантовой механики, описывающее поведение квантовомеханической системы во времени и пространстве; его решение дает полную энергию системы и волновую функцию, с помощью которой можно в принципе рассчитать любое наблюдаемое свойство системы • ¶2Y ¶2Ψ ¶2Y 2m —— + —— + —— + ——— (Е – Еп)Ψ = 0 ¶x2 ¶y2 ¶z2 h2 где Е, Еп – соответственно, полная и потенциальная энергия электрона; m – масса электрона; h – постоянная Планка; Y – волновая функция, квадрат модуля которой ïYï2 характеризует плотность вероятности нахождения электрона в соответствующей области пространства • решением уравнения Шредингера является математическое описание атомной орбитали, которое возможно лишь при вполне определенных, дискретных значениях квантовых чисел |
Характеристики атома
|
|
Подборка статей по вашей теме:
- Излучение и поглощение энергии атомами и молекулами
- Строение атома. Опыты Резерфорда. Постулаты Бора. Теория атома водорода
- Строение атома и систематика химических элементов
- Теоретическая часть. Первая попытка создания модели атома принадлежит Дж
- Атомарность и Interlocked
- Опыт Резерфорда: предложение своей модели атома
- Модели атома Томсона и Резарфорда
- Структура атома. Изотопы. Изотоны. Изобары
- Квантовая модель атома водорода
- Строение атома. Химическая связь
- Ядро атома. Ядерные реакции. Радиоактивность
 2015-06-26
2015-06-26 1765
1765