Методические указания к выполнению самостоятельной работы по курсу «Химия» для студентов технических специальностей и направлений,
по курсу «Общая и неорганическая химия» для студентов направления 240100 «Химическая направления»очной формы обучения
Одобрено
редакционно-издательским советом
Балаковского института техники,
технологии и управления
Балаково 2011
Цель работы: ознакомиться с основными классами неорганических веществ.
ОСНОВНЫЕ ПОНЯТИЯ
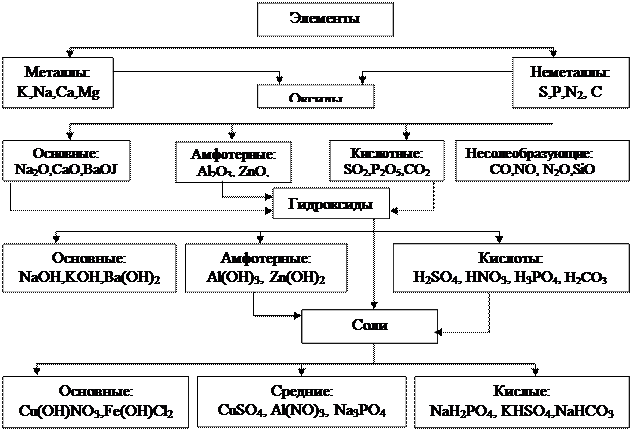 Все неорганические вещества можно разделить на классы, которые объединяют вещества сходные по составу и свойствам. К важнейшим классам неорганических веществ относятся оксиды, основания, амфотерные гидроксиды, кислоты и соли (рис.1).
Все неорганические вещества можно разделить на классы, которые объединяют вещества сходные по составу и свойствам. К важнейшим классам неорганических веществ относятся оксиды, основания, амфотерные гидроксиды, кислоты и соли (рис.1).
 | |||||
 | |||||
 | |||||
 |
Рис. - 1. Взаимосвязь между классами кислородосодержащих
неорганических соединений
Оксиды -это соединения химических элементов с кислородом. Общая формула оксидов - ЭmOn, где m –число атомов элемента, n- число атомов кислорода.
Все оксиды делятся на солеобразующие и несолеобразующие. [1-5, 8]
Несолеобразующие (индифферентные) оксиды (N2O, NO, CO, SiO) не взаимодействуют ни с кислотами, ни с основаниями.
Солеобразующие оксиды образуют соли при взаимодействии с кислотами или основаниями. Большинство солеобразующих оксидов, взаимодействуя с водой, образуют гидроксиды.Гидроксиды – это общее название оснований (NaOH, Cu(OH)2) и кислородосодержащих кислот (H2SO4, Н3РO4).
Некоторые гидроксиды являются амфотерными (Zn(OH)2 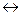 H2ZnО2.
H2ZnО2.
Солеобразующие оксиды подразделяются на основные, кислотные и амфотерные.
Основные оксиды - это оксиды (Na2O, ВаО), взаимодействующие с кислотами, кислотными или амфотерными оксидами с образованием солей:
К2О + 2НС1 = 2КCl + H2O
BaO + P2O5 = Ba3(PO4)2
CaO + Al2O3 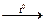 Ca(AlO2)2
Ca(AlO2)2
Основные способы получения основных оксидов:
1.Окисление металлов
СаО + О2 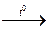 2СаО
2СаО
2.Обжиг сульфидов металлов
2СаS + 3O3 = 2CaO + 2SO2
3. Разложение нерастворимых оснований
Mg(OH)2 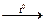 MgO + H2O
MgO + H2O
4. Разложение солей кислородосодержащих кислот
СаСО3 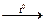 СаО + СО2
СаО + СО2 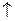
Гидроксиды основных оксидов являются основаниями, например, NaOH, Ba(OH)2. Основные оксиды взаимодействуют с водой, если им соответствуют растворимые основания
Na2O + Н2O = 2NaOH
Кислотные оксиды — это оксиды (СO2, SO3, Р2О5 ), взаимодействующие с основаниями или основными оксидами с образованием солей.
SO3 + 2NaOH = Na2SO4 + Н20
SiO2 + MgO = MgSiO3
Основные способы получения кислотных оксидов:
1. Окисление неметаллов
S + O2 = SO2
2. Окисление солей бескислородных солей
2ZnS + O2 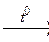 2ZnO + 2SO2
2ZnO + 2SO2
3. Разложение некоторых кислот или солей кислородосодержащих кислот.
H2SO3 =SO2 + H2O
СаСО3 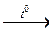 СаО + СО2
СаО + СО2 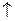
Гидроксиды кислотных оксидов являются кислотами,например: H2CO3, H2SO4. Большинство кислотных оксидов при взаимодействии с водой образуют кислоты: N2O5+ Н2O = 2HNO3
Амфотерные оксиды — это оксиды (A12O3, ZnO), образующие соли при взаимодействии как с основаниями, так с кислотами.
ZnO + 2HCl = ZnCl2 + Н2О
ZnO + 2NaOH 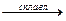 Na2ZnO2 + Н2О
Na2ZnO2 + Н2О
ZnO + 2NaOH + Н2О = Na2[Zn(OH)4]
Амфотерные оксиды с водой не взаимодействуют, поэтому получить основание или кислоту можно только косвенным путем
Al2O3 + 6HNO3 = 2Al(NO3)3 + 3Н2О
2Al(NO3)3 + 3KOH = Al(OH)3 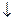 + 3KNO3
+ 3KNO3
Амфотерным оксидам соответствуют амфотерные гидроксиды, например: А1(ОН)3 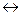 Н AlО3, H2ZnO2
Н AlО3, H2ZnO2 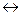 Zn(OH)2
Zn(OH)2
Основные и амфотерные оксиды образуют только металлы, кислотные оксиды – неметаллы и металлы с высшей валентностью.Одновалентные металлы образуют основные оксиды, например, Na2О, К2О, Cu2О и др. Большинство двухвалентных металлов, за исключением (Be, Zn, Pb, Sn), также образуют основные оксиды, например, BaO, СаО, FeO и др.
Be, Zn, Pb, Sn и большинство трех- и четырехвалентных металлов образуют амфотерные оксиды, например, ВеО, ZnО, PbO2, SnO2., А12O3, Сr2O3, Fe2O3 , MnO2 и др.
Пяти-, шести- и семивалентные металлы образуют кислотные оксиды, например, Sb2O3, CrO3, Мп2O7 и др. [ ]
В периодах характер оксидов постепенно изменяется от основных к амфотерным и кислотным, например, в третьем периоде:
Na2O, MgO Al2O3, SiO2, P2O5,, SO3, Cl2O7
основные амфотерные кислотные
У элементов, имеющих различную степень окисления, также наблюдается постепенный переход от основных оксидов к амфотерным и кислотным, например: MnO, Mn2 O3, MnO2, Mn2O5, MnO3, Mn2O7
основные амфотерные кислотные
Основания – это вещества, состоящие из атомов металла и одной или нескольких гидроксидных групп (ОН). Общая формула оснований – Ме(ОН)n, где n- валентность металла. Основания в растворах диссоциируют с образованием катионов металла и анионов – гидроксид-ионов. В результате замещения гидроксидных групп кислотными остатками образуются соли.[1-58 ] Основания взаимодействуют с кислотами, кислотными и амфотерными оксидами c образованием солей
NaOH + HCl = NaCl + H2O
Ba(OH)2 + CO2 = BaCO3 + H2O
Основания классифицируются:
а) по растворимости в воде:
- растворимые. Растворимые в воде основания, за исключением NH4OH, образованы щелочными и щелочно-земельными металлами и называются щелочами: LiOH, NaOH, КОН, RbOH, CsOH, Sr(OH)2, Ва(ОН)2, получаются взаимодействием металлов или оксидов металлов IА или II A групп с водой (кроме Be и Mg, BeО и MgО)
2Na + 2H2O = 2NaOH + H2 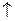
Ba + 2H2O = Ba(OH)2 + H2 
K2O + H2O =2KOH
CaO + H2O =Ca(OH)2
- нерастворимые: Cu(QH)2, Fe(OH)2, Fe(OH)3 и др. Нерастворимые в
воде основания получают косвенным путем
CuO + H2SO4 = CuSO4 + H2O
CuSO4 + 2NaOH = Cu(OH)2  + Na2SO4
+ Na2SO4
б) по числу гидоксидных группв молекуле:
- однокислотные, молекулы, которых содержат одну гидроксидную группу: КОН, LiOH NH4OH и др.;
- двухкислотные, молекулы которых содержат две гидроксидные группы: Mg(ОН)2, Fe(OH)2 и др.;
- трехкислотные, молекулы которых содержат три гидроксидные группы: Ni(OH)3, Bi(OH)j и др.
Кислоты – это вещества, состоящие из атомов водорода, способных замещаться на атомы металла, и кислотного остатка (An). Общая формула кислот - HmAn, где m - валентность кислотного остатка. Валентность кислотного остатка определяется числом атомов водорода в молекуле кислоты.
Кислоты в растворах диссоциируют с образованием катионов водорода и анионов кислотных остатков. В результате замещения атомов водорода в молекулах кислот атомами металла образуются соли. Кислотные остатки An входят как в состав кислот, так и в состав солей.
Кислоты взаимодействуют с основаниями, основными и амфотерными оксидами с образованием солей
HNO3 + NaOH = NaNO3 + H2O
H2SO4 + FeO = FeSO4 + H2O
2 HCl + ZnO = ZnCl2 + H2O
Кислоты классифицируются:
1) по составу (содержанию кислорода):
- бескислородные, в состав молекул которых не входят атомы кислорода; НCl, HI, HBr, HCN, H2S и др. Получают взаимодействием неметаллов с водородом
H2 + Cl2 = 2HCl
- кислородсодержащие, молекулы которых содержат атомы кислорода: HNО3, H2SО4, Н3РО4 и НClO4 др. Получают взаимодействием кислотных оксидов с водой
P2O5 + 3H2O = 2H3PO4
Кислоты из кислотных оксидов, которые не взаимодействуют с водой, можно получить косвенным путем.
SiO2 + 2NaOH = Na2SiO3 + H2O 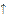
Na2SiO3 + 2HCl  H2SiO3
H2SiO3 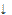 + 2NaCl
+ 2NaCl
2) по основности:
- одноосновные,молекулы которых содержат один атом водорода: HCl, HNО3,HCN, СН3СООН, HMnO4 идр.;
- двухосновные,молекулы которых содержат два атома водорода: H2S, H2SО4, H2S03, Н2СО3, H2 Cr2O7 и др.;
- трехосновные,молекулы которых содержат три атома водорода: H3P04, H3BО3, H3AsО4;
- четырехосновные: Н4Р2О7и др.
Основность кислоты определяется числом атомов водорода,которые в молекуле кислоты могут замещаться атомами металла. Кислоты, молекулы которых содержат два и более атомов водорода, называются многоосновными.
Формулы, названия кислот и их солей приведены в табл.1
Амфотерные гидрооксиды, в зависимости от условий, могут проявлять как основные, так и кислотные свойства, им соответствуют амфотерные оксиды. Они взаимодействуют с кислотами, щелочами, основными и кислотными оксидами.
2 Аl(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
Аl(OH)3 + 3NaOH = Na3[Al(OH)6]
2 Аl(OH)3 + Na2O 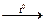 2 NaAlO2 + 3H2O
2 NaAlO2 + 3H2O
2 Аl(OH)3 + 3SO3 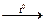 Al2(SO4)3 + 3H2O
Al2(SO4)3 + 3H2O
Амфотерные гидрооксиды получают косвенным путем, т. к. амфотерные оксиды с водой не взаимодействуют.
В периодах характер гидрооксидов постепенно изменяется следующим образом, например, в третьем периоде:
NaOH, Mg(OH)2, Al(OH)3 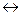 H3AlO3, Si(OH)4
H3AlO3, Si(OH)4  H2SiO3, H3PO4, H2SO4, HClO4
H2SiO3, H3PO4, H2SO4, HClO4
основания амфортерные гидроксиды кислоты
Соли – это вещества, образованные катионом металла и анионом кислотного остатка. Общая формула соли - MemAnn, где m - валентность (заряд) кислотного остатка, n – валентность (заряд) катиона металла.
Соли делятся на три типа: нормальные (средние), кислые, основные.[]
Средние соли в растворах диссоциируют на катионы металлов и анионы кислотных остатков.
Нормальные (средние) соли — это продукты полного замещенияатомов водорода в молекуле кислоты атомами металла
H2СO3 + 2NaOH = Na2СO3 + H2O
или продукты полного замещениягидроксидных групп в молекуле основания кислотными остатками
Ba(OH)2 + 2HCl = BaCl2 + H2O
Кислые соли - это продукты неполного замещенияатомов водорода в молекулах многоосновных кислот атомами металла.
Таблица 1
Названия кислот и их средних солей
| Кислота | Название | |
| кислоты | cредней соли | |
| Н3АsО3 | Мышьяковистая | Арсениты |
| Н3АзO4 | Мышьяковая, орто- | Арсенаты, орто- |
| НзВОз | Борная, орто- | Бораты, орто- |
| НВг | Бромоводород | Бромиды |
| НВгОз | Бромноватая | Броматы |
| НСN | Циановодород (синильная) | Цианиды |
| Н2СОз | Угольная | Карбонаты |
| НСl | Хлороводород (соляная) | Хлориды |
| НСlOз | Хлорноватая | Хлораты |
| НСlO4 | Хлорная | Перхлораты |
| Н2СrO4 | Хромовая | Хроматы |
| Н2Сr2O7 | Двухромовая | Дихроматы |
| НF | Фтороводород(плавиковая) | Фториды |
| НI | Иодоводород | Иодиды |
| НIOз | Йодноватая | Иодаты |
| НМпO4 | Марганцовая | Перманганаты |
| НNO2 | Азотистая | Нитриты |
| НNОз | Азотная | Нитраты |
| НРОз | Фосфорная, мета- | Фосфаты, мета- |
| Н3РО3 | Фосфористая | Фосфиты |
| Н3Р04 | Фосфорная, орто* | Фосфаты, орто- |
| Н4Р207 | Фосфорная, дву- (пиро-) | Дифосфаты |
| Н2S | Сероводород | Сульфиды |
| Н2SOз | Сернистая | Сульфиты |
| Н2SO4 | Серная | Сульфаты |
| Н2SiO3 | Кремниевая | Силикаты |
Молекулы кислых солей содержат атомы водорода, например:
H2СO3 + NaOH = NaHСO3 + H2O
H3PO4+ NaOH = NaH2PO4
H3PO4+ 2NaOH = Na2 HPO4
Кислые соли могут образовывать только многоосновные кислоты Н2CO3, H2SO4, H2SO3, H3PO4. Двухосновная кислота с любым металлом образует одну нормальную и одну кислую соль (NaHCО3— гидрокарбонат натрия). Трехосновная кислота с любым металлом образует одну нормальную и две кислые соли (NaH2PO4 -дигидрофосфат натрия, Na2НРO4 - гидрофосфат натрия).
Основные соли - это продукты неполного замещениягидроксидных групп в молекулах многокислотных оснований кислотными остатками.
Ca(OH)2 + HCl = CaOHCl + H2O
Al(OH)3 + HNO3 = Al (OH)2NO3 + H2O
Al(OH)3 + 2HNO3 = Al OH(NO3)2 + H2O
Двухкислотное основание образует одну нормальную и одну основную соль (CaOHCl - гидроксохлорид кальция). Трехкислотное основание образует одну нормальную и две основные соли Al(OH)2NO3 - дигидрокcонитрат алюминия., AlOH(NO3)2 - гидроксонитрат алюминия).
Двойные соли образуются при замещении атомов водорода в кислотах на два различных катеона. Например: КAl(SO4)2 + 12H2O – додекагидрат сульфата алюминия-калия (алюмокалиевые квасцы)
Пример 1. Классифицируйте и назовите следующие оксиды: K2O, P2O5, Mn2O7, MnO2, BeO, SO3, MgO.
Решение.
Основные оксиды: K2O – оксид калия, MgO – оксид магния.
Кислотные оксиды: P2O5 – оксид фосфора (V), Mn2O7 – оксид марганца (VII), SO3 – оксид серы (VI).
Амфотерные оксиды: MnO2 – оксид марганца (IV), BeO – оксид бериллия.
Пример 2. Классифицируйте следующие основания по кислотности и назовите их: Ni(OH)2, LiOH, Fe(OH)3, Co(OH)3, Mn(OH)3, Fe(OH)2, NaOH.
Решение.
Однокислотные основания: LiOH – гидрооксид лития, NaOH – гидрооксид натрия.
Двухкислотные основания: Ni(OH)2 – гидрооксид никеля (II), Fe(OH)2 – гидрооксид железа (II).
Трехкислотые основания: Fe(OH)3 – гидрооксид железа (III), Co(OH)3 – гидрооксид кобальта (III), Mn(OH)3 – гидрооксид марганца (III).
Пример 3. Назовите и классифицируйте следующие кислоты по основности и по содержанию атомов кислорода: H3PО4, HNО2, H2S, HCN, НСlО3, H2CO3, HF, НзАsO4.
Решение.
Одноосновные кислоты: HNО2 - азотистая, HCN - циановодородная, HF - фтористоводородная, НС1О3 – хлорноватистая кислота
Двухосновные кислоты: H2S - сероводородная, Н2СО3 - угольная
Трехосновные кислоты: H3PO4 - фосфорная, H3AsO4 -
Бескислородные кислоты: H2S, HCN, HF
Кислородсодержащие кислоты: H3PO4, HN02, НСlO3, H2CO3, H3AsO4
Пример 4. Классифицируйте и назовите следующие соли: BaSО4, (CuOH)2SО4, NaH2PО4, Ca(HS)2, FeOHCl2, A1PО4, MnOHNО3.
Решение.
Нормальные соли: BaSО4 - сульфат бария, А1РО4 - фосфат алюминия.
Кислые соли: NaH2PО4 - дигидрофосфат натрия, Ca(HS)2 - гидросульфид кальция.
Основные соли: (CuОH)2SO4 - гидроксосульфат меди (II), FeOHCl2 - гидроксохлорид железа (III), MnOHNО3 - гидроксонитрат марганца (II).
Для закрепления материала используйте программированный контроль в режиме «самоконтроль».
Вопросы для самоконтроля
1. Какую общую формулу имеют оксиды?
1) Ме(ОН)n; 2) ЭmОn; 3) НmАn; 4) МеmАnn
2. Какой из оксидов является несолеобразующим?
1) А12O3; 2) СO2; 3) СО; 4) Fe2O3.
3. Формула высшего оксида элемента, образующего водородное соединение ЭН2, имеет вид
1) Э; 2) ЭО4; 3) ЭО3; 4) ЭО2.
4. Какой из оксидов является амфотерным?
1) ZnO; 2) SiO2; 3) SiO; 4) Na2O.
5. Какой из оксидов является основным?
1) MnO; 2) MnO2; 3) MnO3; 4) Mn2O7.
6. С кислотами и щелочами взаимодействует оксид:
1) хрома (III); 2) хрома (VI); 3) хрома (II); 4) магния.
7. Кислотными являются оксиды
1) магния; 2) железа(II); 3) Серы (IV); 4) Азота (V)
8. В избытке щелочи не растворяется
1) Cr(OH)3; 2) Al(OH)3; 3) Zn(OH)2; 4) Mg(OH)2
9. Какое из оснований является однокислотным?
1) Cu(OH)2; 2) NaOH; 3) Fe(OH)3; 4) Fe(OH)2
10. Какая из кислот является двухосновной?
1) HNO2; 2) НВr; 3) Н2SO4; 4) Н3BO3.
11. Какая из солей является нормальной (средней) солью?
1) NaH2PO4; 2) Na2HPO4; 3) Na3PO4; 4) Na2HPO3
12. Какой соли соответствует название «гидрокарбонат никеля (II)»?
1) Ni(HCO3)3; 2) NiOHCO3; 3) Ni(HCO3)2; 4) (NiOH)2CO3
13. Какой соли соответствует название «дигидроксосульфат висмута (III)»?
1) BiOHSO3; 2) BiOHSO4; 3) [Bi(OH)2]2SO4; 4) [Bi(OH)2]2SO3
Таблица 2
Правильные ответы
| № вопроса | |||||||||||||
| № ответа | 3,4 |
 2015-07-14
2015-07-14 4313
4313








