Ферменти – це каталізатори, активність яких може бути регульована. Більшість ферментів можуть зв’язуватися з малими молекулами, які мають назву модифікатори (ефектори) і можуть змінювати ферментативну активність. До них належать:
- інгібітори – сполуки, які гальмують активність ферменту;
- активатори – сполуки, які збільшують ферментативну активність.
Відповідно результат дії інгібіторів має назву інгібування, активаторів – активація.
Активація ферментативної активності може відбу-ватися під дією кофакторів, субстратів або інших метаболітів.
Кофактори можуть позитивно впливати на зв’язування субстрату з активним центром, каталітичне перетворення S, іноді утворюють метало-субстратні комплекси, які більш ефективно підлягають дії ферменту.
До кофакторів, що здатні активувати ферменти, належать як іони металу, так і невеличкі органічні молекули, наприклад, похідні водорозчинних вітамінів (НАД, ФАД, ТГФК тощо). Усе це стосується лише ферментів, робота яких потребує наявності кофактора.
Молекули субстрату також можуть активувати фермент, але за рахунок інших механізмів. Відомо, що молекули субстрату стабілізують структуру ферменту та індукують необхідні конформаційні зміни в активному центрі.
Інгібування ферментативної активності може відбуватися за різними механізмами, тому існує декілька видів інгібіторів і відповідно інгібування. Слід відзначити, що інгібіторами не є сполуки, які руйнують структуру ферменту шляхом денатурації.
Ці сполуки належать до інактиваторів, а процес має назву інактивація. 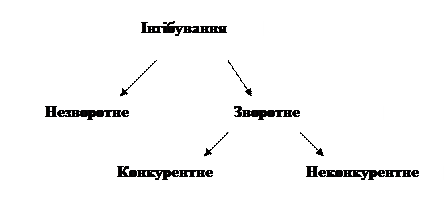
Рисунок 13 - Види інгібування активності ферментів
На рис. 13 наведена класифікація видів інгібування активності ферментів, яке можу бути як зворотним, так і незворотним процесом.
Незворотне інгібування спостерігається в разі, коли інгібітор міцно зв’язується з молекулою ферменту, що викликає незворотну втрату активності. Незворотні інгібітори є отрутами.
Прикладом незворотного інгібування може бути дія отруйної речовини – диізопропілфторфосфату (ДФФ). ДФФ утворює ковалентні зв’язки із залишками серину в активному центрі ацетилхолінестерази, біологічною функцією якої є розщеплення нейромедіатора ацетилхоліну. В результаті цього
|
 ацетилхолін накопичується у синапсах і «отруює» організм.
ацетилхолін накопичується у синапсах і «отруює» організм. 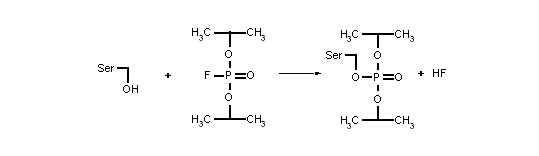
Залишок Сер у складі Еnz ДФФ Диізопропілфосфорил-
фермент
Рисунок 14 - Реакція ДФФ із залишком серину у активному центрі ацетилхолінестерази
На рис. 14 наведений хімізм реакції, яка відбувається в активному центрі ферменту при дії ДФФ. Реактивація ферменту неможлива у зв’язку з неможливістю розірвати зв'язок між інгібітором та залишком серину.
Зворотне інгібування властиве для значної кількості ферментів живих організмів, для яких при різних фізіологічних умовах необхідна зміна активності. Так, наприклад, продукція енергії у мітохондріях залежить від енергетичного статусу клітини, молекулярним показником якого є концентрація АТФ, АДФ, АМФ та ін. сполуки. При зростанні кількості енергії, яка не використовується клітиною, молекула АТФ буде інгібітором деяких ферментів, які задіяні в генерації цієї енергії.
Зворотне інгібування буває двох видів: конкуренте та неконкурентне (рис. 13).
Конкурентне інгібування відбувається в разі, коли молекула інгібітора за структурою схожа на молекулу субстрату і конкурує з ним за активний центр ферменту. В разі, коли в середовищі знаходяться молекули інгібітора, вони зв’язуються з активним центром та перешкоджають зв’язуванню молекул субстрату. Для конкурентного інгібування характерні такі основні кінетичні характеристики ферменту: Km – збільшується, Vmax – залишається без змін.
Зняти цей вид інгібування можна надлишком субстрату, тобто внесення у середовище значної кількості субстрату призводить до того, що молекули субстрату витісняють молекули інгібітора з активного центру ферменту.
Конкурентними інгібіторами можуть бути молекули екзогенного та ендогенного походження. Оскільки вони схожі за будовою на молекули субстрату, їх ще називають антиметабо-літами.
Так, наприклад, структурні аналоги пара-амінобензойної кислоти (ПАБК) – сульфаніламіди - мають антибактеріальну дію, тому що конкурентно інгібують в бактеріальних клітинах утворення дегідрофолієвої кислоти (ДГФК). Ця кислота є попередником синтезу тетрагідрофолієвої кислоти (ТГФК), яка, у свою чергу, необхідна для синтезу нуклеїнових кислот. Таким чином, сульфаніламідні препарати мають бактеріостатичну дію.
Іншим прикладом антиметаболіту є меркаптопурин, який є структурним аналогом пуринових азотистих основ і використовується для лікування деяких онкологічних захворювань. Дія препарату базується на тому, що при його включенні в обмін нуклеотидів порушується синтез пуринів, що, у свою чергу, інгібує синтез нуклеїнових кислот у клітинах, що проліферують в S-фазі клітинного циклу.
Конкурентне інгібування може спостерігатися при отруєнні деякими сполуками. В цьому разі знання механізмів реактивації при конкурентному інгібуванні має велике значення для пошуку підходів до лікування.
Наприклад, при отруєнні метанолом використовують значні дози етанолу, який є субстратом для алкогольде-гідрогенази (АДГ). Метанол – це отрута, яка діє на нервову і судинну систему. Доза 30 мл вважається летальною. В разі отруєння метанол блокує активний центр АДГ, тому що за будовою схожий на етанол. Надлишок етанолу (діє як антидот) знімає інгібування і при вчасній допомозі сприяє одужанню пацієнта.
Аналогічний підхід використовують при лікуванні отруєння етиленгліколем – складовою частиною антифризу. Етиленгліколь під дією алкогольдегідрогенази перетворюється у щавлеву кислоту, яка є дуже токсичною для організму людини, тому, за статистикою, щороку у світі від отруєння етиленгліколем гинуть понад 50 осіб. Використання значних доз етанолу (токсичних для здорової людини) обумовлено ефектом заміщення молекул етиленгліколю в активному центрі АДГ на етанол і блокування утворення отруйної щавлевої кислоти. В результаті етиленгліколь виводиться з організму.
Неконкурентне інгібування ферментативної активності є результатом зв’язування молекули інгібітора не з активним центром, а з іншою ділянкою молекули білка-ферменту. Оскільки інгібітор не впливає на зв’язування ферменту з субстратом, у результаті може утворитися потрійний комплекс ферменту (Е), субстрату (S) та інгібітора (I):
Е + S + I ↔ ESI
Механізм інгібування полягає в тому, що після такого зв’язування відбуваються конформаційні зміни в активному центрі, який у подальшому не може нормально функціонувати та перетворювати S у Р.
При неконкурентному інгібуванні Km – не змінюється, Vmax – зменшується.
За будовою неконкурентний інгібітор не схожий на молекулу субстрату, тому зняти цей вид інгібування надлишком субстрату неможливо. Для цього існують спеціальні сполуки – реактиватори, які міцно зв’язують інгібітор і, таким чином, звільняють фермент від нього.
Прикладами неконкурентного інгібування можуть бути:
1) дія іонів важких металів (ртуті, свинцю, кадмію та ін.), які блокують SH-групи активного центру. Зняти таке інгібування допомагають реактиватори – SH-комплексони (цистеїн, димеркаптопропанол). Ці сполуки містять SH-групи, які зв’язують іони важких металів:
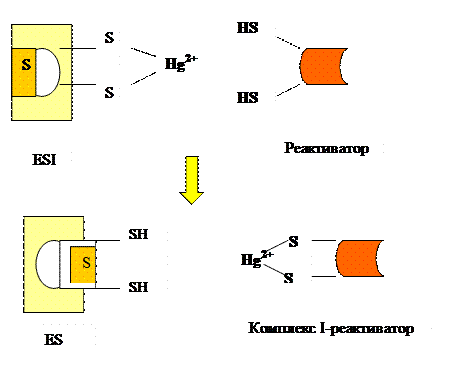
2) дія ціанідів CN- , які реагують з Fe3+, що входить до складу цитохромоксидази – ферменту дихального ланцюга мітохондрій і повністю блокують синтез АТФ у клітині.
 2015-08-13
2015-08-13 1005
1005








