Белки
Белки – это биополимеры, мономерами которых являются аминокислоты.
Аминокислоты – низкомолекулярные амфотерные органические соединения, хорошо растворимые в воде, плохо- в органических растворителях;
содержащие -
1. амино – ( - NH2) группу;
2. карбоксильную – (-СООН) группу, которыесоединены с одним и тем же атомом углерода.
R (СН3) R – радикал,придающий каждой аминокислотесвои
определенные свойства
H2N--- С---- СООН
I. В зависимости от количества амино-, карбоксильных-групп:
· Нейтральные -АК, содержащие одну карбоксильную и одну аминогруппу(аланин).
· Основные - АК, содержащие более, чем одну аминогруппу (лизин).
· Кислые - АК, содержащие более, чем одну карбоксильную группу (глутаминовая).
II. По возможности синтезироваться ЖО:
§ Незаменимые АК -которые животные и человек не могут сами синтезировать и должны получать в готовом виде, с пищей. (перечислить См. эти АК)
III. От количества АК:
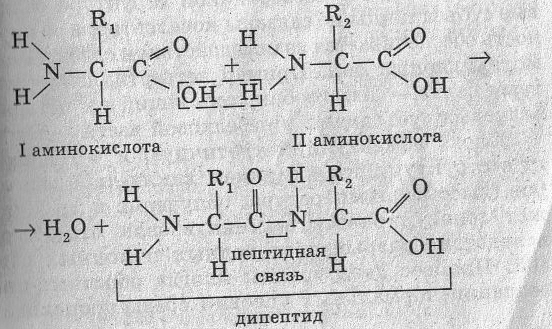
ü Дипептид – соединение, состоящее из 2-х молекул АК, соединенных пептидной связью;
ü Олигопептиды – вкл. от 2 до 10 АК (гормоны гипофиза окситоцин, вазопрессин, брадикинин – пептид боли, опиаты – выполн. функцию обезболивания);
ü Полипептид - более 10АК (инсулин);
ü Белки – от 50 до несколько тыс. АК остатков, с мол. массой свыше 5000.
IV. По форме молекул:
v Фибриллярные – нерастворимые белки, склонны к образованию волокон (кератин - кожи, волос, ногтей; миозин - мышц; коллаген - сухожилий);
v Глобулярные – растворимые белки, требующие подвижности (транспортные; ферменты; защитные)
V. По составу:
o Простые -белки образованные только АК (сывороточный альбумин крови, фибрин, трипсин).
o Сложные – имеющие в своем составе компонент неаминокислотной природы (ионы металлов – металлопротеины, липиды - липопротеины; сахара – глико-протеины; нуклеотиды - нуклеопротеины) - иммуноглобулины.
Уровни организации белковых молекул
| Название структуры | Особенности структуры | Характерные химические связи |
| Первичная (не менее 50 аминокислот) | Цепочка аминокислот | Пептидные связи (ковалентные, прочные) |
| Вторичная | Цепочка закручена в спираль – α – спираль; β – складчатый слой | Водородные связи(непрочные) между NH-группами и СО-группами соседних витков |
| Третичная | Дальнейшее «сворачивание» молекулы, образование глобулы, специфичной для каждого белка. Данной структурой определяется специфичность и биологическая активность белковых молекул. | Водородные (непрочные) и ковалентные связи между удаленными друг от друга радикалами. А также S-S (дисульфидными мостиками), аминокислота содержащая серу (цистеин) |
| Четвертичная(есть не у всех белков) | Комплекс из нескольких белковых макромолекул с третичной структурой. | Прочность обеспечивается за взаимодействием слабых межмолекулярных связей. |
| Необратимая деструкция - после прекращения действия фактора белок не восстанавливается (разрушение вторичной и первичной структуры) - |
Денатурация белка - нарушение природной структуры белка под действием природных факторов (температуры, радиации, химических веществ, и т.д.)
| Обратимая - после прекращения действия фактора, белок восстанавливает свою структуру и свойства (разрушение только третичной структуры) |
Все белки живых организмов построены из 20 аминокислот.
Функции белков зависит от:
1. Состава,
2. Количества
3. Порядка расположения - аминокислот.
 2015-10-16
2015-10-16 791
791







