Газовыеэлектроды могут быть обратимыми относительно анионов (кислородный) или относительно катионов (водородный). Газовые электроды состоят из металлического проводника (Pt или металлов платиновой группы), контактирующего одновременно с газом и раствором, содержащим ионы этого газа. Металлический проводник служит для подвода и отвода электронов, а также является катализатором электродной реакции (ускоряет установление равновесия на электроде). Так как в равновесных электродных реакциях газовых электродов участвуют газообразные компоненты, то потенциалы этих электродов зависят от парциальных давлений газов.
Равновесие на водородном электроде выражается уравнением 2Н++ 2 
 Н2. Уравнение Нернста для расчета потенциала водородного электрода имеет следующий вид:
Н2. Уравнение Нернста для расчета потенциала водородного электрода имеет следующий вид:
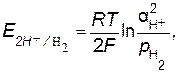 (8.5)
(8.5)
где 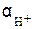 −активность ионов Н+ в электролите; р Н
−активность ионов Н+ в электролите; р Н 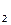 −парциальное давление водорода.
−парциальное давление водорода.
Е 2Н+ / Н2 = −0,059 рН. (8.6)
Подставляя числовые значения R, F, стандартной температуры, равной Т =298 К, и учитывая, что lgH+ =−pH, уравнение Нернста при р Н 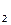 =1 приобретает вид:
=1 приобретает вид:
Кислородный электрод состоит из платиновой пластинки, контактирующей с кислородом и раствором, содержащим ионы, которые образуются при восстановлении кислорода (ионы ОН-):
О2, Pt │ОН-.
Если на кислородном электроде протекает реакция по уравнению
2Н2О + О2 + 4 
 4ОН-,
4ОН-,
то выражение равновесного потенциала при Т = 298 К имеет вид:
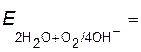
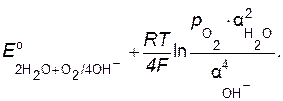 (8.7)
(8.7)
Так как активность воды в ходе реакции изменяется незначительно, то ее считают величиной постоянной и уравнение для расчета потенциала кислородного электрода при подстановке значений R, F и T = 298 К приобретает вид:
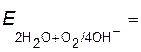
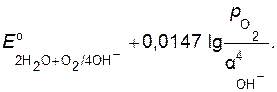 (8.8)
(8.8)
где Е о2Н 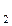 О+О
О+О 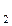 /4ОН-–стандартный потенциал кислородного электрода, равный 0,401 В (при
/4ОН-–стандартный потенциал кислородного электрода, равный 0,401 В (при 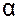 ОН- =1 моль/л).
ОН- =1 моль/л).
Проведя ряд преобразований, получаем уравнение Нернста для расчета кислородного электрода в виде:
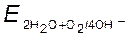 =1,229−0,059рН. (8.9)
=1,229−0,059рН. (8.9)
Зависимости значений равновесных потенциалов водородного и кислородного электродов от рН приведены в приложении (табл. 14).
 2015-10-22
2015-10-22 5926
5926







