ВИЗНАЧЕННЯ ПИТОМОЇ ТЕПЛОТИ ПАРОУТВОРЕННЯ КАЛОРИМЕТРИЧНИМ МЕТОДОМ
Мета роботи: Вивчити явище пароутворення і визначити питому теплоту пароутворення води.
Прилади і приладдя: електроплитка, колба з водою, сухопарник, калориметр з мішалкою і кришкою, термометр, технічні терези, різноваги.
Література
1. Грабовский Р.И. Курс физики: Учеб. пособие для с.-х. ин-тов. – М., 1979. – 552 с.
2. Розумнюк В.Т., Якименко І.Л. Фізика. Основні поняття, явища і закони. – Біла Церква, 2004. – 71 с.
Теоретичні відомості
Пароутворенням називають перехід речовин із рідкого стану в газоподібний.
Існує два процеси пароутворення – випаровування і кипіння.
Випаровуванням називають відрив молекул від поверхні рідини.
У процесі випаровування від поверхні відриваються ті молекули, що мають кінетичну енергію, достатню для подолання сил притягання до сусідніх молекул. Таким чином, при випаровуванні відриваються від поверхні рідини молекули з більшою енергією, а залишаються в рідині молекули з меншою енергією. Це означає, що внаслідок випаровування температура рідини зменшується. (Нагадаємо, що температура будь-якого тіла залежить від середньої кінетичної енергії його молекул. Чим більша середня енергія молекул, тим температура тіла вища і навпаки).
|
|
|
Випаровування відбувається при будь-якій температурі, тому що при будь-якій температурі є молекули, що мають достатню енергію для розриву міжмолекулярних зв’язків. Цю енергію вони отримують від своїх сусідок при взаємному зштовхуванні внаслідок хаотичного руху. При більш низьких температурах таких молекул менше, а значить менша й інтенсивність випаровування.
Кипінням називають відрив молекул як від поверхні рідини, так і в її об’ємі.
В об’ємі молекули відриваються в бульбашки повітря, які завжди є всередині будь-якої рідини. Найчастіше всього вони знаходяться в подряпинах, щілинах чи місцях стінок посудини, не змочених рідиною. На відміну від випаровування, кипіння відбувається не при будь-якій, а при певній для кожної рідини температурі. Для води при нормальному тиску ця температура дорівнює 100 °С. По мірі кипіння молекули рідини, що оточують бульбашку повітря, відриваються від рідини в бульбашку і її розмір зростає. Зростає в бульбашці й величина тиску. Коли цей тиск дорівнює або є більшим суми гідростатичного тиску стовпчика рідини над бульбашкою і атмосферного тиску, бульбашка спливає на поверхню і лопається, переносячи таким чином молекули рідини в атмосферу.
Пароутворення, як при випаровуванні, так і при кипінні, вимагає затрат енергії для подолання сил притягання між молекулами рідини. Ці затрати при певних зовнішніх умовах (температурі і тиску) характеризуються питомою теплотою пароутворення.
|
|
|
Питомою теплотою пароутворення називають кількість теплоти, яку необхідно витратити для перетворення одиниці маси рідини в пару при температурі пароутворення.
В СІ питома теплота пароутворення λ вимірюється в Дж/кг. Різні рідини мають різні значення λ тому, що в них різні сили притягання між молекулами.
Кількість теплоти  Q, необхідноїдля перетворення деякої маси m рідини в пару при температурі пароутворення, буде:
Q, необхідноїдля перетворення деякої маси m рідини в пару при температурі пароутворення, буде:
∆Q = λ m, (1)
де  (лямбда) – питома теплота пароутворення.
(лямбда) – питома теплота пароутворення.
Теплота – це фізична величин, що є мірою сумарної кінетичної енергії хаотичного руху молекул тіла.
Температура є кількісною характеристикою інтенсивності хаотичного руху молекул тіла, показником середньої швидкості хаотичного руху молекул та середньої кінетичної енергії хаотичного руху молекул.
В даній роботі для визначення питомої теплоти пароутворення води використовують визначення теплоти, що віддається водяною парою воді в калориметрі й самому калориметру, коли пару напускають в калориметр з холодною водою. При цьому калориметр і вода в ньому нагріваються.
Запишемо рівняння теплового балансу для цього процесу:
 , (2)
, (2)
де  Q1 – енергія, отримана водою в калориметрі при нагріванні від
Q1 – енергія, отримана водою в калориметрі при нагріванні від  до
до  .
.
 , (3)
, (3)
де  – питома теплоємність води; m
– питома теплоємність води; m  – маса води в калориметрі до початку досліду;
– маса води в калориметрі до початку досліду;  – температура води в кінці досліду;
– температура води в кінці досліду;  – початкова температура води в ньому.
– початкова температура води в ньому.
 Q
Q 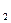 – енергія, отримана калориметром при нагріванні від
– енергія, отримана калориметром при нагріванні від  до
до  .
.
 , (4)
, (4)
де  – питома теплоємність латуні (матеріалу калориметра); m
– питома теплоємність латуні (матеріалу калориметра); m 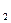 – маса калориметра; θ – температура калориметра в кінці досліду; t1 – температура калориметра на початку досліду.
– маса калориметра; θ – температура калориметра в кінці досліду; t1 – температура калориметра на початку досліду.
 Q
Q  – енергія, що передається парою при конденсації (конденсацією називають перехід речовини із газоподібного стану в рідкий).
– енергія, що передається парою при конденсації (конденсацією називають перехід речовини із газоподібного стану в рідкий).
 , (5)
, (5)
де  – питома теплота пароутворення; m
– питома теплота пароутворення; m  – маса пари.
– маса пари.
ΔQ  – енергія, що передається конденсатом (сконденсованою парою) при його охолодженні від температури кипіння
– енергія, що передається конденсатом (сконденсованою парою) при його охолодженні від температури кипіння  до температури
до температури  :
:
 , (6)
, (6)
де  – питома теплоємність води; m
– питома теплоємність води; m  – маса пари;
– маса пари;  – температура пари (температура кипіння води); θ – температура води в кінці досліду.
– температура пари (температура кипіння води); θ – температура води в кінці досліду.
Підставивши формули(3), (4), (5) і (6) у рівняння (2) знаходимо робочу формулу для визначення λ:
 (7)
(7)
Опис установки
Калориметр являє собою латунну посудину 6 (рис. 7.1) з мішалкою 8 і кришкою 7. Сухопарник 4 висушує пару, звільнюючи її від крапель води, що сконденсувалися при проходженні пари по трубці. Ця вода відводиться через трубку із зажимом 3, який відкривають по мірі накопичення води в сухопарнику. 1 – скляна колба, в яку наливається досліджувана рідина, 10 – термометр, 5 – стакан, 2 – електроплитка, 9 – ексікатор (повітряний термостат).

Рис. 7.1.
 2015-10-22
2015-10-22 408
408








