В настоящее время иммунология определяет иммунитет как метод защиты организма от живых тел и веществ, несущих на себе признаки чужеродности.
Разработка теории иммунитета дала возможность медицине решить такие проблемы, как:
· безопасность переливания крови,
· создание вакцин против оспы, бешенства, сибирской язвы, дифтерии, полиомиелита, коклюша, кори, столбняка, газовой гангрены, инфекционного гепатита, гриппа и других инфекций.
Благодаря этой теории была:
· устранена опасность резус-гемолитической болезни новорожденных,
· в практику медицины введена пересадка органов,
· стала возможна диагностика многих инфекционных болезней.
Громадное значение для сохранения здоровья человека имело познание законов иммунологии.
Но еще большее значение для медицинской науки имеет дальнейшее раскрытие секретов иммунитета в профилактике и лечении многих опасных для здоровья и жизни человека болезней.
1. Неспецифическая система защиты предназначена противостоять действию различных внешних для организма повреждающих факторов любой природы.
При возникновении заболевания неспецифическая система осуществляет первую, раннюю защиту организма, давая ему время для включения полноценного иммунного ответа со стороны специфической системы.
Неспецифическая защита включает в себя деятельность всех систем организма.
Она формирует:
· воспалительный процесс,
· лихорадку,
· механическое выделение повреждающих факторов с рвотой, кашлем…
· изменение обмена веществ,
· активацию ферментных систем,
· возбуждение ферментных систем
· торможение различных отделов нервной системы.
Механизмы неспецифической защиты включают:
клеточные и гуморальные элементы, обладающие сами по себе или в комплексе бактерицидным действием.
2. Специфическая (иммунная) система на проникновение чужеродного агента реагирует следующим образом:
· при первичном попадании развивается первичный иммунный ответ,
· при повторном проникновении в организм – вторичныйиммунный ответ
Они имеют определенные отличия.
При вторичномответе на антиген сразу вырабатывается IgG.
Первичный иммунный ответ – это первое взаимодействие антигена (вируса или бактерии) с лимфоцитом вызывающее реакцию.
В ходе него лимфоциты начинают постепенно развиваться, претерпевая дифференцировку:
· некоторая часть становится клетками памяти,
· другие преобразуются в зрелые клетки, продуцирующие антитела.
При первой встрече с антигеном сначала появляются антитела класса IgM, затем – IgG, а позже – IgА.
Вторичный иммунный ответ развивается при повторном контакте с тем же самым антигеном.
В данном случае происходит уже более быстрая выработка лимфоцитов с превращением их в зрелые клетки и быстрая выработка значительного количества антител, которые высвобождаются в кровь и тканевую жидкость, где они могут встретиться с антигеном и эффективно побороть болезнь.
Неспецифическая и специфическая системы защиты организма.
Неспецифическая система защиты, как уже указывалось выше, включает:
Клеточные элементы
2. гуморальные элементы.
1. Клеточные элементы неспецифической защиты – это фагоциты:
· макрофаги
· нейтрофильные гранулоциты (нейтрофилы, или макрофаги).
Это высокоспециализированные клетки, дифференцирующиеся из стволовых клеток, вырабатываемых костным мозгом.
Макрофаги составляют в организме отдельную мононуклеарную (одноядерную) систему фагоцитов, в которую входят промоноциты костного мозга, дифференцирующиеся из них моноциты крови и тканевые макрофаги.
Их особенностью является активная подвижность, способность прилипать и интенсивно осуществлять фагоцитоз.
Моноциты, созрев в костном мозге, циркулируют в течение 1-2-х суток в крови, а затем проникают в ткани, где дозревают до макрофагов и живут 60 и более суток.
Макрофаги содержат ферменты для переваривания фагоцитированных веществ.
Эти ферменты содержатся в вакуолях (пузырьках), называемых лизосомами, и способны расщеплять белки, жиры, углеводы и нуклеиновые кислоты.
Макрофаги очищают организм человека от частиц неорганического происхождения, а также от бактерий, вирусных частиц, отмирающих клеток, токсинов – ядовитых веществ, образующихся при распаде клеток или вырабатываемых бактериями.
Кроме того, макрофаги выделяют в кровь некоторые гуморальные и секреторные вещества:
· элементы комплемента С2, С3, С4,
· лизоцим,
· интерферон,
· интерлейкин-1,
· простагландины,
· макроглобулин,
· монокины, регулирующие иммунный ответ,
· цитоксины – ядовитые для клеток вещества.
Макрофаги обладают тонким механизмом распознавания чужеродных частиц антигенной природы.
Они различают и быстро поглощают старые и новорожденные эритроциты, не трогая нормальных.
Долгое время за макрофагами была закреплена роль «чистильщиков», но они являются и первым звеном специализированной системы защиты.
Макрофаги, включая антиген в цитоплазму, распознают его с помощью ферментов.
Из лизосом выделяются вещества (лизоцим), растворяющие антиген в течение приблизительно 30 мин, после чего он выводится из организма.
Но некоторые антигены не могут быть полностью переваренными, они деградируют и выводятся из макрофагов в течение суток.
Переработанный таким образом антиген несет на себе «отметку», которую способны воспринимать клетки или гуморальные элементы специфической защиты.
Антиген проявляется и опознается макрофагом, после чего переходит к лимфоцитам.
Нейтрофильные гранулоциты (нейтрофилы, или микрофаги) также формируются в костном мозге, откуда поступают в кровоток, в котором циркулируют в течение 6-24 ч.
В отличие от макрофагов созревшие микрофаги получают энергию не от дыхания, а от гликолиза, как прокариоты, т. е. становятся анаэробами, и могут осуществлять свою деятельность в бескислородных зонах, например в экссудатах при воспалении, дополняя деятельность макрофагов.
Макрофаги и микрофаги на своей поверхности несут рецепторы к иммуноглобулину IgG и к элементу комплемента С3, которые помогают фагоциту в распознавании и прикреплении антигена к поверхности его клетки.
Нарушение деятельности фагоцитов довольно часто проявляется в виде
· повторяющихся гнойно-септических заболеваний, таких как хроническая пневмония, пиодермия, остеомиелит и др.
· кожно-слизистый кандидоз является следствием дефекта нейтрофилов, который делает их неспособными убивать грибок Candida. \
Это заболевание протекает как массивное разрушение тканей и не поддается обычным методам лечения, включая интенсивную комбинированную антибиотикотерапию.
· При ряде инфекций возникают различные приобретения фагоцитоза.
например, туберкулезные микобактерии не разрушаются при фагоцитировании.
Стафилококк тормозит поглощение его фагоцитом.
· Нарушение деятельности фагоцитов приводит также к развитию хронического воспаления и болезням, связанным с тем, что накопленный макрофагами материал от разложения фагоцитированных веществ не может быть выведен из организма вследствие недостаточности некоторых ферментов фагоцита.
Патология фагоцитоза может быть связана с нарушением взаимодействия фагоцитов с другими системами клеточного и гуморального иммунитета.
Так, при инфекциях, возбудители которых паразитируют внутри клетки (туберкулезе, лепре, листериозе), большое значение имеет активация макрофагов Т-лимфоцитами.
Таким образом, на процесс фагоцитоза влияют факторы как неспецифической, так и специфической систем защиты.
Фагоцитозу способствуют:
· нормальные антитела и иммуноглобулины,
· комплемент,
· лизоцим,
· лейкины,
· интерферон
· ряд других ферментов и секретов крови, предварительно обрабатывающих антиген, делая его более доступным для захвата и переваривания фагоцитом.
2. Гуморальные элементы неспецифической защиты:
Комплемент – ферментная система, которая состоит из 11 белков сыворотки крови, составляющих 9 компонентов (от С1 до С9) комплемента.
Система комплемента способствует:
· стимуляции фагоцитоза,
· хемотаксиса (привлечения или отталкивания клеток),
· выделению фармакологически активных веществ (анафилотоксина, гистамина и др.),
· усиливает бактерицидные свойства сыворотки крови,
· активирует цитолиз (лизирование клеток)
· совместно с фагоцитами принимает участие в уничтожении микроорганизмов и антигенов.
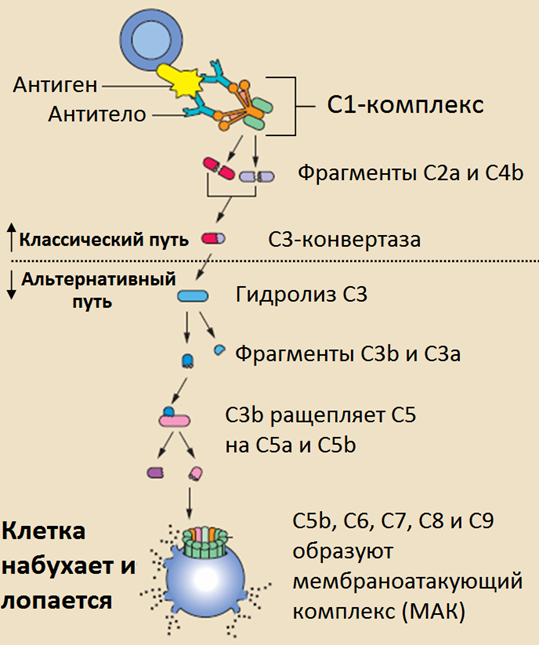
Каждый из компонентов комплемента играет свою роль в иммунном ответе:
Недостаточностькомпонентов комплемента:
· недостаточность комплемента С1 вызывает снижение бактерицидности плазмы крови и способствует частому развитию инфекционных заболеваний верхних дыхательных путей, хронического гломерулонефрита, артрита, отита и др.
· комплемент С3 подготавливает антиген к фагоцитозу.
при его недостаточности значительно снижается ферментативная и регуляторная активность системы комплемента, что приводит к более тяжелым последствиям, чем недостаточность комплементов С1 и С2, вплоть до смертельного исхода.
Его модификация С3а откладывается на поверхности бактериальной клетки, что приводит к образованию отверстий в оболочке микроба и его лизису, т. е. растворению лизоцимом.
· при наследственной недостаточности компонента С5 встречаются нарушение развития ребенка, дерматиты и диарея.
· специфический артрит и нарушение свертываемости крови наблюдаются при дефиците С6.
· диффузные поражения соединительной ткани возникают при снижении концентрации компонентов С2 и С7.
Врожденная или приобретенная недостаточность компонентов комплемента способствует развитию различных заболеваний как в результате снижения бактерицидных свойств крови, так и вследствие накопления в крови антигенов.
Кроме недостаточности, встречается также и активация компонентов комплемента:
· активация С1 приводит к отеку Квинке и др.
Активно потребляется комплемент при термическом ожоге, когда создается дефицит комплемента, что может определить неблагоприятный исход термической травмы.
Нормальные антитела выявлены в сыворотке здоровых людей, которые ранее не болели.
По-видимому, эти антитела возникают при:
· наследовании или же
· антигены поступают с пищей, не возбуждая соответствующего заболевания.
Обнаружение таких антител свидетельствует о зрелости и нормальном функционировании иммунной системы.
К нормальным антителам относится, в частности, пропердин.
Пропердин - высокомолекулярный белок, обнаруживаемый в сыворотке крови:
· обеспечивает бактерицидное и вирусонейтрализирующее свойства крови (в совокупности с другими гуморальными факторами)
· активизирует реакции специализированной защиты.
Лизоцим – это фермент ацетилмурамидаза, разрушающий оболочки бактерий, лизирующий их.
Он находится почти во всех тканях и жидкостях организма.
· Способность к разрушению клеточных оболочек бактерий, с чего и начинается уничтожение, объясняется тем, что лизоцим в высокой концентрации находится в фагоцитах и его активность увеличивается при микробной инфекции.
· Лизоцим усиливает антибактериальное действие антител и комплемента.
· Он входит в состав слюны, слез, кожных выделений как средство, усиливающее барьерную защиту организма.
Ингибиторы ( замедлители ) вирусной активности представляют собой первый гуморальный барьер, препятствующий контакту вируса с клеткой.
Люди с высоким содержанием ингибиторов высокой активности отличаются высокой устойчивостью к вирусным инфекциям, при этом для них малоэффективны вирусные вакцины.
Неспецифические механизмы защиты – клеточные и гуморальные – защищают внутреннюю среду организма от различных повреждающих факторов органической и неорганической природы на тканевом уровне.
Они достаточны для обеспечения жизнедеятельности низкоорганизованных (беспозвоночных) животных.
Усложнение организма животных, в частности, привело к тому, что неспецифическая защита организма оказалась недостаточной.
Усложнение организации привело к увеличению количества специализированных клеток, отличающихся друг от друга.
На этом общем фоне в результате мутации могли появляться клетки, вредные для организма, или могли внедриться в организм похожие, но чужеродные клетки.
Необходимым становится генетический контроль клеток, и появляется специализированная система защиты организма от клеток, отличающихся от его родных, необходимых.
Вероятно, лимфатические механизмы защиты поначалу развивались не для защиты от внешних антигенов, а для обезвреживания и устранения внутренних элементов, которые ведут «подрывную работу» и угрожают целостности особи и выживанию вида.
Видовая дифференциация позвоночных при наличии общей для любого организма основы-клетки, различающейся по структуре и функциям, привела к необходимости создания механизма различения и обезвреживания клеток организма, в частности клеток-мутантов, которые, размножаясь в организме, могли привести его к гибели.
Механизм иммунитета, возникший как средство внутреннего контроля над клеточным составом тканей органа, в силу своей высокой эффективности использован природой против повреждающих факторов-антигенов: клеток и продуктов их деятельности.
С помощью этого механизма складывается и закрепляется генетически реактивность организма к одним видам микроорганизмов, к взаимодействию с которыми он не адаптирован, и иммунитет клеток, тканей и органов к другим.
Возникают формы иммунитета:
1. видовая и
2. индивидуальная,
Формирующиеся соответственно в адаптациогенезе и адаптациоморфозе как проявления компенсациогенеза и компенсациоморфоза.
Обе формы иммунитета могут быть:
· абсолютными, когда организм и микроорганизм практически не взаимодействуют ни при каких условиях, или
· относительными, когда взаимодействие вызывает патологическую реакцию в определенных случаях, ослабляющих иммунитет организма, делающих его восприимчивым к воздействию микроорганизмов, безопасных в нормальных условиях.
Задача специфической иммунологической системы защиты организма заключается в том, чтобы:
· компенсировать недостаточность неспецифических факторов органического происхождения – антигенов, в частности микроорганизмов и токсических продуктов их деятельности.
Она начинает действовать тогда, когда неспецифические механизмы защиты не могут уничтожить антиген, близкий по своим характеристикам клеткам и гуморальным элементам самого организма или обеспеченный собственной защитой.
Поэтому специфическая система защиты предназначена:
распознавать, обезвреживать и уничтожать генетически чужеродные вещества органического происхождения:
· инфекционные бактерии и вирусы,
· трансплантированные от другого организма органы
· ткани, изменившиеся в результате мутации клетки собственного организма.
Точность различения очень высокая, до уровня одного гена, отличающегося от нормы.
Специфическая иммунная система – это совокупность специализированных лимфоидных клеток: Т-лимфоцитов и В-лимфоцитов.
Различают органы иммунной системы:
I. центральные
II. периферические.
I. Центральные:
· костный мозг
· тимус (вилочковая железа)
II. Периферические:
· селезенка,
· лимфатические узлы,
· лимфоидная ткань кишок, миндалин и других органов,
· кровь.
Все клетки иммунной системы (лимфоциты) являются высокоспециализированными.
Их поставщиком служит костный мозг, из стволовых клеток которого дифференцируются все формы лимфоцитов, так же как и макрофаги, микрофаги, эритроциты, тромбоциты крови.
Вторым важнейшим органом иммунной системы является вилочковая железа (тимус).
Под влиянием гормонов тимуса стволовые клетки тимуса дифференцируются в тимусзависимые клетки (или Т-лимфоциты): они обеспечивают клеточные функции иммунной системы.
Помимо Т-лимфоциты, тимус секретирует в кровь гуморальные вещества, способствующие дозреванию Т-лимфоцитов в периферических лимфатических органах (селезенке, лимфоузлах), и некоторые другие вещества.
Селезенка имеет структуру, сходную со структурой вилочковой железы, но в отличие от тимуса лимфоидная ткань селезенки участвует в иммунных реакциях гуморального типа.
В селезенке содержится до 65 % В-лимфоцитов, которые обеспечивают накопление большого количества плазматических синтезирующих антитела.
Лимфатические узлы содержат преимущественно Т-лимфоциты (до 65 %), а В-лимфоциты, плазмоциты (происходят от В-лимфоцитов) синтезируют антитела, когда иммунная система только созревает, особенно у детей первых лет жизни.
Поэтому удаление миндалин (тонзилэктомия), произведенное в раннем возрасте, снижает способность организма к синтезу некоторых антител.
Кровь относится к периферическим тканям иммунной системы и содержит, кроме фагоцитов, до 30 % лимфоцитов.
Среди лимфоцитов преобладают Т-лимфоциты (50–60 %).
В-лимфоциты составляют 20–30 %, около 10 % приходится на киллеры, или «нуль-лимфоциты», не имеющие свойств Т– и В-лимфоцитов (Д-клетки).
Т-лимфоциты образуют три основные субпопуляции:
· Т-киллеры осуществляют иммунологический генетический надзор, разрушая мутированные клетки собственного организма, в том числе и опухолевые, и генетически чужеродные клетки трансплантатов. Т-киллеры составляют до 10 % Т-лимфоцитов периферической крови. Именно Т-киллеры своим воздействием вызывают отторжение пересаженных тканей, но это и первая линия защиты организма от опухолевых клеток;
· Т-хелперы организуют иммунный ответ, воздействуя на В-лимфоциты и давая сигнал для синтеза антител против появившегося в организме антигена. Т-хелперы секретируют интерлейкин-2, воздействующий на В-лимфоциты, и интерферон. Их в периферической крови до 60–70 % общего числа Т-лимфоцитов;
· Т-супрессоры ограничивают силу иммунного ответа, контролируют активность Т-киллеров, блокируют деятельность Т-хелперов и В-лимфоцитов, подавляя избыточный синтез антител, которые могут вызывать аутоиммунную реакцию, т. е. обратиться против собственных клеток организма.
Т-супрессоры составляют 18–20 % Т-лимфоцитов периферической крови.
Избыточная активность Т-супрессоров может привести к угнетению иммунного ответа вплоть до его полного подавления.
Это бывает при хронических инфекциях и опухолевых процессах.
В то же время недостаточная деятельность Т-супрессоров приводит к развитию аутоиммунных заболеваний в связи с повышенной активностью Т-киллеров и Т-хелперов, не сдерживаемых Т-супрессорами.
Для регулирования иммунного процесса Т-супрессоры секретируют до 20 различных медиаторов, ускоряющих или замедляющих активность Т– и В-лимфоцитов.
Кроме трех основных видов, существуют и другие виды Т-лимфоцитов, в том числе Т-лимфоциты иммунологической памяти, сохраняющие и передающие информацию об антигене.
При повторной встрече с этим антигеном они обеспечивают его распознавание и тип иммунологического ответа.
Т-лимфоциты, выполняя функцию клеточного иммунитета, кроме того, синтезируют и секретируют медиаторы (лимфокины), которые:
· активизируют или
· замедляют деятельность фагоцитов,
· медиаторы с цитотоксилогическим и интерфероноподобным действиями, облегчая и направляя действие неспецифической системы.
В-лимфоциты дифференцируется в костном мозге и групповых лимфатических фолликулах и выполняет функцию гуморального иммунитета.
При взаимодействии с антигенами В-лимфоциты изменяются в плазмоциты, синтезирующие антитела (иммуноглобулины).
На поверхности В-лимфоцита может содержаться от 50 до 150 тыс. молекул иммуноглобулинов.
По мере созревания В-лимфоциты изменяют класс синтезируемых ими иммуноглобулинов.
Первоначально синтезируя иммуноглобулины класса Ig M, при созревании:
· 10 % В-лимфоцитов продолжают синтезировать Ig M
· 70 % переключаются на синтез IgG
· 20 % – на синтез Ig A.
Так же как и Т-лимфоциты, В-лимфоциты состоят из нескольких субпопуляций:
· В1-лимфоциты – предшественники плазмоцитов, синтезирующие антитела Jg M без взаимодействия с Т-лимфоцитами;
· В2-лимфоциты – предшественники плазмоцитов, синтезирующие иммуноглобулины всех классов в ответ на взаимодействие с Т-хелперами. Эти клетки обеспечивают гуморальный иммунитет на антигены, распознаваемые Т-хелперами;
· В3-лимфоциты (К-клетки), или В-киллеры, убивают клетки-антигены, покрытые антителами;
· В-супрессоры тормозят функцию Т-хелперов, а В-лимфоциты памяти, сохраняя и передавая память об антигенах, стимулируют синтез определенных иммуноглобулинов при повторной встрече с антигеном.
Особенностью В-лимфоцитов является то, что они специализируются на конкретных антигенах.
При реакции В-лимфоцитов с антигеном, встреченным впервые, образуются плазмоциты, выделяющие антитела именно против этого антигена.
Образуется клон В-лимфоцитов, ответственный за реакцию с этим конкретным антигеном.
При повторной реакции размножаются и синтезируют антитела только В-лимфоциты, а точнее – плазмоциты, направленные против этого антигена.
Другие клоны В-лимфоцитов не участвуют в реакции.
В-лимфоциты непосредственно не участвуют в борьбе с антигенами.
Под влиянием стимулов от фагоцитов и Т-хелперов они трансформируются в плазмоциты, которые и синтезируют антитела иммуноглобулины, обезвреживающие антигены.
Иммуноглобулины – белки сыворотки крови и других жидкостей организма, которые действуют как антитела, связывающиеся с антигенами и обезвреживающие их.
В настоящее время известно пять классов иммуноглобулинов человека, которые существенно различаются по своим физико-химическим свойствам и биологическим функциям:
· Ig G
· Ig M
· Ig A
· Ig D
· Ig E
Иммуноглобулины класса G составляют около 70 % от общего количества иммуноглобулинов.
К ним относятся антитела против антигенов различной природы, вырабатываемые четырьмя подклассами.
Они в основном выполняют:
· противо-бактериальные функции
· образуют антитела против полисахаридов бактериальных оболочек,
· образуют противорезусные антитела,
· обеспечивают реакцию кожной чувствительности и связывания комплемента.
IgM
(около 10 %) – наиболее древние, синтезируются на ранних стадиях иммунного ответа на большинство антигенов.
К этому классу относятся антитела против:
· полисахаридов микроорганизмов и вирусов,
· ревматоидного фактора и др.
Иммуноглобулины класса D составляют менее 1 %.
Их роль в организме почти не изучена.
Есть сведения об увеличении их при некоторых инфекционных заболеваниях, остеомиелите, бронхиальной астме и т. п.
IgE или реагины
Имеют более низкую концентрацию.
IgE играют роль пускового механизма в развертывании аллергических реакций немедленного типа.
Связываясь в комплекс с аллергеном, IgE вызывают выброс в организм медиаторов аллергических реакций (гистамина, серотонина и др.)
IgA
IgA составляют около 20 % от общего количества иммуноглобулинов.
К этому классу относятся антитела против вирусов, инсулина (при сахарном диабете), тиреоглобулина (при хроническом тиреоидите).
Особенностью этого класса иммуноглобулинов является то, что существуют они в двух формах:
· сывороточной (IgA)
· секреторной (S IgA).
Антитела класса А:
· нейтрализуют вирусы,
· обезвреживают бактерии,
· предупреждают фиксацию микроорганизмов на клетках эпителиальной поверхности слизистых оболочек.
Можно сделать следующий вывод:
Специфическая системаиммунологической защиты – это
· многоуровневый механизм элементов организма,
· обеспечивающий их взаимодействие и взаимодополняемость,
· включающий по мере необходимости компоненты защиты против любого взаимодействия организма с повреждающими факторами,
· дублирующий в нужных случаях механизмы клеточной защиты гуморальными средствами, и наоборот.
Система иммунитета, сложившаяся в процессе адаптациогенеза, закрепившая генетически видовые реакции организма на повреждающие факторы, является гибкой системой.
В процессе адаптациоморфоза она корректируется, включает новые виды реакций на повреждающие факторы, вновь появившиеся, с которыми организм не встречался ранее.
В этом смысле она играет приспособительную роль, объединяя адаптивные реакции, в результате которых структуры организма меняются под действием новых факторов среды, и компенсаторные реакции, сохраняющие целостность организма, стремящиеся уменьшить цену адаптации.
В качестве этой цены выступают необратимые адаптивные изменения, в результате которых организм, приспосабливаясь к новым условиям существования, теряет способность существовать при первоначальных условиях.
Так, клетка-эукариот, приспособившаяся существовать в условиях кислородной атмосферы, уже не может обойтись без нее, хотя анаэробы могут это делать.
Цена адаптации в этом случае – потеря способности к существованию в анаэробных условиях.
Таким образом, иммунная система включает ряд компонентов, самостоятельно вступающих в борьбу с любыми чужеродными факторами органического или неорганического происхождения:
· фагоциты,
· Т-киллеры,
· В-киллеры
· целая система специализированных, нацеленных на конкретного врага средств-антител.
Проявление иммунного ответа специфической иммунной системы разнообразно.
В случае, если мутировавшая клетка организма приобретает свойства, отличные от свойств генетически присущих ему клеток (например, опухолевые), Т-киллеры поражают клетки самостоятельно, без вмешательства других элементов иммунной системы.
В-киллеры самостоятельно уничтожают распознанные антигены, покрытые нормальными антителами
Полный иммунный ответ возникает против некоторых антигенов, впервые проникших в организм. Макрофаги, фагоцитируя такие антигены вирусного или бактериального происхождения, не могут их полностью переварить и через некоторое время выбрасывают.
Антиген, прошедший через фагоцит, несет на себе метку, свидетельствующую о его «неперевариваемости».
Фагоцит таким образом подготавливает антиген к «подаче» в систему специфической иммунной защиты.
Он распознает антиген и соответствующим образом его метит.
Кроме того, макрофаг одновременно секретирует интерлейкин-1, активирующий Т-хелперы.
Т-хелпер, столкнувшись с таким «меченым» антигеном, подает сигнал В-лимфоцитам о необходимости их вмешательства, секретируя интерлейкин-2, активирующий лимфоциты.
Сигнал Т-хелпера включает две составляющие:
· во-первых, это команда о начале действия;
· во-вторых, это информация о виде антигена, полученная от макрофага.
Получив такой сигнал, В-лимфоцит превращается в плазмоцит, синтезирующий соответствующий специфический иммуноглобулин, т. е. конкретное антитело, предназначенное для противодействия этому антигену, которое связывается с ним и обезвреживает его.
Следовательно, в случае полного иммунного ответа В-лимфоцит получает команду от Т-хелпера и информацию об антигене от макрофага.
Возможны и другие варианты иммунного ответа:
Т-хелпер, столкнувшись с антигеном до обработки его макрофагом, дает сигнал В-лимфоциту о выработке антител.
В этом случае В-лимфоцит превращается в плазмоцит, вырабатывающий неспецифические иммуноглобулины класса Ig М.
Если же В-лимфоцит взаимодействует с макрофагом без участия Т-лимфоцита, то, не получив сигнала о выработке антител, В-лимфоцит не включается в иммунную реакцию.
В то же время иммунная реакция синтеза антител начнется, если В-лимфоцит вступит во взаимодействие с антигеном, соответствующим его клону, обработанным макрофагом, даже при отсутствии сигнала от Т-хелпера, поскольку он специализирован по этому антигену.
Таким образом, специфический иммунный ответ предусматривает различные случаи взаимодействия антигена и иммунной системы.
В нем участвуют комплемент, подготавливающий антиген к фагоцитозу, фагоциты, обрабатывающие антиген и подающие его лимфоцитам, Т– и В-лимфоциты, иммуноглобулины и другие составляющие.
В процессе эволюции выработались различные сценарии борьбы с чужеродными клетками.
Можно сделать вывод что Иммунитет является сложной многоэлементной системой. Но, как и любая сложная система, иммунитет имеет недостаток. Дефект одного из элементов приводит к тому, что может отказать вся система.
Возникают болезни, связанные с иммунодепрессией, когда организм не может самостоятельно противодействовать инфекции.
 2017-12-14
2017-12-14 2297
2297
