1. Термічний розклад: CaCO3 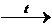 CaO + CO2↑.
CaO + CO2↑.
2Cu(NO3)2 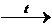 2CuO + 4NO2↑ + O2↑.
2CuO + 4NO2↑ + O2↑.
2. Обмінні реакції з кислотами, основами й іншими солями:
AgNO3 + HCl = AgCl↓ + HNO3;
Fe(NO3)3 + 3NaOH = Fe(OH)3↓ + 3NaNO3;
Na2SO4 + BaCl2 = 2NaCl + BaSO4.
3. Взаємодія з металами, які більш активні за метал, що входить до складу солі:
Zn + CuSO4 = ZnSO4 + Cu;
Cu + Hg(NO3)2 = Cu(NO3)2 + Hg.
4. Окисно-відновні реакції, що обумовлені властивостями катіона чи аніона:
2KMnO4 + 16HCl = 2MnCl2 + 2KCl + 5Cl2↑ + 8H2O.
Кислі солі (гідрогенсолі) утворюються внаслідок неповного заміщення атомів Гідрогену багатоосновних кислот на атоми металу. До складу кислих солей, крім катіона металу, входять один або кілька катіонів Гідрогену. В назві вказують спочатку назву катіона, а потім аніона, до якого додають слово „гідроген”, яке пишеться разом.
Наприклад, NaHSO4 – натрій гідрогенсульфат, KH2PO4 – калій дигідрогенортофосфат, Fe(НSO4)2 – ферум(ІІ) гідрогенсульфат.
Кислі солі, подібно багатоосновним кислотам, дисоціюють ступінчасто на катіони металів (або подібні їм), гідрогену (якщо аніон належить кислоті сильній або середньої сили) і аніони кислотних залишків: NaHSO4 ⇄ Na+ + HSO  ;
;
HSO  ⇄ Н+ + SO
⇄ Н+ + SO 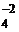 .
.
 2017-12-16
2017-12-16 590
590








