ЛЕКЦИЯ 13
Металлические покрытия помимо экранирующего оказывают и электрохимическое воздействие на металл основы.
Катодные покрытия, например на основе хрома, никеля или титана на углеродистой стали, в случае образования несплошности приводят к локальному растворению основного металла, протекающего с большой скоростью за счет действия короткозамкнутого гальванического элемента ”покрытие-основа,” в котором сталь является анодом, а покрытие катодом с большой площадью по отношению к площади анода. Сопротивление электролита в несплошности покрытия и экранирующее действие продуктов коррозии основного металла могут в некоторой степени уменьшить скорость коррозии основного металла.
Однако при долговременной защите конструктивно сложных изделий с высокоразвитой поверхность использование катодных покрытий малоэффективно вследствие высокой вероятности появления несплошности при их нанесении и эксплуатации.
Анодное покрытие, растворяясь, обеспечивает электрохимическую защиту основы в местах несплошностей (порах) покрытия. Растворение анодного покрытия вблизи пор приводит к постепенному увеличению обнаженной поверхности основы и соответственно уменьшению плотности коррозионного тока, который со временем может стать недостаточным, чтобы сохранять действие в центре обнаженной поверхности. Скорость анодного растворения понижается за счет сопротивления электролита внутри поры, блокирования пор продуктами коррозии или образования защитных пленок на обнаженной поверхности металла. Срок службы анодного покрытия в этом случае продлится.
Полярность покрытия определяется не только соотношением электродных потенциалов основы и покрытия, но в значительной степени зависит от состава среды. В процессе коррозии может в результате поляризации или других факторов произойти изменение знака потенциала покрытия. Например, анодное алюминиевое покрытие в результате пассивации может стать катодным. В сероводородсодержащих средах кадмиевые и никелевые покрытия являются катодными в отношении стали, однако в присутствии ионов хлора потенциал покрытий может сместиться в отрицательном направлении и покрытие становится анодным в отношении стали. Цинковое покрытие в сероводородсодержащей среде не меняет знака потенциала: как без ионов хлора, так и при их наличии оно является анодным по отношению к стальной основе. Однако в горячей воде (выше 60 °С) происходит перемена полярности цинка и он становится катодом по отношению к железу. Нормальный электродный потенциал у кадмия (-403 В) более положительный, чем у железа (-0,440 В), но в 0,5 н аэрированном растворе NaCl кадмий становится анодным по отношению к железу, потенциалы железа и кадмия в таком электролите имеют значения: - 0,300 и -0,531 В соответственно.
Механизм защитного действия металлических покрытий в наводороживающих средах связан как с экранирующим действием к потоку водорода, так и с электрохимическим поведением. Главные факторы, определяющие защитное действие покрытий в наводороживающих средах, приведены на рис. 53.
Экранирующий эффект покрытий связан в основном с их во-дородопроницаемостью и пористостью. Водородопроницаемость определяется растворимостью в металле покрытия и диффузией водорода через него. По критерию водородопроницаемости эффективным барьером наводороживания являются алюминий, цинк и медь, растворимость водорода в которых на два–три порядка выше, чем в стали.

Рис.53 Факторы, определяющие механизм защитного действия
металлических покрытий
В водном растворе сероводорода (1200 мг/л) стационарный потенциал незащищенной стали составляет -650 мВ, алюминиевого покрытия -570, никелевого -280, кадмиевого -410; то есть все эти покрытия в сероводородсодержащем растворе имеют катодные функции по отношению к стали, значительно облагораживая ее стационарный потенциал. В присутствии ионов хлора электродный потенциал покрытий смещается в отрицательном направлении и покрытие может стать анодным по отношению к стали. Так, для алюминия потенциал в хлорсодержащем растворе составляет -680 мВ, для никеля -400мВ. Цинковое покрытие в сероводородсодержащей среде как без ионов хлора, так и при их наличии по отношению к стальной основе является анодным.
В сероводородсодержащих средах покрытия имеют высокий защитный эффект, что подтверждается данными по поляризационным сопротивлениям как без воздействия растягивающих нагрузок, так и при напряжении σ=1,1σ0,2 (табл.16).
Таблица 16
Значения поляризационного сопротивления покрытий в электролитах: числитель – раствор, содержащий 1200 г/л H2S;
знаменатель – раствор, содержащий 1200 мг/ л H2S+30 г/ л NaCl.
| Покрытие | Поляризационое сопротивление, Всм2/А | |
| σ = 0 | σ = 1,1σ02 | |
| Алюминиевое | 3,5 ·104 1,53 ·104 | 2,4 ·104 1·104 |
| Кадмиевое | 2,5 ·104 6,0·104 | 2,25 ·104 1,2·104 |
| Никелевое | 1·104 1,5·103 | 2,2 ·102 2,1 ·102 |
| Цинковое | 7·104 5,8·104 | 2,8. 104 2·10 4 |
| Сталь 40Х без покрытия | 8·102 2·102 | 3,5·102 1,4·102 |
Наиболее высоким поляризационным сопротивлением в растворе H2S (1200 г/л) обладает цинковое покрытие. Поляризационное сопротивление уменьшается от цинкового к алюминиевому, кадмиевому, никелевому покрытиям. Наложение растягивающих напряжений облегчает анодный и катодный процессы, потенциал для всех покрытий сдвигается к более отрицательным значениям. Алюминиевое, цинковое, кадмиевое покрытия сохраняют высокий защитный эффект при воздействии растягивающего напряжения σ = 1, 1σ0 2, вызывающего малые пластические деформации, тогда как никелевое, обладающее значительной хрупкостью, снижает сплошность покрытия из-за его растрескивания; при этом наблюдается резкое разблагороживание потенциала. Присутствие хлор-ионов снижает степень анодного и катодного контроля, однако сохраняется достаточно высокий защитный эффект. В этой среде поляризационное сопротивление кадмиевого покрытия увеличивается в 2–2,5 раза, в то время как для других покрытий оно уменьшается. Общий вид зависимостей времени до разрушения образцов от растягивающих напряжений (рис.54) одинаков для всех образцов с различными покрытиями, и по мере увеличения защитного эффекта сдвигается параллельно в сторону увеличения σ/ σотр.
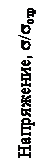
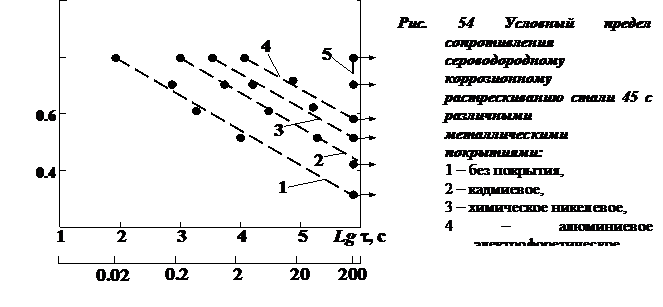
По росту защитного эффекта в условиях сероводородного коррозионного растрескивания при базе испытаний, равной 200 ч, покрытия располагаются в ряд: Cd, Ni, A1. Ниже (табл.17) приведены данные по условному пределу сероводородного коррозионного растрескивания на базе 200 ч и времени до разрушения при σотн = 0,7σотр и σотн = 0,8σотр
Таблица 17
| Без покрытия | Кадмиевое | Никелевое | Алюминиевое | |
| Время до разрушения, ч | ||||
| σ=0,7σотр | 8,5 | |||
| σ=0,8 σотр | 1,5 | |||
| Условный предел сероводородного коррозионного растрескивания | ||||
| σ/σотр | 0,3 | 0,4 | 0,5 | 0,6 |
Металлические покрытия могут наноситься и формироваться различными способами.
Нанесение металлических покрытий погружением в расплав является самым старым, простым и дешевым методом, но оно имеет некоторые ограничения: металл или сплав для покрытия должен плавиться при относительно низкой температуре, а металл подложки при этой температуре не должен претерпевать нежелательных изменений свойств. Методом горячего погружения наносят покрытия преимущественно из алюминия, цинка, олова, свинца. Покрытия наносятся на стали различных составов, чугуны и др.
Металл подложки и жидкий металл покрытия взаимодействуют, образуя промежуточный слой – интерметаллиды. Для влияния на природу и количество интерметаллидного слоя в ванну жидкого металла покрытия добавляют различные вещества: в ванну для алюминирования – кремний, для цинкования – алюминий.
Плакирование является одним из самых распространенных способов получения биметаллического материала и применяется в основном для нанесения защитных покрытий на стальные листы и трубы. В качестве плакирующих материалов используют цветные металлы – алюминий, цинк, олово, а также легированные стали ОХ13, Н18Н9Т и др. Обычно толщина плакирующего слоя составляет 1–5 % от толщины листа.
Плакирование производится механотермической обработкой путем совместной прокатки плакирующего материала с основой в виде листа или плиты, или прессованием при плакировании труб или проволоки. Эффективным способом плакирования является получение покрытий методом взрыва. Соединение стали с плакирующим металлом методом взрыва осуществляется при непосредственном контакте взрывчатого вещества с составляющими биметалла, в результате чего импульс высокой энергии, возникающей во время детонации взрывчатого вещества, не рассеивается, а оказывает концентрированное действие на металл в зоне соударения.
Разработана технология получения биметаллического листа при равном соотношении толщин слоев до 10 мм. Биметаллические листы Х18Н9Т–АМг6 имели механические свойства: σв = 550–640 МПа, σт = 400–500 МПа, δ = 15–20 %, прочность сцепления слоев σсц = 100 МПа, σср = 50 МПа. Высокое относительное удлинение обеспечивает возможность их гибки, штамповки, формовки. Теплопроводность биметалла нержавеющая сталь–алюминий примерно в 5 раз больше, чем нержавеющей стали. Примечательно, что при воздействии растягивающих напряжений в коррозионно-активных средах на биметаллическом материале Cт3 - Х18Н9 трещина распространяется только на глубину плакирующего слоя и останавливается.
Известна технология получения сваркой взрывом би- и три-металлических переходников и труб (Х18Н9Т–АД1) и (Х18Н9Т– АД1–АМг6), позволяющая обеспечить прочность сцепления стали марки Х18Н9Т и алюминия АД1 на отрыв не менее 50 МПа.
Электрохимические методы реализуются при формировании покрытий тремя различными способами:
- электроосаждение из водных растворов (гальванический метод);
- электроосаждение из расплавов солей или органических жидкостей;
- электрофоретический способ.
Гальваническое осаждение зачастую более экономично, чем другие способы нанесения покрытий. Этот способ позволяет получать сравнительно равномерный слой с заданным химическим составом, высокими механическими и коррозионно-защитными свойствами.
При гальваническом методе покрываемая деталь завешивается в электролитической ванне на катоде. Основным катодным процессом является восстановление ионов металла из раствора до металлического состояния и образование на подложке прочносцепленного компактного покрытия. Если коррозионная стойкость покрытия определяется его пассивностью, то обычно после нанесения гальванического покрытия наносится конверсионное, упрочняющее пленку. Цинковые, кадмиевые, оловянные покрытия обрабатываются растворами хроматов, в результате чего происходит упрочнение защитных окисных пленок.
Толщина гальванических покрытий является весьма важным параметром, определяющим его коррозионную стойкость. В некоторых случаях толщина покрытия имеет функциональное значение, например, в случае ограничения на допуск, как это имеет место для изделий с резьбой. На выступающих частях изделия, например, на углах, ребрах, выпуклостях, образуются более толстые покрытия, а в углублениях и более удаленных от анода участках детали, наоборот, покрытие получается более тонким. Гальваническое осаждение, как правило, более экономично, чем другие электрохимические способы, и поэтому применяется более широко.
Электроосаждение из расплавов солей или органических жидкостей применяется для получения покрытий из металлов, в том числе алюминия, которые не могут быть осаждены из водных растворов солей вследствие высокого отрицательного нормального потенциала.
При электрофоретическом способе формирование покрытий происходит так же, как при электролитическом осаждении, под действием постоянного тока, но более высокого напряжения (50–500 В), в диэлектрическом растворе, содержащем диспергированные частицы осаждаемого вещества.
Термодиффузионный способ получает все большее применение благодаря существенным достоинствам – большой прочности сцепления с основой, плавному снижению концентрации наносимого вещества по глубине покрытия, что обеспечивает менее резкое изменение свойств при переходе от покрытия к основе, возможность повышения коррозионной стойкости, жаростойкости, жаропрочности, износостойкости конструкционных материалов. Наибольшее распространение в нашей стране и за рубежом нашли способы: диффузионного алитирования, хромирования, борирования и в меньшей степени силицирование, титанирование.
Для нефтегазовой промышленности большое значение имеет алитированная сталь, получаемая химико-термической обработкой с образованием на поверхности стали диффузионного слоя, богатого алюминием. Наиболее характерной особенностью алитированной стали является ее высокая жаростойкость, которая в десятки раз превышает таковую у неалитированной стали. Трубы из алитированной стали нашли большое применение в промышленности в трубных печах, в теплообменной и конденсационной аппаратуре. Алитированная сталь при температурах 500–600 °С успешно конкурирует с нержавеющей сталью типа 18–8 в средах, содержащих сероводород. При толщине алити-рованного слоя 0,2 мм предел усталостной прочности снижается на 45–50 %; при толщине слоя 0,1 и 0,045 мм снижение предела усталости составляет 35 и 15 % соответственно. Применение алитированных труб на установке обессеривания нефти, где обрабатываемый продукт содержал 10–15 % сероводорода и поступал по трубам при температуре 345–400 °С под давлением 490 МПа, показало, что потеря массы по сравнению с трубами из хромомолибденовой стали (9 % Сг, 1 % Мо) оказалась на порядок меньше, а также увеличился срок службы алитированных труб, который составлял для хромомолибденовых труб не более 196 ч.
Диффузионное алитирование обеспечивает низкоуглеродистой стали сравнительно высокую коррозионную стойкость в атмосфере, содержащей сернистый газ, в 3%- ном растворе NaCl, в морской атмосфере и при погружении в морскую воду. В морской воде коррозионная стойкость алитированной стали значительно лучше оцинкованной, что связано с известной способностью алюминия самопассироваться за счет кислорода, растворенного в воде.
В сероводородсодержащей среде (2,5 г/л H2S + 3 % NaCl) стационарный потенциал диффузионных покрытий определяется основными насыщающими элементами. Хромовые и боридные покрытия – катодные по отношению к стали, алитировенные и цинковые покрытия -- анодные.
В табл.18 приведены результаты испытаний стальных образцов с диффузионными покрытиями на сероводородное коррозионное растрескивание.
Таблица 18
| Тип покрытия | Без покрытия | Покрытие | |||
| боридное | алитированное | цинковое | хромированное | ||
| Условный предел сопротивления СКР, σотн | 0,28 | 0,4 | 0,48 | 0,52 | 0,55 |
| Время до разрушения, мин, при σ=0,1σотр | 8,5 |
Видно, что лучшей защитной способностью по сравнению с другими исследованными покрытиями обладает диффузионно-хромированное. Это объясняется наличием в наружной зоне хромированного покрытия слоя карбидов состава (Сr, Fe)23C6 или (Сr, Fe)7C3 переходного слоя из обогащенного углеродом аустенита и обезуглероженной зоны. В результате встречной диффузии хрома и углерода образуется непрерывный карбидный барьер, эффективно блокирующий дальнейшую диффузию водорода в металлическую основу.
Эффективность термодиффузионного хромирования существенно зависит от содержания углерода в стали. Целесообразно подвергать диффузионному хромированию лишь стали, содержащие не менее 0,4–0,5 % С. Доля хрома на поверхности диффузионно-хромированной стали достигает 70–80%, что значительно выше, чем его содержание в кислотостойких хромистых сталях и определяет ее стойкость в различных кислотах – серной, азотной, фосфорной и др.
Сталь, хромированная электролитическим методом, обнаруживает более низкую стойкость против сероводородного коррозионного растрескивания, чем сталь с термодиффузионным покрытием. Это связано с высокой растворимостью водорода в электролитическом хромовом покрытии
При наличии в сероводородсодержащем потоке абразивных частиц резко возрастает доля механического фактора в общем процессе разрушения покрытия. Особенно резкое возрастание механического фактора наблюдается у цинкового покрытия, у которого при скорости потока с абразивом более 2 м/с доля влияния механического фактора составляет 88 %. Доля коррозионного фактора мала в силу относительно высокой коррозионной стойкости цинковых диффузионных покрытий в сероводородсодержащих растворах. У боридных диффузионных покрытий высокая износостойкость, но низкая коррозионная стойкость в сероводородсодержащих средах. По возрастанию суммарных потерь массы диффузионные покрытия располагаются в ряду в сероводородсодержащем потоке электролита с абразивом: хромовое - алюминиевое - боридное - ст 45 без покрытия - цинковое; в том же потоке электролита, но без абразива расположение диффузионных покрытий в возрастающем ряду иное: хромовое - цинковое - алюминиевое - боридное - ст45 без покрытия.
Металлизация осуществляется путем напыления на основу наносимого вещества газопламенным, электродуговым или плазменным способами. Ниже приведена некоторые характеристики газотермических напыленных покрытий (табл.19).
Таблица 19
Характеристика газотермических напыленных покрытий
| Метод напыления | Температура газовой струи,K | Скорость напыляемых частиц,м/с | Пориcтость,% | Прочность сцепления, МПа |
| Газопламенный | до 150 | 15-30 | ||
| Электродуговой | 4000-10000 | до 150 | 10-20 | 10-20 |
| Плазменный | 10000-20000 | до 600 | 2-10 | до 40 |
К достоинствам металлизации относится возможность покрывать детали и конструкции значительных размеров в полевых и эксплуатационных условиях, способ металлизации сравнительно дешевый. Плазменный способ напыления позволяет наносить тугоплавкие металлы, оксиды, карбиды, нитриды, бориды и композиции на их основе.
В соответствии с технологическими особенностями металлизационное покрытие является пористым, причем наибольшая пористость присуща покрытию, полученному газоплазменным способом, наименьшая – плазменным. Металлизационные покрытия применяются в основном для защиты от атмосферной коррозии и могут быть использованы также для восстановления размеров изношенных деталей. Влияние пористости может быть уменьшено механическим способом (крацовкой) или заполнением лаком и др. Пористость можно уменьшить увеличением толщины покрытия, однако одновременно повышается его хрупкость. Оптимальной считается толщина металлизационного покрытия 0,15–0,30 мм. При большей толщине покрытие может отслоиться от основы. Это связано с тем, что в процессе формирования покрытия не происходит значительного повышения температуры основы, а охлаждающиеся частицы напыляемого материала сокращаются в размерах в большей степени, чем металл основы. В результате при нормальной температуре в напыленном покрытии возникают остаточные касательные напряжения, которые могут привести к образованию трещин в напыленном слое или его отделению от основы. Так, например, для газопламенного накелевого покрытия толщиной 0,5 мм на стали касательные напряжения достигают 20 МПа. Металлизация покрытий напылением имеет и другие надостатки. Сила сцепления покрытия с основой небольшая, покрытие имеет низкую пластичность, поэтому исключается возможность деформирования изделий; металлизационное покрытие имеет грубую поверхность, неравномерную толщину и химический состав, в процессе напыления имеет место большая потеря металла (15–20 %).
Вместе с тем, металлизация по сравнению с другими способами нанесения покрытий обладает высокой мобильностью и простотой аппаратурного оформления, что особенно важно для нанесения покрытий на габаритные изделия.
Для защиты от коррозии наиболее широко используют покрытия алюминием и цинком, которые являются анодами в большинстве коррозионно-активных сред. По физическим свойствам алюминиевые покрытия имеют ряд преимуществ перед цинковыми (табл. 20).
Таблица 20
| Материал покрытия | Плотность, г/см3 | Масса покрытия, кг/м2 при толщине 0,025 мм | Твердость, НВ |
| Цинк | 6,35 | 0,159 | 20-28 |
| Алюминий | 2,35 | 0,059 | 25-35 |
Напыленный цинк при толщине 30 мкм приобретает стабильный отрицательный потенциал по отношению к стали и обеспечивает надежную протекторную защиту. Цинковые покрытия толщиной 80 – 350 мкм успешно используются в промышленности для защиты стальных конструкций от воздействия атмосферы, пресной и соленой воды. Скорость коррозии цинкового покрытия возрастает при увеличении влажности атмосферы, особенно в присутствии кислых газов. В природных водах цинковые покрытия имеют ограниченный срок службы вследствие высокой скорости анодного растворения в контакте со сталью, достигающей 0,05 – 0,1 мм/год.
Для улучшения протекторных свойств цинкового протектора в его состав можно вводить Ag (до 0,5%), Cd (до 0,15%), Hg, In и др.
Алюминиевые покрытия предпочтительно применяют для защиты конструкций, работающих в промышленной атмосфере, морской и пресной воде при повышенной температуре, так как степень протекторной защиты стали алюминиевыми покрытиями возрастает при увеличении в растворе ионов хлора и температуры. При концентрации ионов хлора менее 0,1 г/л в области температур 293 – 313К протекторное действие покрытия практически отсутствует и оно подвергается питтинговой коррозии. Алюминиевые покрытия, как правило, характеризуются тремя периодами электрохимического действия. Первоначально несколько месяцев они ведут себя как катод из-за частичной пассивации алюминия. Затем щелочность у катодных участков повышается, пассивная пленка на алюминии разрушается с образованием алюминатов, потенциал покрытия разблагороживается и покрытие становится анодным. В третьем периоде происходит блокирование пор продуктами коррозии алюминия, и покрытие в отсутствии макронесплошностей защищает сталь барьерно. Активации алюминиевых покрытий способствует закалка, приводящая к межкристаллитной коррозии и увеличению активной поверхности протектора. Однако, более эффективным является легирование алюминиевых покрытий Na (0,1%), Ca (до 3,5%), Mg (1,0%), Sn (1,0%) или Zn (до 10%). С целью улучшения условий напыления алюминиевых покрытий и их активации в состав шихты вводятся солевые композиции, оказывающие флюсовое действие на алюминий. В качестве флюсующих добавок используются хлориды щелочных и щелочноземельных металлов, которые обычно используются как основа флюсовых добавок при сварке, пайке и рафинировании алюминия.
Низкотемпературные флюсы способствуют созданию микропористой структуры покрытия и свариванию частичек алюминия между собой, а также повышению прочности сцепления покрытия со стальной основой. Применение натрийсодержащих флюсов снижает пористость металлизационных алюминиевых покрытий до 5 % при исходной пористости электрометаллизационных покрытий 10–15 %.
Введение в шихту для напыления алюминиевого покрытия хлоридов щелочных и щелочноземельных металлов способствует и активирующему действию на металлизационное алюминиевое покрытие – анодная поляризация покрытия уменьшается, а ток и дальнодействие протекторной защиты увеличиваются. Введение в состав натрийхлоридного флюса жидкого стекла способствует дальнейшему улучшению протекторных свойств покрытия и позволяет повысить критическую деформацию композиции до 2 %. Протекторные характеристики напыленного модифицированного алюминиевого покрытия с хлоридно-силикатным активатором в значительной степени определяются соотношением компонентов шихты. Анализ поляризационных диаграмм “покрытие - основа” показывает, что электродный потенциал, степень анодного контроля и ток протекторной защиты, независимо от теплофизических условий на поверхности металла, имеют оптимальные значения при содержании жидкого стекла в шихте 2,5 – 3,5% с модулем от 1,6 до 2, NaCl 3-4% и AlCl3 от 1,5 до 2%.
Модифицирование хлоридно-силикатного флюса тетраборатом, молибдатом и вольфраматом натрия в количестве 1-1,5% приводит к улучшению протекторных свойств напыленного алюминиевого покрытия. При этом снижается анодная поляризуемость покрытия и отмечается ингибирующее воздействие компонентов активатора на продукты коррозии стали. Оксиды бора и молибдена значительно повышают катионообменные свойства алюмосиликатного активатора.
Алюминиевые и цинковые покрытия значительно повышают срок службы металлических конструкций от атмосферной коррозии. В табл. 21 приведены данные по минимальной долговечности покрытий в условиях атмосферной коррозии.
Таблица 21
| Покрытие | Толщина, мкм | Характеристика атмосферы | |
| средняя | жесткая | ||
| Цинковое | |||
| Алюминиевое | |||
В промышленных атмосферах, загрязненных сероводородом, сернистым газом и др., алюминиевые покрытия более стойки по сравнению с цинковыми. Эффективность защиты стали в атмосфере влажного сернистого газа увеличивается в 7–8 раз, в морской атмосфере – в 6–7 раз. Так при испытании в течение 18 мес. алюминиевых и цинковых покрытий в атмосфере Оренбургского ГПЗ, отличающейся высоким содержанием сероводорода и сернистого газа скорость коррозии алюминиевого покрытия составила 0,01г/м2ч, цинкового – 0,08 г/м2ч, а стали ст5 без покрытия – 9 г/м2ч.
С целью уменьшения расхода протектора большое значение имеет повышение катодной поляризации защищаемой стали, что способствует уменьшению величины защитного тока и скорости гальванического растворения протектора при адекватном защитном эффекте, при этом увеличивается радиус дальнодействия протекторной и катодной защиты. В природных водах увеличению катодной поляризации способствуют образующиеся катодные солевые осадки (КСО), состоящие в основном из CaCO3 и Mg(OH)2. Формирование КСО происходит за счет участия ионов кальция и магния в углекислотно-карбонатном равновесии природных вод и смещения его в сторону образования нерастворимых солевых отложений на катодных участках вследствие протекания катодной электрохимической реакции восстановления молекулярного кислорода, приводящей к повышению рН пограничного слоя до 9 –11. Образованное таким образом солевое покрытие выполняет барьерные функции, препятствует диффузии молекулярного кислорода к корродирующей поверхности и увеличивает катодную поляризацию стали. При этом качество и физико-химические свойства КСО определяют параметры электрохимической защиты и состав воды. Однако самопроизвольное образование карбонатных осадков приводит к уменьшению проходного сечения труб, а для теплообменного оборудования еще и к увеличению термического сопротивления и ухудшению процесса теплопередачи.
Для защиты от коррозии водоохлаждаемых систем разработано оригинальное цинк-карбонатное покрытие. Цинк наносится металлизацией (плазменным, электродуговым, газотермическим способами) на стальную поверхность с последующим формированием на покрытии катодно-солевых осадков (КСО). Рентгеноструктурным анализом показано, что пленки КСО в основном состоят из кристаллогидрата СаСО3-6Н2О.
Формирование цинк-карбонатных покрытий может производиться различным методами:
- обработкой изделия с напыленным цинковым покрытием известковым раствором. При этом образование фазы КСО происходит при карбонизации Са(ОН)2 атмосферной двуокисью углерода и одновременной кристаллизацией СаСО3 на катодной поверхности образующегося во влажной пленке гальванического элемента «покрытие–основа»;
- сдвигом карбонатного равновесия в сторону образования карбоната кальция.
Образование КСО осуществляется на катодных участках в местах несплошности покрытия, а также в его порах. Тем самым происходит уплотнение покрытия и достигается практически полная изоляция стальной подложки от внешней среды. Обратного растворения солевой фазы в цинк-карбонатном покрытии не происходит, так как она обладает свойством саморегуляции и самовозобновления воды, заключающимся в том, что в местах наибольшей катодной плотности тока происходит преимущественное формирование солевых осадков. Это приводит к залечиванию мест разрушения солевого покрытия и его уплотнению. Увеличение катодной поляризуемости стали способствует ее катодной поляризации на линии дренажа и уменьшению анодной поляризации цинкового покрытия на границе контакта, чем предотвращается тангенциальное растворение протектора там же. Для дискретных покрытий с переменным профилем сохраняется термомеханическая устойчивость покрытия.
Внедренный в состав покрытия карбонат кальция оказывает активирующее действие на цинк и снижает степень анодного контроля. Защитное действие цинк-карбонатного покрытия при повышении температуры воды до 343 К практически не изменяется, тогда как при отсутствии КСО у цинкового покрытия нагревание приводит к интенсивному снижению защитного действия на сталь. С ростом экспозиции для цинк-карбонатного покрытия характерно повышение защитного действия, в то время как для немодифицированного цинкового покрытия защитный эффект во времени снижается вследствие тангенциального растворения покрытия. Скорость растворения цинк-карбонатного покрытия не превышает 5–15 мкм/год. Применительно к теплообменному аппарату оно может обеспечить эксплуатацию в течение срока амортизации (10 лет) без возобновления покрытия, то есть обеспечить работу оборудования до его морального износа. Термическое сопротивление, обусловленное наличием пленок КСО, практически не уменьшает коэффициента теплопередачи по сравнению с чистой поверхностью стали, тогда как в процессе коррозии незащищенных теплообменных труб коэффициент теплопередачи уменьшается в аналогичных гидродинамических условиях на 40 – 70%.
Неметаллические покрытия
Механизм защитного действия неметаллических покрытий связан как с изолирующим действием, так и с влиянием на электрохимические процессы, протекающие под неметаллической пленкой. Поэтому защитные свойства полимерных покрытий определяются суммой физико-химических характеристик, таких как:
- способность пленок замедлять диффузию и перенос коррозионных реагентов к металлической поверхности;
- электрохимические свойства покрытий;
- способность покрытий, содержащих пигменты или ингибиторы, пассивировать или электрохимически защищать металл;
- адгезионные и механические свойства покрытий.
Потому индивидуальные характеристики покрытий, такие как адгезия,сколь высокого значения она бы не достигала, или диффузионные ограничения, не могут обеспечить длительную эффективную защиту металла.
Экранирующее действие неметаллических покрытий обусловлено их способностью замедлять диффузию и перенос через покрытие компонентов коррозионно-активной среды к поверхности металла и определяется в значительной степени пористостью покрытий. Проникновение электролита через поры покрытия или межмолекулярные несовершенства пленкообразующего вещества (в процессе теплового движения) происходит под действием капиллярных сил. Осмотическое давление, возникающее вследствие перепада концентрации электролита на поверхности капиллярной пленки, контактирующей с внешней средой и прилегающей к защитному металлу, способствует диффузии среды через покрытие. При осмотическом перемещении влаги через пленку давление может быть больше, чем сила адгезии пленки к металлу, в результате чего происходит локальный отрыв пленки от поверхности металла, что приводит к образованию вздутий и пузырей, являющихся первоначальным очагом коррозионного поражения металлической основы.
Однако за счет чисто осмотических явлений через покрытие переносится небольшое количество, около 10%, электролита к поверхности металла, а основную роль в этом переносе играет электроосмотическое проникновение жидкости.
На скорость и направление электроосмотического переноса влаги через покрытие оказывает влияние знак электрического заряда на стенках капилляра пленки. Электроосмотическая активность пленки снижается с уменьшением величины заряда. Электроосмотическое проникновение воды и растворенных в ней веществ заметно увеличивается под влиянием градиента потенциала окрашенной поверхности, обладающей электрохимической гетерогенностью.
Скорость диффузии воды и кислорода через различные полимерные пленки находится в следующих пределах:
вода 0,190 – 1,122 г/ (см2 ∙ год),
кислород 0,004 – 0,050 г/ (см2 ∙ год).
То есть вода и кислород могут проникать через полимерные покрытия с такой скоростью, что коррозия могла бы развиваться на стальной поверхности под покрытием с такой же скоростью, как и на незащищенной поверхности. Однако этого не происходит из-за затрудненности отвода продуктов коррозии – ионов железа через пленку полимерного покрытия в раствор, что, вероятно, связано с большим размером иона железа (Fe3+ ) и его большим зарядом. Кроме того, Fe3+, внедряясь в адсорбционную часть двойного слоя, может сообщать ей больший заряд, что приведет к изменению количества катионов в диффузионной части слоя, а в результате – к уменьшению электрокинетического потенциала и к уменьшению избирательной проводимости, то есть способности не в одинаковой степени пропускать через себя ионы различного знака. Диффузионные свойства полимерных покрытий и их ионная проницаемость зависят от природы, структуры полимера и свойств покрытия. Наличие преимущественно катионной проводимости указывает на то, что полимерная пленка обладает отрицательным зарядом. А преимущественно анионная проводимость свидетельствует о положительном заряде пленки. Ионная проводимость у некоторых полимеров может существенно изменяться с изменением рН среды. Так, например, у сополимера винилхлорида с винилиденхлоридом (СВХ-40) наблюдается переход от преимущественно анионной проводимости в кислой области рН электролитов к преимущественно катионной – в щелочнолй области рН, тогда как у пленок из хлорированного поливинилхлорида (ПСХ 0) и нитроцеллюлозы зависимость типа проводимости от рН электролита выражена слабо.
Покрытия на основе линейных полимеров с волокнистой структурой имеют более высокую проницаемость, чем на основе полимеров, образующих кристаллическую структуру.
| Покрытие | Эпоксидная шпатлевка ЭН-0010 | Эпоксидная порошковая краска П-ЭП-117 | Полиэтилен высокого давления | Пенопласт |
| Коэффициент проницаемости, (гּсм)/(см2ּс) | 9,98ּ10–12 | 6ּ10–12 | 6,2ּ10–13 | 1,42ּ10–13 |
Эти данные показывают, что время диффузии мало по сравнению со сроком эксплуатации полимерных покрытий, поэтому решающая роль принадлежит не экранирующей функции пленки, а электрохимическому поведению металла под покрытием.
В зависимости от природы вводимых компонентов механизм защитного действия неметаллических покрытий связывают с влиянием их на протекание электрохимических реакций: с пассивирующим действием на покрываемый металл, обеспечением за счет вводимых компонентов катодной защиты, образованием труднорастворимых продуктов коррозии, которые снижают скорость диффузии агрессивного агента к металлу.
Эффективным методом улучшения защитной способности неметаллических покрытий является повышение адгезионной связи покрытия с основой. Высокая прочность сцепления покрытия с металлом обеспечивается за счет хемосорбционный связи при взаимодействии активных функциональных групп как самих пленкообразующих, так и отвердителей, вулканизаторов, модифицирующих добавок с активными центрами поверхности металла.
При этом снижается вероятность адсорбции ионов электролита, проникающего через поры к поверхности металла, затрудняется реакция ионизации металла, хемосорбционная пленка препятствует образованию продуктов коррозии, приводящих к снижению адсорбционной связи.
Величина адгезионной связи покрытия с металлом зависит прежде всего от наличия полярных функциональных групп. Покрытия на основе фенолформальдегидных, алкидных, эпоксидных смол имеют активные функциональные группы и обладают более значительной прочностью сцепления, чем покрытия на основе полиэтилена, пентапласта, фторопласта, в то время как их сопротивление потоку электролита и водопоглощению незначительно. Защитный эффект усиливается ингибирующим действием компонентов, приводящих поверхность металла в адсорбционно-пассивное состояние.
Таблица 22
| Типы смол и отвердители | Близкое по химической структуре органическое соединение | Функциональные группы |
| Дивинилацетиленовый лак этиноль | Производные пропаргилового спирта | Ненасыщенная ацетиленовая связь |
| Поливинилпиридиновые смолы | Винилпиридин | Атом азота в гетероцикле |
| Эпоксидные смолы | Окись этилена, пропилена | Гетероатом кислорода в эпокси-группах |
| Каменноугольные смолы | Производные пиридина, хинолина | Атомы азота в гетероциклах компонентов каменноугольной смолы |
| Сополимеры алифатических соединений с карбоновыми кислотами (стирол с малеиновым ангидридом) | Малеиновая кислота | Карбоксильные группы |
| Отвердители | Гетероциклические амины: пиридины, пиперазин, пиперадин, пирролидин, морфолин, анабазин и их производные. | Гетероатом азота в цикле |
| Отвердитель | Мочевина, меламин, имидазолы, интрозамины | Гетероатомы азота, аминогруппы |
| Вулканизирующие агенты | Тиазолин меркаптоимидазалин, меркаптобензотиазол | Гетероатомы азота и серы |
Для покрытий, характеризующихся отсутствием явно выраженных функциональных групп (полиэтилен, пентопласт, фторопласт), образование хемосорбированной адгезионной связи полимера с металлом может достигаться оптимальным режимом термической обработки, а так же за счет химического модифицирования поверхности, приводящего к повышению стабильности адгезии в воде и электролитах.
Повышение пластичности способствует сохранению защитных свойств покрытий в условиях знакоперемещенных и растягивающих нагрузок в электролитах, в том числе и вызывающих наводороживание. При этом важна способность покрытий сохранять свою эластичность в процессе длительной эксплуатации и при изменении температур.
Введение в покрытие ингибирующих добавок, растворимых в воде, приводит к их адсорбции на активных центрах металла под пленкой покрытия. Однако в этом случае снижаются барьерные функции пленки за счет вымывания водой добавок, происходит усиление осмотического явления, а также может снижаться адгезионная связь пленок с металлом в результате конкурентной адсорбции ингибитора и функциональных групп полимерной пленки.
Совмещение полимерных материалов различных классов и создание многослойных систем позволяют обеспечить долговременную защиту оборудования. Наиболее перспективное направление повышения эффективности антикоррозионных полимерных покрытий – это разработка полимерных композиций адгезионно - ингибирующего действия, компоненты которой обеспечивают прочную хемосорбционную адгезионную связь с поверхностью металла в процессе формирования полимерного слоя и ингибирующее действие в процессе эксплуатации покрытия.
О пористости полимерных покрытий, их защитных свойствах и кинетике разрушения, то есть потере защитных свойств, можно судить по таким характеристикам, как величина и характер изменения емкости, сопротивления, тангенс угла диэлектрических потерь и их частотной зависимости. Сопротивления омическое и поляризационное характеризуют защитные свойства покрытий. При этом для пигментированных покрытий основное значение имеет поляризационное сопротивление. Количественно величины омического и поляризационного сопротивлений можно определять в электролите при постоянном токе осциллографическим методом, который был разработан в институте Физической химии РАН. Для пористых покрытий по времени поляризации можно определить площадь пор, а для непористых покрытий, через которые перенос ионов и воды совершается по самому материалу и временным, скрытым порам – “условную пористость”, эквивалентную активной части поверхности.
Другой характеристикой защитной способности покрытий является емкость окрашенного электрода. Если само по себе покрытие не набухает и его диэлектрическая постоянная не меняется, то она может характеризрвать пористость покрытия. Если же покрытие набухает, то диэлетрическая постоянная характеризует объем абсорбированной воды. По изменению дисперсии емкости окрашенного электрода с частотой переменного тока можно определить характер покрытия и что с ним происходить под воздействием электролита. Так, если емкость не зависит от частоты переменного тока, то покрытие сплошное, с плотной структурой, а измеряемая емкость является электрической. Если наблюдается сильная зависимость измеряемой емкости от частоты тока, то в этом случае измеряется электрохимическая емкость пористого покрытия.
Тангенс угла диэлектрических потерь представляет собой произведение емкости (Спосл), сопротивления (Rпосл) и частоты переменного тока:
tgδ = 2π / Cпосл Rпосл = 1 / 2πCпар Rпар,
где Cпосл, Rпосл, Cпар, Rпар – емкости и сопротивления, измеренные соответственно по последовательной и параллельной схемам.
Чем выше изоляционные свойства покрытия, тем больше тока будет расходоваться на зарядку конденсатора и тем меньше оно будет пропускать тока; у такого покрытия tgδ будет небольшим. Изменение tgδ со временем при воздействии на покрытие электролита характеризует снижение защитных свойств покрытия. Таким образом, стабильность частотной зависимости исходных значений емкости и сопротивления указывает на то, что данное покрытие не набухает, не разрушается, сохраняет адгезию и защитные свойства.
Полимерные покрытия широко применяются для защиты от коррозии металлоконструкций и оборудования производственных объектов нефте- и газоперерабатывающих заводов.
Формирование противокоррозионной защиты с использованием полимерных материалов производится в следующий последовательности: удаление ржавчины с поверхности металлоконструкции, ее пескоструйная очистка, обезжиривание бензином Б-70 или уайт-спиритом, нанесение системы покрытий, последующая выдержка покрытия в течение 7 суток до пуска в эксплуатацию.
Так, например, эпоксидные покрытия применяются для защиты от коррозии изготовленных из углеродистой стали емкостей орошения атмосферных колонн, емкостей орошения стабилизационных колонн, барометрических емкостей установок первичной переработки нефти.
Электрохимическое исследование комбинированных систем, состоящих из слоев грунтовки и лака, показало, что грунтовка или лак не могут сами по себе каждый в отдельности обеспечить надежную защиту металла от коррозии из-за слабых барьерных свойств или из-за отсутствия пассивирующих агентов и более слабой адгезии. При наличии комбинированной системы они усиливают друг друга.
Характеристика защитных свойств некоторых полимерных покрытий для различных условий эксплуатации металлических элементов градирен приведена в табл. 23.
Таблица 23
| Металлические элементы градирен | Условия эксплуатации | Система покрытий | Состояние покрытия за время эксплуатации |
| Металлоконструкция лестниц и ограждений | Слабоагрессивная среда: промышленная атмосфера повышенной влажности. Температура окружающей среды от –40 до +400С. | По одному слою грунтовки ВЛ-02, ФЛ-03К или ГФ-021, два слоя эмали ХС-416, ХС-413 или ХС-717 | Посветление покрытий через 24 месяца |
| Стояки подачи воды, наружная поверхность диффузоров. | Слабоагрессивная среда: промышленная атмосфера повышенной влажности, туман, пары и брызги оборотной воды, температура окружающей среды от –40 до +400С. | По двум слоям грунтовки ВЛ-02, ФЛ-03К или ГФ-021, два слоя эмали ХС-416, ХС-413, ХС-717. | Без изменений через 24 месяца |
| Вентиляционные установки, внутренняя поверхность диффузоров. | Сильноагрессивная среда: поток восходящего влажного воздуха, водяная пыль с растворенными солями, нефтепродуктами и микроорганизмами; постоянная конденсация влаги. Температура окружающей среды от +35 до –450С. | По одному слою грунтовки ФЛ-03К, ВЛ-02, ГФ-021 или ЭП-057, два слоя противокоррозионной эмали ЭП-44, ЭП-46, ХС-416 или ХС-717 и два слоя противобрастающей эмали ХС-519 или ХС-592. | Посветление покрытия через 36 месяцев |
| Водораспределительная система труб (наружная поверхность) | Сильноагрессивная среда: распыленная оборотная вода с растворенными минеральными солями, примесями нефтепродуктов, микроорганизмами. Восходящий поток воздуха, температура от +40 до-600С. | По одному слою грунтовки ВЛ-02 или двум слоям ЭП-057, три слоя эмали ЭП-44, ЭП-46, ЭП-773, ХС-413, ХС416 и один – два слоя противообрастающей эмали ХС-519 или Х-522 | Посветление покрытия через 36 месяцев |
В процессе эксплуатации на элементах градирен появляются слизистые образования, состоящие из простейших водорослей и различных видов микроорганизмов, которые вызывают как разрушение полимерных пленок, так и коррозию защищаемого металла. Использование систем с противообрастающими эмалями на основе виниловых пленкообразователей и канифоли (ХС-519, ХС-522, ХС-526) по противокоррозионным эмалям позволяет избавиться от обрастаний, что увеличивает срок службы лакокрасочных покрытий и металлоконструкций. Пленки этих покрытий после 2 лет испытаний только незначительно изменили цвет. Слизистые образования на вышеперечисленных образцах практически отсутствуют.
Покрытия на основе полимеров могут обеспечивать защиту стали от коррозии и в сероводородсодержащих средах. В табл.24 приведены данные по влиянию покрытий на основе эпоксидных смол на скорость коррозии стали 20 и количество адсорбированного водорода после экспозиции в 3%-ном растворе NaCl, насыщенном сероводородом при температуре 200С.
Таблица 24
Скорость коррозии и количество адсорбированного водорода сталью 20
в сероводородосодержащем электролите.
| Полимерное покрытие | Скорость коррозии, мм/год, за время испытаний, сут. | Количество адсорбированного сталью водорода, см3/100г., при растягивающем напряжении | ||
| σ = 0,96σт | ||||
| Сталь без покрытия | 0,28 | 0,134 | 1,36 | 3,55 |
| Эпоксидный компонент П-ЭП-177 ЭП-00-10 | 0,0062 0,0368 | 0,05 0,13 | 0,53 0,71 |
Защитный эффект композиций на основе эпоксидных смол связан в основном с высокой адгезионной способностью к стали этой группы полимеров. Прочная хемосорбционная связь покрытий со сталью происходит за счет гетероатома кислорода в эпокси-группах и гетероатома азота в отвердителе
 2018-01-08
2018-01-08 2423
2423