Расплав флюса гасит дугу, и процесс автоматически переходит в электрошлаковый, при котором тепло выделяется за счет электросопротивления шлака. Электрод из обычной стали расплавляется в шлаке и капли 11, проходя через слой шлака 10, очищаются от примесей и скапливаются под шлаком в виде ванночки 12, питающей растущий вверх слиток 13.
Вакуумно-дуговой переплав (рис. 11.9, г) внешне похож на электрошлаковый, но расплавленный металл не проходит через слой шлака; между ванночкой расплавленной стали и расходуемым электродом постоянно горит электрическая дуга 15. Очистка, в основном от газов и частично от неметаллических включений, происходит под воздействием вакуума в камере 14 ив результате направленной кристаллизации слитка 13 снизу вверх.
Производство меди
В земной коре содержится около 0,01 % меди. Обычно это сульфидные руды, состоящие из смеси CuS, Cu2S и FeS. Среднее содержание меди в рудах менее 3 %, пустая порода состоит из песка, глины и известняка. В связи с низким содержанием меди руды подвергаются обогащению.
Извлечение меди из руд производится двумя способами: пи- рометаллургическим и гидрометаллургическим. Первый чаще применяется для сульфидных, а второй — для оксидных руд.
Общая схема пиро металлургического способа получения меди приведена на рис. 12.1. Как следует из схемы, перед обогащением руда измельчается. Наиболее приемлемым методом обогащения медных руд считается флотация. Смесь измельченной руды с водой, называемая пульпой 2, загружается в чаны 1 и продувается сжатым воздухом. Пузырьки воздуха 3 адсорбируют на своей поверхности несмачиваемые водой частицы руды 4, содержащие соединения металлов, и поднимают их на поверхность, образуя пену. Пустая порода смачивается водой и в виде шлама 5 оседает на дне чанов.
Пену снимают, сушат и получают концентрат, который перед плавкой спекается в обжиговых печах. Чаще других используется обжиг в кипящем слое, при котором концентрат 6 загружается на решетку 7, через которую снизу из топки 8 подается горячий воздух 9. При температуре свыше 600 °С происходит частичное удаление серы и спекание руды в комки, которые называют огарком.
| 12.1; |
| МЕТАЛЛУРГИЯ ЦВЕТНЫХ МЕТАЛЛОВ |
Огарок плавят в отражательных печах, куда он засыпается из бункеров 10. Печные газы 11 плавят огарок, перегревают расплав до 1600 °С и обеспечивают дальнейшее окисление FeS с образованием FeO и S02. Сплавляясь с пустой породой, FeO образует шлак 12, ниже которого располагаются более тяжелые сульфиды меди и железа, так называемый медный штейн 13.
| NJ 00 |

 |
| Руда ■ 3 % Си |
| а |
| ~ 20 % | ~ 30 % Fe ~ 50 % S |

| Огарок |
| Техническая медь ~ 99,5 % Си |
| ж Электротехническая медь |
| Штейн |
| Рис. 12.1. Схема пирометаллургического способа получения меди: а — измельчение руды; б — обогащение флотацией; в — обжиг руды; г — плавка огарка; д — конвертирование штейна; е — огневое рафинирование; ж — электролитическое рафинирование |
| ~ 25 % Си ~ 30 % Fe ~ 45 % S |

| (Fe0)2Si02 |
| ~ 35 % Cu ~ 30 % Fe ~ 35 % S |
| 16 IВоздух I. 2FeS + 302= 2FeO + 2S02 2FeO + Si02= (Fe0)2Si02 II. 2Cu2S + 302= 2Cu20 + 2S02 Cu2S + 2Cu20 = 6Cu + S02 |
| ~ 99,99 % Си |
2FeS + 302 = 2FeO + 2S02 2FeO + Si02= (FeO)2SiQ2A
Конвертирование штейна, содержащего около 35 % меди, 40 % железа в виде сульфидов и некоторое количество Si02, осуществляют в горизонтальных конвертерах, футерованных изнутри магнезитовым кирпичом 14. Опорно-приводные ролики 25 позволяют поворачивать конвертер для заливки штейна и выдачи черновой меди через горловину 17,. Продувку воздухам осуществляют через фурмы 16. Процесс превращения штейна в черновую медь разделяется на два периода. В первом периоде происходит окончательное окисление FeS и связывание FeO пустой породой (Si02). В ходе второго периода Cu2S окисляется кислородом воздуха и S02удаляется через горловину. Реакция первого периода идет с выделением тепла, разогревая ванну свыше 1300 °С. В ходе второго периода температура расплава снижается, так как реакцйи этого периода идут с поглощением тепла.
Черновая медь содержит примеси неметаллических включений и около 2 % примесей железа, цинка, никеля, свинца и др. Слитки черновой меди нуждаются в рафинировании, которое осуществляется огневым или электролитическим способом. При огневом рафинировании слитки расплавляют в пламенных печах и расплав окисляют продувкой воздухом через стальные трубы. Так как большинство примесей (Si, Мп, Zn, Fe, Si и др.) имеют более высокое сродство к кислороду, чем медь, они окисляются и переходят в шлак, который удаляют в конце периода окисления примесей. Продувка расплава меди природным газом во втором периоде способствует ее раскислению и удалению неметаллических включений. Окончательное раскисление меди осуществляют древесным углем и добавкой фосфористой меди.
| 12.2. |
Электролитическое рафинирование основано на анодном растворении чушек черновой меди в растворе медного купороса и серной кислоты 18. Катионы меди из раствора поступают на катод и там разряжаются. Процесс идет в течение нескольких дней. Примеси выпадают в осадок 19, а медь после переплава и разливки подается на прокатку.
Алюминий относится к наиболее распространенным в земной коре металлам. Он встречается в виде смеси оксидов алюминия, кремния и железа. В порядке уменьшения содержания
глинозема (А1203) и увеличения содержания силиката различают бокситы, нефелины, алуниты, каолины.
Технологический процесс производства алюминия разбивается на три этапа: извлечение глинозема из руд, его электролиз с целью получения алюминия и рафинирование. Предложено много различных методов извлечения глинозема из руд, но для самой богатой руды (боксита), содержащей до 50 % А1203 и 10 % Si02, чаще других применяют мокрый щелочной метод.
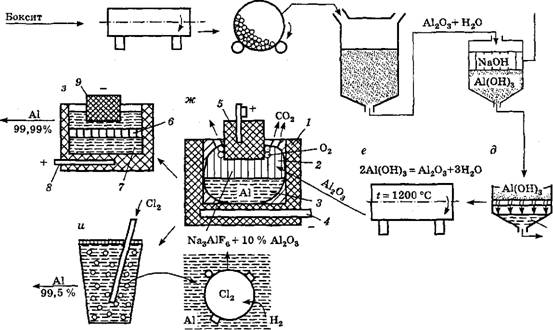
Общая схема технологического процесса производства алюминия приведена на рис. 12.2. Бокситы прокаливают в проходных трубчатых печах и измельчают в мельницах, после чего загружают в автоклав для выщелачивания при температуре около 200 °С и давлении до 3 МПа. При этом протекает реакция образования растворимого в воде алюмината натрия:
А1203 + ЗН20 + 2NaOH = Na20Al203+ 4Н20.
Параллельно идет процесс образования нерастворимого в воде NazO• А1203 ■ 2Si02• 2Н20. Чем выше содержание Si02в боксите, тем больше необратимые потери А1203 и NaOH. Пульпа после фильтрации сливается в отстойник и охлаждается, в результате чего гидрооксид алюминия выпадает в осадок:
Na20 • А1203 + 4Н20 = 2NaOH + 2А1(ОН)3!.
Воду отделяют от А1(ОН)3 фильтрованием, после чего гидрооксид обезвоживают нагреванием в печах и образующийся глинозем подают в электролизные ванны. Алюминий получают электролизом глинозема в расплавленном криолите Na3AlF6. Сварные стальные ванны футеруют изнутри угольными блоками 1, а у стенок — шамотным кирпичом. Стальные катодные шины 4 вмонтированы в футеровку, благодаря чему угольный слой футеровки является катодом. Анодами 5 служат самообжигающиеся угольные электроды, которые по мере обгорания снизу наращиваются сверху анодной массой, отвердевающей в результате коксования. Температура электролита 2 порядка 950 °С. Глинозем, расходуемый в ходе электролиза, загружается в ванну сверху, для чего твердая корка электролита периодически проламывается. При этом происходит удаление С02 в атмосферу.
Растворенный в электролите глинозем диссоциирует на ионы (А1203 = 2А13+ + ЗО2). На поверхности катода ионы алюминия
 |
| (=1000 °с |
| в г t= 200 °С NaOH + Н20 Р = 3 МПа |
| 50Al203+30Fe203 10Si02+10H20 |
| Н„0 |
| Рис. 12.2. Технологический процесс получения алюминия: а — прокалка руды; б — измельчение руды; в — выщелачивание; г — охлаждение раствора; д — осаждение гидрооксида; е — обезвоживание глинозема; ж — электролизная ванна; з — электрическое рафинирование; и — рафинирование хлором |
восстанавливаются до металла (2А13+ + бе = 2А1), который собирается на дне ванны 3, откуда периодически удаляется через металлическую летку. Кислородные ионы разряжаются на угольном аноде 5 и, взаимодействуя с ним, образуют С02.
Алюминий, полученный в электролизной ванне, загрязнен примесями кремния, железа, неметаллическими включениями и газами, в основном водородом, и нуждается в рафинировании. Для очистки от газов и неметаллических включений расплав алюминия продувают хлором. Пузырьки хлора и А1С13 (парообразного при температуре жидкого алюминия) растворяют водород и адсорбируют на своей поверхности включения, вынося их в верхние слои расплава и атмосферу. Более чистый алюминий можно получить повторным электролизом через расплав хлористых и фтористых солей 6, подобранных таким образом, чтобы их плотность была выше 2,7 г/см3. В рафинируемый алюминий для увеличения плотности добавляют медь 7. При этом анодом 8 является угольная ванна, а катодом 9 — угольный электрод. В расплавленном электролите алюминий подвергается анодному растворению и электролизу, скапливаясь в верхней части ванны. В ходе электролиза он очищается не только от неметаллических включений, растворяющихся в электролите, но и от металлических примесей.
mm Производство магния
Магний относится к числу широко распространенных металлов. Его содержание в земной коре превышает 2,3 %. Встречается он в виде следующих минералов:
□ магнезита — природного карбоната магния (MgC03), содержащего 28,8 % магния;
□ доломита — двойного карбоната магния и кальция (MgC03• СаС03), содержащего 13,2 % магния;
□ карналлита — двойного хлорида магния и калия (MgCl2• КС1 • 6Н20), содержащего 8,8 % магния;
□ бишофита — шеетиводного хлорида магния (MgCl2• 6Н20), растворенного в морской воде.
Независимо от вида исходного сырья процесс получения магния можно разбить на три периода: подготовку сырья, получение из него магния и рафинирование. Магний можно получать термическим и электролитическим способами. Последний способ применяется наиболее часто.
Общая схема технологического процесса производства магния из карналлита приведена на рис. 12.3. Карналлит обезвоживают и плавят в печах, после чего подают на электролиз, который протекает при температуре выше 700 °С, поддерживаемой пропусканием электрического тока (U = 6...7 В, I = 30 ООО...70 ООО А). Электролизер представляет собой сварную стальную ванну, футерованную внутри огнеупорным кирпичом 1. В расплав карналлита 3 опускают стальные катоды 4, облицованные с внутренней стороны огнеупором. Графитовый анод 5 устанавливается между двумя катодами и сверху закрывается хлороуловителем 6. Выделяющийся на аноде хлор в виде пузырьков 7 всплывает, собираясь в хлороуловителе, из которого он удаляется через отверстие 8.
Ионы магния разряжаются на катоде (Mg2++ 2е-Mg). Плотность электролита поддерживают выше плотности магния 2, вследствие чего последний всплывает на поверхность, откуда периодически удаляется с помощью вакуумных ковшей и насосов. При этом применяются определенные меры предосторожности, исключающие контакт расплавленного магния с кислородом воздуха (чтобы избежать возгорания).
Дальнейшую очистку магния можно осуществлять возгонкой, используя сравнительно низкую температуру его кипения, или за счет повторного плавления смеси магниевых чушек и специально подобранного флюса 9, растворяющего неметаллические включения чернового магния.
Если в качестве исходного сырья применяют магнезит или доломит, то процесс подготовки руды включает ее обжиг при 900 °С с целью разложения карбонатов, после чего полученный оксид магния смешивают с углем и нагревают в атмосфере хлора. Образующийся в ходе реакции хлорид магния используют для получения магния в электролизерах:
MgO + С + С12 = MgCl2+ СО.
Процесс получения бишофита из морской воды и его переработку с целью производства магния применяют редко, так как он связан со значительными затратами энергии и большой трудоемкостью.
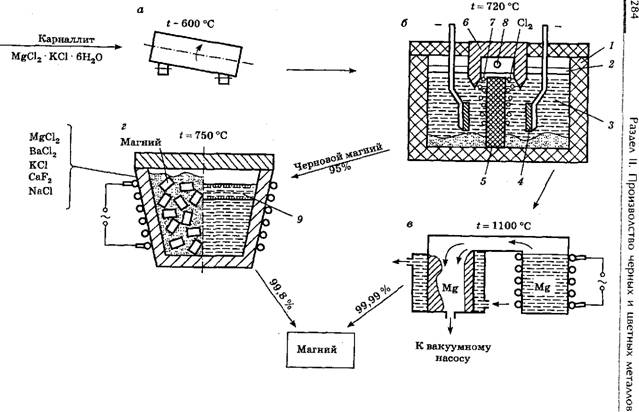 Рис. 12.3. Схема производства магния: а - обезвоживание карналлита; б - электролиз; в — рафинирование возгонкой; г - рафинирование переплавом Рис. 12.3. Схема производства магния: а - обезвоживание карналлита; б - электролиз; в — рафинирование возгонкой; г - рафинирование переплавом |
Производство титана
Титан относится к числу широко распространенных в природе металлов, его содержание в земной коре превышает 0,6 %. Но из-за трудности восстановления из оксидов он до сих пор не нашел такого широкого применения в технике, как, например, алюминий или железо. Известны две основные разновидности титановых руд: рутил ТЮ2 и ильменит FeO • Ti02.
Технологический процесс получения титана из ильменита представлен на рис. 12.4. В первом приближении он может быть разбит на следующие этапы: обогащение руды и получение двуокиси титана, получение четыреххлористого титана, восстановление титана и получение губки и, наконец, переплавка титановой губки в слитки.
Обогащение титана можно производить как магнитной сепарацией, так и флотацией. Смесь концентрата с углем загружают в отражательные или индукционные печи и нагревают до температуры плавления чугуна. В результате восстановления железа из оксида и его науглероживания углем на подине печи образуется расплав чугуна, а сверху — слой белого титанового шлака, содержащего 90 % ТЮ2. Порошок ТЮ2 смешивают с углем и после добавки каменноугольной смолы в качестве связующего брикетируют. Брикеты прокаливают при 800 °С и загружают в хлораторы, где они при такой же температуре подвергаются хлорированию. В его ходе идет реакция образования четыреххлористого титана:
ТЮ2+ 2С12+ С = TiCl4+ С02.
Четыреххлористый титан представляет собой бурую жидкость с температурой кипения 136 °С. Вместе с ним образуются хлористые соединения элементов, входящих в состав руды в виде примесей (Fe, V, Si). Для разделения хлоридов используется принцип ректификации, для чего пары смеси хлоридов пропускают через систему термостатов, в которых поддерживается температура более низкая, чем температура кипения соответствующего хлорида.
Восстановление титана из TiCl4осуществляется магнийтер- мическим или натрийтермическим методами. На рис. 12.4, г

| „ вакуумному насосу |
| Рис. 12.4. Технологический процесс получения титана: а — получение титанового шлака; б — брикетирование; в — получение TiCl4;г — получение титановой губки; д — рафинирование губки; е — брикетирование губки; ж — электродуговой переплав |
| Ильменит | Обогащение | Концентрат | >- |
| - 40 % ТЮ2 | - 60 % ТЮ2 | гх | |
| - 40 % FeO |
показана сущность наиболее часто используемого магнийтер- мического метода. В герметически закрываемых ретортах (реакторах) расплавляют чушки магния и при температуре свыше 900 °С к нему добавляют жидкий ТЮ14. В результате реакции
TiCI4+ 2Mg = Ti + 2MgCl2+ Q
образуется MgCl2, который периодически сливают из реактора, и хлопья титана, осаждающиеся в виде пористой массы (губки) на стенках реактора. Губку, содержащую до 60 % титана и в виде примесей MgCl2, и магний рафинируют при 900...950 °С отгонкой магния и MgCl2в водоохлаждаемые кристаллизаторы с помощью вакуума, после чего ее размалывают, брикетируют и переплавляют в слитки в вакуумных электрических дуговых печах с расходуемым электродом. Чтобы исключить загрязнение титана материалом тигля, плавку ведут в водоохлаждаемой медной изложнице. Электрическая дуга горит между расходуемым электродом из прессованной титановой губки и жидкой ванной металла. По мере оплавления электрод опускается вниз. Качество металла улучшается, если переплавка производится дважды.
Готовые слитки титана поступают на прокатку или на производство титановых сплавов.
ЛИТЕЙНОЕ ПРОИЗВОДСТВО
13. Изготовление отливок в разовых песчаных формах
14. Плавка сплавов
| Раздел |
 |
15. Специальные способы литья
 |
ИЗГОТОВЛЕНИЕ ОТЛИВОК В РАЗОВЫХ ПЕСЧАНЫХ ФОРМАХ
ш........... ::........... : i:,imi................ —г.-и,,,,, | мг.....,........ „„„...............,
Обшее понятие о литейной технологии
Сущность процесса получения отливок заключается в том, что расплавленный металл определенного состава заливается в литейную форму, внутренняя полость которой с максимальной степенью приближения воспроизводит конфигурацию и размеры будущей детали. В ходе дальнейшего охлаждения металл затвердевает, сохраняя приданную ему форму. Из всех известных способов формообразования (ковка, обработка резанием, сварка, порошковая металлургия и т.д.) литейная технология наиболе эффективна, так как позволяет получать изделия необходимой конфигурации непосредственно из расплава при сравнительно небольших затратах энергии, материалов и труда.
Эффективность литейной технологии объясняется ее универсальностью, позволяющей получать изделия из сплавов практически любого состава массой от нескольких граммов до сотен тонн. В настоящее время объем выпуска фасонных отливок в мире превышает 70 млн т. Литейная технология может быть реализована различными и весьма многообразными способами, но доминирующей пока остается технология получения отливок в разовой песчаной форме.
Процесс изготовления отливок в разовых песчаных формах
Основой для разработки технологического процесса изготовления отливки (литой заготовки) служит чертеж детали. Технолог-конструктор выбирает разъем модели и формы исходя из конструктивных особенностей детали, затем определяет припуски на механическую обработку, учитывая специфику существующего на заводе технологического процесса производства отливок,
после чего определяет литейные уклоны и рассчитывает литниковую систему. Таким образом получают чертеж отливки, который служит основой для разработки чертежей модели и стержневых ящиков, по которым изготавливается так называемый модельный комплект (рис. 13.1). Для изготовления формы и стержня кроме модельного комплекта нужна формовочная и стержневая смеси. Их изготавливают из соответствующих компонентов в смесителях.
б
'' —г
 |
| "43 Е--Э |
Q----------- -.-ai
Рис. 13.1. Модельный комплект: а — эскиз детали; б — модель; в — стержневой ящик; г — отливка
Общая схема последовательности операций по изготовлению отливки показана на рис. 13.2. На модельную плиту устанавливают модель и опоку, после чего слоями засыпают и уплотняют формовочную смесь. После завершения набивки опоку поворачивают, извлекают из нее модель и получают полуформу. Таким же образом изготавливают и вторую половинку формы. Стержневой ящик используют для получения стержня, образующего внутреннюю полость отливки. Как правило, после извлечения из стержневого ящика стержни подвергают сушке, а формы подаются на сборку сырыми. На следующем этапе форму собирают, для чего в нижнюю полуформу устанавливают стержень и закрывают верхней полуформой. Затем в зазор между стержнем и формой через литниковую систему заливают расплавленный металл, который плавят одновременно с изготовлением формы. Залитая форма выдерживается некоторое время, чтобы дать возможность металлу закристаллизоваться и охладиться до заданной температуры, после чего происходит выбивка отливки
 |
| ; гп—hд. |
| Рис. 13.2. Последовательность операций изготовления отливки: о — изготовление модельного комплекта; б — приготовление смесей; в — изготовление формы; г — изготовление стержня; д — сборка и заливка формы; е — выплавка сплава; ж — выбивка формы; з — удаление стержня; и — обрубка литников; к — очистка |
из формы. Затем из отливки выбивают стержень, обрубают литники и очищают отливки от пригоревшего к поверхности песка. Теперь рассмотрим каждый из этих этапов более подробно.
Формовочные и стержневые смеси и их приготовление
Для изготовления форм и стержней используют специально приготовленные из формовочных материалов смеси. Основными исходными материалами являются песок и глина, но кроме них используют связующие вещества и добавки. Кроме исходных материалов для приготовления формовочных смесей широко используют оборотные (бывшие в употреблении) смеси.
| 13.3. |
Качество отливок непосредственно связано со свойствами смесей. Существует большое количество различных критериев оценки качества смесей, но основными считают прочность,
газопроницаемость, противопригарность, пластичность и податливость.
Различают два способа оценки прочности смесей: на сжатие — для сырых форм и на растяжение — для сухих форм и стержней. В обоих случаях по оговоренной стандартом технологии приготавливают образцы и испытывают их на лабораторных установках. Предел прочности на сжатие составляет 1...10 Па для сырых смесей и после сушки повышается на порядок, что связано с упрочнением пленки связующих веществ, обволакивающих песчинки. Прочность смесей зависит от содержания влаги, количества и типа связующего вещества, степени уплотнения и, в меньшей степени, от зерновой структуры песка, качества перемешивания и т.д. При низкой прочности смесей формы и стержни не выдерживают динамического удара струи заливаемого в форму металла или статического давления столба расплавленного металла, в результате чего происходит их разрушение, что в итоге приводит к появлению брака в отливках.
Газопроницаемость характеризует способность смеси пропускать через толщу формы или стержня образующиеся в них газы. При низкой газопроницаемости газы, образующиеся при испарении влаги или в результате выгорания связующих материалов, поступают в заливаемый металл, вызывают его вскипание и образование в отливках газовых раковин. Газопроницаемость зависит от влажности смеси, размеров и однородности зерен песка, степени уплотнения и содержания глины. Она определяется путем измерения времени прохождения стандартного объема воздуха через образец, условия изготовления которого регламентированы стандартом.
Противопригарность — это способность смеси не оплавляться, не спекаться под воздействием расплавленного металла и не образовывать с его оксидами химические соединения, которые способствуют образованию на поверхности отливок (пригара) — трудноудаляемого металлокерамического слоя. Для борьбы с пригаром стараются создать в полости формы восстановительную атмосферу, добавляя в состав смесей мазут или каменноугольную пыль. Чтобы исключить механическое проникновение расплава в поры смеси, поверхность стержней окрашивают, а рабочую полость припыливают огнеупорными припылами.
Пластичность необходима смеси для обеспечения четкого отпечатка модели в форме. При высокой пластичности смесь в процессе уплотнения перемещается не только в направлении приложения силы, но и перпендикулярно ему, что обеспечивает заполнение углов формы. На пластичность влияет количество влаги и глины, а также зерновая структура песка.
Податливость — способность смеси сокращаться в объеме под действием сжимающих усилий отливки при ее усадке в процессе охлаждения. Низкая податливость приводит к возникновению напряжений в отливке и даже появлению в ней трещин. Податливость связана с потерей смесью прочности при прогреве от отливки, а также с ее пористостью, зерновой структурой и наличием специально вводимых добавок (древесных опилок).
Основа любой смеси — пески, глины и связующие добавки. Формовочные пески делят на классы в зависимости от содержания в них глинистой составляющей и примесей, а также на группы — в зависимости от размера основной фракции. Основной составляющей песка является кремнезем Si02, но в виде примесей он может содержать каолин, слюду, полевой шпат, оксиды железа, магнезит и т.д. Для приготовления огнеупорных облицовочных смесей и стержневых красок используют шамот, оли- винит, цирконовый концентрат и другие материалы.
Формовочные глины служат минеральным связующим в формовочных смесях. Их классифицируют по минералогическому составу, прочности, огнеупорности и пластичности. По минералогическому составу глины подразделяют на каолиновые (A1Z03■ 2Si02• 2Н20), бентонитовые (А1203 ■ 4Si02■ Н20 • 2Н20) и полиминеральные. Бентонитовые глины обладают более высокой способностью к набуханию и более высокой прочностью по сравнению с другими. Как связующий материал глина обладает рядом недостатков. Высокая прочность смеси может быть получена только в том случае, когда она содержит большое количество глины, а это снижает газопроницаемость,и способствует образованию пригара на поверхности отливок. В связи с этим содержание глины в смесях ограничивается, а для обеспечения требуемых свойств в них вводят специальные связующие добавки.
Эти добавки делят на три класса. К классу А относят органические связующие, нерастворимые и несмачиваемые водой, к классу Б — органические связующие, растворимые или смачиваемые водой, и к классу В — неорганические связующие, растворимые водой в незатвердевшем состоянии (жидкое стекло). Основной характеристикой связующих является их удельная прочность при растяжении сухого образца, т.е. прочность в расчете на 1 % связующего. Широкое распространение в качестве связующих находят синтетические смолы, смолосодержащие продукты (пеки) и их смеси с органическими водными материалами, а также коллоидные растворы органических веществ (сульфидная патока, декстрин).
Особенно перспективно введение в состав смесей синтетических смол, способных к отвердеванию в холодной или нагреваемой оснастке. Для холоднотвердеющих смесей широко применяются смолы на карбомидофурановой (БС-40), карбомидоформальде- гидной (КФ-Ж), фенолформальдегидной (ОФ-1) и фенолфурано- вой (ФФ-1Ф) основе, которые растворяются в фуриловом спирте и отвердевают в стержневых ящиках при добавке 0,7... 1,0 % ортофосфорной кислоты. Содержание смолы в смеси обычно не превышает 2 %.
 2018-01-08
2018-01-08 1049
1049








