Первый закон термодинамики — это закон сохранения и превращения энергии в применении к тепловым процессам.
Если механическая энергия системы не изменяется, а система не замкнута и между ней и окружающей средой происходит теплообмен, то изменяется внутренняя энергия.
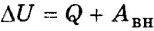
Первый закон термодинамики формулируется так:
изменение внутренней энергии при переходе системы из одного состояния в другое равно работе внешних сил плюс количество теплоты, переданное системе в процессе теплообмена.
Если вместо работы внешних сил А внввести работу А системы над внешними телами А = -Авн, то запишется: 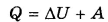
Тогда I закон термодинамики можно сформулировать так: количество теплоты, сообщенное системе, идет на изменение ее внутренней энергии и на совершение системой работы против внешних сил.
Из первого закона термодинамики вытекает невозможность создания вечного двигателя первого рода, т.е. такого двигателя, который совершал бы работу без затраты энергии извне.
Действительно, если к системе не подводится энергия Q = 0, то А =-ΔU и работа может быть совершена за счет убыли внутренней энергии системы. После того, как запас энергии окажется исчерпанным, двигатель перестанет работать.
Если система замкнута (Авн=0) и адиабатически изолирована (Q = 0) то первый закон термодинамики будет иметь вид:ΔU=0
Если в такой системе имеются тела с различной температурой, то между ними будет происходить теплообмен: тела, у которых температура выше, будут отдавать энергию и охлаждаться, а тела с меньшей температурой будут получать энергию и нагреваться. Это будет происходить до тех пор, пока температуры у всех тел не станут одинаковыми. При этом ΔU1+ΔU2+…ΔUn=0 или Q1+Q2+…+Qn=0
Первый закон термодинамики для незамкнутой и адиабатически изолированной системы называют уравнением теплового баланса.
 2018-01-08
2018-01-08 446
446








