Внутренняя энергия реального газа
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул (определяет внутреннюю энергию идеального газа, равную CVT; см. § 53) и потенциальной энергии межмолекулярного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к возникновению внутреннего давления на газ (см. (61.1)):
p'=a/V2m
dРабота, которая затрачивается для преодоления сил притяжения, действующих между молекулами газа, как известно из механики, идет на увеличение потенциальной энергии системы, т. е. A=p'dVm=dП=(a/VdП, или 2m)dVm, откуда
П=-a/Vm
(постоянная интегрирования принята равной нулю). Знак минус означает, что молекулярные силы, создающие внутреннее давление р', являются силами притяжения (см. § 60).
Учитывая оба слагаемых, получим, что внутренняя энергия моля реального газа
Um = CVT-a/Vm (63.1)
растет с повышением температуры и увеличением объема.
|
|
|
dЕсли газ расширяется без теплообмена с окружающей средой (адиабатический процесс, т. е. Q Q=(UdA=0), то на основании первого начала термодинамики (d= 0) и не совершает внешней работы (расширение газа в вакуум, т. е. 2-U1)+dA) получим, что
U1=U2. (63.2)
Следовательно, при адиабатическом расширении без совершения внешней работы внутренняя энергия газа не изменяется.
Равенство (63.2) формально справедливо как для идеального, так и для реального газов, но физически для обоих случаев совершенно различно. Для идеального газа равенство U1=U2 означает равенство температур (Т1=Т2), т. е. при адиабатическом расширении идеального газа в вакуум его температура не изменяется. Для реального газа из равенства (63.2), учитывая, что для моля газа
U1=CVT1-a/V1, U2=CVT2-a/V2,
(63.3) получаем
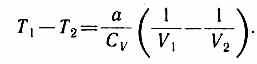
Так как V2>V1, то Т1>Т2, т. е. реальный газ при адиабатическом расширении в вакуум охлаждается. При адиабатическом сжатии реальный газ нагревается.
§ 64. Эффект Джоуля — Томсона
Если идеальный газ адиабатически расширяется и совершает при этом работу, то он охлаждается, так как работа в данном случае совершается за счет его внутренней энергии (см. § 55). Подобный процесс, но с реальным газом — адиабатическое расширение реального газа с совершением внешними силами положительной работы — осуществили английские физики Дж. Джоуль (1818—1889) и У. Томсон (лорд Кельвин, 1824—1907).
Рассмотрим эффект Джоуля — Томсона. На рис. 93 представлена схема их опыта. В теплоизолированной трубке с пористой перегородкой находится два поршня, которые могут перемещаться без трения. Пусть сначала слева от перегородки газ под поршнем 1 находится под давлением р1, занимает объем V1 при температуре Т1, а справа газ отсутствует (по-
|
|
|
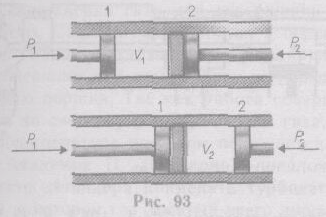
ршень 2 придвинут к перегородке). После прохождения газа через пористую перегородку в правой части газ характеризуется параметрами р2, V2, Т2. Давления р1 и р2 поддерживаются постоянными (р1>р2).
Так как расширение газа происходит без теплообмена с окружающей средой (адиабатически), то на основании первого начала термодинамики
dQ=(U2-U1d)+A=0. (64.1)
Внешняя работа, совершаемая газом, состоит из положительной работы при движении поршня 2 (A2=p2V2) и отрицательной при движении поршня 1 (A1=p1V1), dт.е. A=A2-А1. Подставляя выражения для работ в формулу (64.1), получим
U1+p1V1=U2+p2V2. (64.2)
Таким образом, в опыте Джоуля — Томсона сохраняется (остается неизменной) величина U+pV. Она является функцией состояния и называется энтальпией.
Ради простоты рассмотрим 1 моль газа. Подставив в формулу (64.2) выражение (63.3) и рассчитанные из уравнения Ван-дер-Ваальса (61.2) значения p1V1 и p2V2 (символ «m» опять опускаем) и производя элементарные преобразования, получим
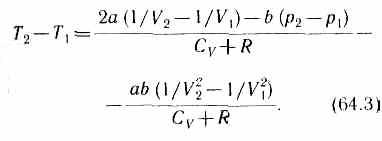
Из выражения (64.3) следует, что знак разности (T2-T1) зависит от того, какая из поправок Ван-дер-Ваальса играет большую роль. Проанализируем данное выражение, сделав допущение, что p2<<p1
и V2>>V1:
0— не учитываем силы притяжения между молекулами, а учитываем лишь размеры самих молекул. Тогда»1) a
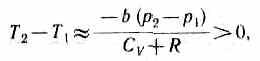
т. е. газ в данном случае нагревается;
0 - не учитываем размеров молекул, а учитываем лишь силы притяжения между молекулами. Тогда»2) b
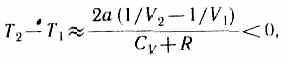
т. е. газ в данном случае охлаждается;
3) учитываем обе поправки. Подставив в выражение (64.3) вычисленное из уравнения Ван-дер-Ваальса (61.2) значение p1, имеем
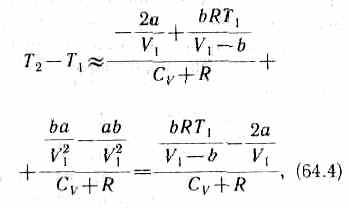
т. е. знак разности температур зависит от значений начального объема V1 и начальной температуры Т1.
Изменение температуры реального газа в результате его адиабатического расширения, или, как говорят, адиабатического дросселирования — медленного прохождения газа под действием перепада давления сквозь дроссель (например, пористую перегородку), называется эффектом Джоуля — Томсона. Эффект Джоуля — Томсона принято называть положительным, TDесли газ в процессе дросселирования охлаждается (<0), и отрицательным, TDесли газ нагревается (>0).
В зависимости от условий дросселирования для одного и того же газа эффект Джоуля — Томсона может быть как положительным, так и отрицательным. Температура, при которой (для данного давления) происходит изменение знака эффекта Джоуля — Томсона, называется температурой инверсии.
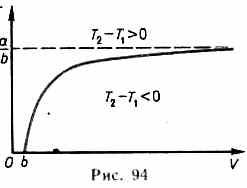
Ее зависимость от объема получим, приравняв выражение (64.4) нулю:
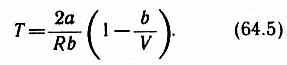
Кривая, определяемая уравнением (64.5),— кривая инверсии — приведена на рис. 94. Область выше этой кривой соответствует отрицательному эффекту Джоуля — Томсона, ниже — положительному. Отметим, что при больших перепадах давления на дросселе температура газа изменяется значительно. Так, при дросселировании от 20 до 0,1 МПа и начальной температуре 17 °С воздух охлаждается на 35 °С.
Эффект Джоуля — Томсона обусловлен отклонением газа от идеальности. В самом деле, для моля идеального газа pVm = RT, поэтому выражение (64.2) примет вид
CVT1+RT1=CVT2 + RT2, откуда следует, что T1=T2
 2018-01-08
2018-01-08 4349
4349








