Твердые тела. Моно- и поликристаллы
Твердые тела (кристаллы) характеризуются наличием значительных сил межмолекулярного взаимодействия и сохраняют постоянными не только свой объем, но и форму. Кристаллы имеют правильную геометрическую форму, которая, как показали рентгенографические исследования немецкого физика-теоретика М. Лауэ (1879-1960), является результатом упорядоченного расположения частиц (атомов, молекул, ионов), составляющих кристалл. Структура, для которой характерно регулярное расположение частиц с периодической повторяемостью в трех измерениях, называется кристаллической решеткой. Точки, в которых расположены частицы, а точнее — точки, относительно которых частицы совершают колебания, называются узлами кристаллической решетки.
Кристаллические тела можно разделить на две группы: монокристаллы и поликристаллы. Монокристаллы — твердые тела, частицы которых образуют единую кристаллическую решетку. Кристаллическая структура монокристаллов обнаруживается по их внешней форме. Хотя внешняя форма монокристаллов одного вида может быть различной, но углы между соответствующими гранями у них остаются постоянными. Это закон постоянства углов, сформулированный М. В. Ломоносовым. Он сделал важный вывод, что правильная форма кристаллов связана с закономерным размещением частиц, образующих кристалл. Монокристаллами являются большинство минералов. Однако крупные природные монокристаллы встречаются довольно редко (например, лед, поваренная соль, исландский шпат). В настоящее время многие монокристаллы выращиваются искусственно. Условия роста крупных монокристаллов (чистый раствор, медленное охлаждение и т. д.) часто не выдерживаются, поэтому большинство твердых тел имеет мелкокристаллическую структуру, т. е. состоит из множества беспорядочно ориентированных мелких кристаллических зерен. Такие твердые тела называются поликристаллами (многие горные породы, металлы и сплавы).
|
|
|
Характерной особенностью монокристаллов является их анизотропность, т. е. зависимость физических свойств — упругих, механических, тепловых, электрических, магнитных, оптических — от направления. Анизотропия монокристаллов объясняется тем, что в кристаллической решетке различно число частиц, приходящихся на одинаковые по длине, но разные по направлению отрезки (рис. 102), т. е. плотность расположения частиц кристаллической решетки по разным направлениям не одинакова, что и приводит к различию свойств кристалла вдоль этих направлений. В поликристаллах анизотропия наблюдается только для отдельных мелких кристалликов, но их различная
|
|
|

ориентация приводит к тому, что свойства поликристалла по всем направлениям в среднем одинаковы.
§71. Типы кристаллических твердых тел
Существует два признака для классификации кристаллов: 1) кристаллографический; 2) физический (природа частиц, расположенных в узлах кристаллической решетки, и характер сил взаимодействия между ними).
1. Кристаллографический признак кристаллов. В данном случае важна только пространственная периодичность в расположении частиц, поэтому можно отвлечься от их внутренней структуры, рассматривая частицы как геометрические точки.
Кристаллическая решетка может обладать различными видами симметрии. Симметрия кристаллической решетки — ее свойство совмещаться с собой при некоторых пространственных перемещениях, например параллельных переносах, поворотах, отражениях или их комбинациях и т. д. Кристаллической решетке, как доказал русский кристаллограф Е. С. Федоров (1853—1919), присущи 230 комбинаций элементов симметрии, или 230 различныхпространственных групп.
С переносной симметрией в трехмерном пространстве связывают понятие трехмерной периодической структуры — пространственной решетки, или решетки Бравэ, представление о которой введено французским кристаллографом О. Бравэ (1811 —1863). Всякая пространственная решетка может быть составлена повторением в трех различных направлениях одного и того же структурного элемента — элементарной ячейки. Всего существует 14 типов решеток Бравэ, различающихся по виду переносной симметрии. Они распределяются по семи кристаллографическим системам, или сингониям, представленным в порядке возрастающей симметрии в табл. 3. Для описания элементарных ячеек пользуются кристаллографическими осями координат, которые проводят параллельно ребрам элементарной ячейки,
а начало координат выбирают в левом углу передней грани элементарной ячейки. Элементарная кристаллическая ячейка представляет собой параллелепипед, построенный на ребрах а, b, с называютсяg и b, a между ребрами (табл. 3). Величины а, b и с и g и b, aс углами параметрами элементарной ячейки и однозначно ее определяют. 
Анизотропия кристаллов
Анизотропия– это зависимость свойств материала от направления. Материал считаетсяизотропным, когда его свойства во всех направлениях одинаковые. Если же с изменением направления свойства материала изменяются, материал считаетсяанизотропным.
Анизотропия характерна для кристаллов и обусловлена их упорядоченной структурой. В кристаллах в различных направлениях атомы располагаются с различной плотностью, т.е. на различном расстоянии друг от друга, что отражается на силе взаимодействия атомов. Как следствие, свойства кристаллов в различных направлениях оказываются различными. Например, в кубическом кристалле в направлении координатных осей атомы вещества располагаются на расстоянии друг от друга равном а (рис.1). В направлении диагонали атомы располагаются на расстоянии а 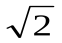 , а в направлении пространственной диагонали – а
, а в направлении пространственной диагонали – а  . Очевидно, такой кристалл легче разорвать в направлении пространственной диагонали, чем в направлении координатных осей, где он обнаруживает наибольшую прочность из-за того, что атомы расположены ближе и сильнее взаимодействуют.
. Очевидно, такой кристалл легче разорвать в направлении пространственной диагонали, чем в направлении координатных осей, где он обнаруживает наибольшую прочность из-за того, что атомы расположены ближе и сильнее взаимодействуют.
Анизотропия распространяется практически на все свойства кристаллов. Так, кристалл в одном направлении лучше, чем в другом может проводить тепло, электрический ток, свет, лучше намагничиваться и т.д. При этом, чем ниже система симметрии кристалла, тем сильнее проявляется анизотропия его свойств.
В аморфных материалах, из-за хаотического внутреннего строения, атомы в различных направлениях располагаются примерно с одинаковой плотностью. В результате свойства данных материалов в различных направлениях оказываются одинаковыми, т.е. вещество оказывается изотропным.
|
|
|
Металлы и сплавы, полученные в обычных условиях, также очень часто обнаруживают равенство свойств в различных направлениях, хотя и являются материалами кристаллическими, а не аморфными. Это объясняется их зернистым строением. Зёрна данных материалов, будучи кристаллами, в различных направлениях обнаруживают различные свойства, однако в целом материал оказывается изотропным, поскольку зёрна случайным образом ориентированы в пространстве и при сложении свойств в каждом направлении получается примерно одна, усреднённая величина. Такую изотропию называют ложной изотропией или квазиизотропией.
Иногда зёрна поликристаллических материалов оказываются ориентированными преимущественно в одном направлении. Например, зёрна металлов и сплавов при пластическом деформировании вытягиваются в направлении деформации. Такое явление называют текстурой. При появлении текстуры свойства кристаллических материалов вновь начинают зависеть от направления, т.е. материал оказывается анизотропным.
1.7 Дефекты кристаллической структуры
Структура реальных кристаллов не является идеально симметричной. В реальных кристаллах всегда имеются те или иные отклонения от периодичности расположения атомов. Эти нарушения порядка называют дефектами кристаллической структуры.
Дефекты кристаллической структуры, в зависимости от размеров, подразделяют на точечные, линейные, поверхностные и объёмные.
Точечные дефекты кристаллической структуры во всех трёх измерениях имеют размеры сравнимые с межатомным расстоянием, т.е. порядка одного нанометра. К точечным дефектам структуры относятся вакансии, межузельные атомы и атомы примесей.
Вакансией называют незанятое атомом свободное место в узле кристаллической решётки.Межузельным называют атом, смещённый из узла кристаллической решётки в положение между узлами (рис.3). Данные дефекты возникают, как правило, парами, поскольку смещение атома в межузельное положение сопровождается появлением вакансии.
|
|
|
Примесные атомы – это инородные атомы, которые размещаются либо в узлах кристаллической решётки (примесные атомы замещения), либо в межузельном пространстве (примесные атомы внедрения).
 В – вакансия;
В – вакансия;
МА – межузельный
атом;
ПАЗ – примесный атом
замещения;
ПАВ – примесный атом
внедрения.



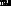 Рис. 3. Точечные дефекты кристаллической структуры.
Рис. 3. Точечные дефекты кристаллической структуры.
Вакансии и межузельные атомы непрерывно появляются в кристаллах за счёт энергии тепловых колебаний атомов. Они относительно свободно перемещаются по кристаллу и могут встречаться друг с другом. При встрече межузельного атома с вакансией возможна рекомбинация, т.е. замещение вакантного места межузельным атомом. Дефекты также могут исчезать на любых свободных поверхностях кристалла: на порах, границах зёрен, микротрещинах, которые называют стоками дефектов. Процессы непрерывной рекомбинации, а также исчезновения дефектов на стоках, уравновешиваются процессами их генерации так, что в кристалле всегда поддерживается некоторая равновесная концентрация точечных дефектов. Чем выше температура кристалла, тем выше эта равновесная концентрация дефектов.
Вакансии и межузельные атомы обычно не оказывают заметного влияния на механические свойства материалов, поскольку искажения, вносимые ими в структуру, имеют очень маленький размер. Однако, при возрастании концентрации данных дефектов до значений, значительно превышающих равновесное, это влияние становиться более заметным. Например, при бомбардировке материалов потоком высокоэнергетичных частиц в их поверхностном слое образуется большое число точечных радиационных дефектов, что приводит к существенному изменению поверхностных свойств материала. Имеются сведения о повышении твёрдости и износостойкости облучённой поверхности. Изменяются и другие характеристики облучённых материалов.
Поскольку все точечные дефекты, и особенно примесные атомы, препятствуют прохождению электрического тока через металлические материалы, возрастание их концентрации в металлах приводит к повышению электросопротивления.
Линейные дефекты кристаллической структурыв двух измерениях имеют размеры, сравнимые с межатомным расстоянием, а в третьем измерении простираются на многие сотни и тысячи периодов кристаллической решётки. К линейным дефектам структуры относяткраевые и винтовые дислокации.
Краевую дислокациюобразует край АА' «лишней» атомной полуплоскости, называемой экстраплоскостью (рис. 4).
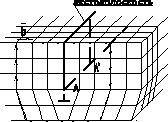 Рис.4. Краевая дислокация.
Рис.4. Краевая дислокация.
Если экстраплоскость располагается в верхней части кристалла, то соответствующую дислокацию обозначают значком «^», а если в нижней, то знаком «┬». Вдоль линии дислокации кристаллическая структура материала искажена, однако на расстоянии всего в несколько периодов кристаллической решётки от данной линии искажений структуры уже не наблюдается. Линия краевой дислокации обычно бывает изогнутой, а не прямой. Форма этой линии под воздействием внешних и внутренних факторов может изменяться, так же как и её местоположение в кристалле.
В  интовую дислокациюможно определить как сдвиг одной части кристалла относительно другой его части, происходящий по некоторой плоскости скольжения – ПС (рис.5). ЛиниюL, лежащую в этой плоскости и отделяющую ту её часть, где сдвиг уже произошел от той её части, где сдвиг ещё не происходил, называютлинией винтовой дислокации. Кристалл как бы закручивается в спираль вокруг этой линии. Если закручивание происходит по часовой стрелке, то соответствующую дислокацию называют правой, если против часовой стрелки – то левой.
интовую дислокациюможно определить как сдвиг одной части кристалла относительно другой его части, происходящий по некоторой плоскости скольжения – ПС (рис.5). ЛиниюL, лежащую в этой плоскости и отделяющую ту её часть, где сдвиг уже произошел от той её части, где сдвиг ещё не происходил, называютлинией винтовой дислокации. Кристалл как бы закручивается в спираль вокруг этой линии. Если закручивание происходит по часовой стрелке, то соответствующую дислокацию называют правой, если против часовой стрелки – то левой.
Рис. 5. Винтовая дислокация.
Линия любой отдельной дислокации не может обрываться внутри кристалла. Она либо выходит на поверхность кристалла, в частности на границы зёрен, либо замыкается сама на себя, образуя дислокационную петлю. Под плотностью дислокацийпонимают суммарную протяжённость всех дислокаций, находящихся в единице объёма материала:
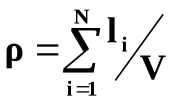 , (1)
, (1)
где li – длина отдельной дислокации;N– общее число дислокаций в материале;V– объём материала. Единицей измерения ρ является см/см3или см-2.
Равновесная плотность дислокаций в полупроводниковых кристаллах находится в пределах 104 10¸5см–2, а в металлах – 106 10¸8см–2.
В определённых условиях дислокации, также как и точечные дефекты, способны перемещаться по кристаллу. При этом дислокации одного знака отталкиваются друг от друга, а противоположенных знаков – притягиваются. При встрече двух дислокаций противоположенных знаков может произойти их аннигиляция, т.е. взаимоуничтожение. Под воздействием внешних нагрузок, вызывающих пластическую деформацию материала, происходит перемещение дислокаций в сторону свободных поверхностей кристалла. Вместо вышедших на поверхность, а также аннигилировавших дислокаций, в деформируемом материале нарождаются новые дислокации.
Дислокации, благодаря их значительной протяжённости, оказывают существенное влияние на механические свойства материалов. Они играют важную роль в механизме пластического деформирования материалов. При пластической деформации материалов наблюдается сдвиг атомных слоёв относительно друг друга и дислокации способствуют этому процессу. Благодаря дислокациям атомные слои могут смещаться относительно друг друга не сразу целиком, а поэтапно, т.е. атомными рядами. Такой поэтапный сдвиг атомных слоёв выглядит как движение дислокаций в противоположенном направлении и требует при деформировании значительно меньших усилий.
Учитывая вышесказанное можно утверждать, что металлы и сплавы своей высокой пластичностью обязаны наличию в них достаточно большого количества подвижных дислокаций. Под воздействием холодной пластической деформации плотность дислокаций в металлах возрастает до 101110¸12см–2. При такой высокой плотности дислокации начинают интенсивно взаимодействовать и мешать друг другу, что приводит к ограничению их подвижности. В результате металл становится менее пластичным и более прочным. Такое явление называютнаклёпом.
Поверхностные дефектыкристаллическойструктурыв одном из измерений имеют размеры, сравнимые с межатомным расстоянием, а в двух других измерениях простираются на многие сотни и тысячи межатомных расстояний. К поверхностным дефектам структуры относят границы зёрен, фрагментов и блоков. Указанные границы являются местом скопления всевозможных точечных и линейных дефектов. Они выглядят как дислокационные стенки, разделяющие кристаллический материал на участки (рис.6).
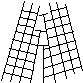 Рис.6. Дислокационная стенка.
Рис.6. Дислокационная стенка.
Порядок расположения атомов в зоне границ сильно нарушен. Это наиболее дефектная область материала. По границам зёрен обычно распространяются трещины, разрушающие металлический материал, а также более активно идут процессы взаимодействия металла с химически активными веществами, в частности, процессы окисления, а также травления кислотами.
Поверхностные дефекты оказывают существенное влияние на свойства материалов. Они, в частности, способствуют процессам диффузии, но препятствуют процессу прохождения электрического тока через материал. Для механических свойств особое значение имеет общая протяженность межзёренных границ в единице объёма, т.е. плотность границ. С уменьшением размера зёрен, а, следовательно, увеличением плотности их границ, увеличиваются вязкость, пластичность и прочность металлических материалов.
Объёмные дефекты структуры имеют значительные размеры во всех трех измерениях. К объёмным дефектам структуры относят всевозможные поры, инородные включения, выбоины и царапины на поверхности, микротрещины и т.п. При разрушении материалов объёмные дефекты обычно играют роль концентраторов напряжений и источников трещин, а поэтому являются причиной снижения прочностных характеристик материала.
58. Теплоемкость твердых тел. Закон Дюлонга и Пти.
Теплоемкость кристаллов. Закон Дюлонга-Пти. Теория теплоемкости Эйнштейна и Дебая
Расположение частиц в узлах отвечает минимуму их взаимной потенциальной энергии. При смещении частиц из узла решетки возникает возвращающая сила, вследствие которой возникнут колебания частиц, которые можно представить как наложение колебаний вдоль трех координатных осей, т.е. приписать колебанию частицы три колебательные степени свободы. На каждую колебательную степень свободы приходится энергия, равная kT (1/2 kT – в виде кинетической и 1/2 kT – в виде потенциальной энергии). Следовательно, на каждую частицу в узле решетки приходится энергия, равная 3 kT, а энергия одного моля вещества будет равна внутренней энергии U
U = 3NAkT = 3 RT
и молярная теплоемкость твердого тела (для них Сv = Сp)
C = 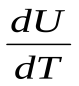 = 3R.
= 3R.
Это соотношение носит название закона Дюлонга-Пти. Этот закон выполняется только при температурах близких кнормальной и не выполняется при низких температурах.
Для выяснения зависимости теплоемкости кристаллов Эйнштейн предложил теорию, в которой систему из N атомов представил в виде 3N независимых гармонических осцилляторов, колеблющихся с одинаковой частотой ν. Энергия каждого гармонического осциллятора может иметь значения
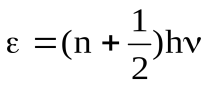 n = 0, 1, 2, 3, …
n = 0, 1, 2, 3, …
Тогда для системы 3N осцилляторов энергия будет равна
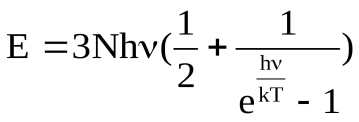 ,
,
а теплоемкость твердого тела равна
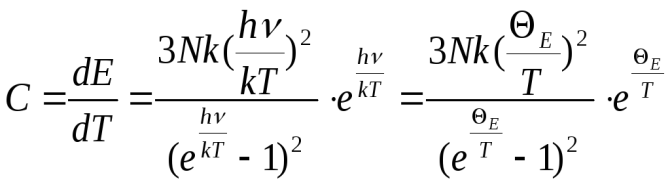 ,
,
где 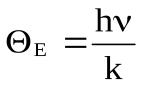 - характеристическая температура Эйнштейна из условия, что hν = ΘEk. Это формула теплоёмкости кристаллов по теории Эйнштейна.
- характеристическая температура Эйнштейна из условия, что hν = ΘEk. Это формула теплоёмкости кристаллов по теории Эйнштейна.
При высоких температурах когда kT» hν теплоемкость 1моля будет равна
С = 3NAk = 3R.
т.е. отражает закономерность Дюлонга-Пти.
При низких температурах (kT«hν) эта формула качественно правильно описывает ход снижения теплоемкости твердого тела, но все же расходится с опытными данными для температур близких к абсолютному нулю
Пренебрегая единицей в знаменателе, получим выражение для теплоёмкости
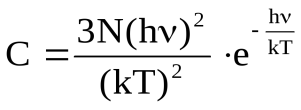 .
.
При Т→0 экспоненциальный множитель изменяется значительно быстрее, чем Т2. Поэтому при приближении к абсолютному нулю теплоёмкость будет стремиться к нулю по экспоненциальному закону. Опыт показывает, что теплоёмкость кристаллов вблизи абсолютного нуля изменяется не экспоненциально по закону Т3.
Дебай посчитал, что предположение Эйнштейна о равенстве частот всех гармонических осцилляторов является чрезмерно упрощенным. Он предположил, что гармонические осцилляторы обладают спектром (набором) частот, общее число которых ограничено и равно 3N. В соответствии с этим Дебай получил формулы для молярных (См) теплоёмкостей кристаллов
 - при высоких температурах и
- при высоких температурах и
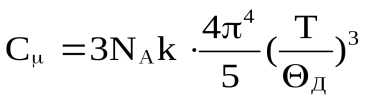 - при низких температурах.
- при низких температурах.
где 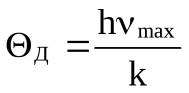 - характеристическая температура Дебая.
- характеристическая температура Дебая.
Это соотношение носит название закона кубов Дебая.
Понятие о зонной теории твердых тел
Взаимодействие электронов и ядер в свободном атоме является весьма сложным. Еще более сложно описать их взаимодействие в кристалле, где каждая частица взаимодействует с огромным числом соседних частиц. Известно, что в изолированном атоме электроны находятся в дискретных энергетических состояниях. Из соотношения неопределенностей для энергии и времени
ΔЕ·Δt 
ширина энергетического уровня для электрона в свободном возбужденном атоме (Δt∼10-8 с) составляет величину порядка 10-7 эВ, а в основном состоянии (Δt→∞) –ΔЕ ≃0. Для электронов в кристалле ширина энергетического уровня  от 1 до 10 эВ. Почему возрастает неопределенность в определении энергии электронов атома в кристалле?
от 1 до 10 эВ. Почему возрастает неопределенность в определении энергии электронов атома в кристалле?
В свободном атоме энергетические состояния определяются взаимодействием их с ядром своего атома. При сближении двух атомов на расстояние менее 10-10м А электронные оболочки валентных (внешних) электронов настолько перекроются, что энергетические уровни уже не будут соответствовать энергетическим уровням электронов свободного атома. В отличие от изолированных атомов, где энергетические уровни электрона представляют резкие линии (определенные значения), при образовании кристалла происходит расщепление уровней и энергетический спектр электронных состояний представляет собой совокупность энергетических уровней, называемых зоной.
Расщепление уровней присуще всем электронам атома, но величина расщепления для разных уровней разная.
Для внутренних оболочек величина расщепления очень мала и внутренние электроны в кристалле ведут себя практически также как и в изолированных атомах.
В результате расщепления энергетических уровней область возможных значений энергии электронов кристалла разделяется на ряд зон (рис. 181) – разрешенных и запрещенных значений энергии. С уменьшением энергии ширина разрешенных зон убывает, а запрещенных – возрастает.
Энергетическая зона не является непрерывным рядом значений энергий электрона, а представляет собой ряд конкретных дискретных уровней, отстоящих друг от друга на величину порядка 10-22 эВ. Разрешенные энергетические зоны в кристалле могут быть по разному заполнены электронами – в предельных случаях либо полностью свободны, или целиком заполнены.
Возможны переходы электронов из одной разрешенной зоны в другую. Для этого необходимо затратить энергию, численно равную ширине запрещенной зоны. Для внутризонных переходов с уровня на уровень требуется очень небольшая энергия (10-4 – 10-8 эВ). Существование энергетических зон позволяет объяснить разделение твердых веществ по электропроводности на металлы, полупроводники и диэлектрики (рис. 182). Электропроводность металла объясняется тем, что электроны валентной зоны (у металлов она является и зоной проводимости) под действием незначительной сообщенной им энергии могут совершать внутризонные переходы, а поскольку они слабо связаны с узлами кристаллической решетки, то под действием слабого электрического поля могут ускоряться и приобретать дополнительную скорость в направлении противоположном полю, т.е. обеспечивать электрический ток.

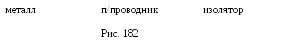
У полупроводников валентная зона полностью заполнена и для вовлечение электронов в электрический ток им необходимо сообщить энергию не меньшую ширины запрещенной зоны, т.е. перевести электроны из валентной в свободную зону. Ширина запрещённой зоны у полупроводников имеет величину порядка 1эВ.
Еще большая энергия требуется для перевода электрона из валентной в зону проводимости (свободную зону) у изоляторов, почему они и не проводят электрический ток.
У металлов две соседние разрешенные зоны могут перекрываться и тогда переход электрона из валентной зоны в свободную по энергетическим затратам эквивалентен внутризонному переходу.
 2018-01-08
2018-01-08 5968
5968








