Средняя длина свободного пробега < λ >-расстояние, которое пробегает молекула между двумя очередными столкновениями. Зависит от эффективного сечения –то наименьшее расстояние, на которое сближаются молекулы в момент удара
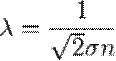
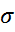 — эффективное сечение молекулы, n — концентрация молекул.
— эффективное сечение молекулы, n — концентрация молекул. 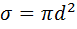 (
(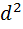 –эффективный диаметр)
–эффективный диаметр)
За одну секунду молекула проходит путь, равный средней арифметической скорости 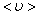 . За ту же секунду молекула претерпевает z столкновений. Следовательно, <z>=
. За ту же секунду молекула претерпевает z столкновений. Следовательно, <z>= 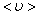 /<λ>
/<λ> 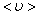 - скорость
- скорость
Билет N9
№1.Закон сохранения механической энергии. Абсолютно упругий и неупругий удар
Если тела, составляющие замкнутую механическую систему, взаимодействуют между собой только посредством сил тяготения и упругости, то работа этих сил равна изменению потенциальной энергии тел, взятому с противоположным знаком: 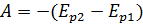
По теореме о кинетической энергии эта работа равна изменению кинетической энергии тел: 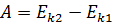
Следовательно 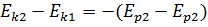 или
или
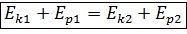
Сумма кинетической и потенциальной энергий тел, составляющих замкнутую систему и взаимодействующих между собой посредством сил тяготения и сил упругости, остается низменной.
Это утверждение выражает закон сохранения механической энергии. Он является следствием законов Ньютона. Сумму 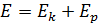 называют полной механической энергией.
называют полной механической энергией.
Ударом(или столкновением) принято называть кратковременное взаимодействие тел, в результате которого их скорости испытывают значительные изменения.
Абсолютно неупругим ударом называют такое ударное взаимодействие, при котором тела соединяются друг с другом и движутся дальше как одно тело. Механическая энергия не сохраняется, она частично или полностью переходит во внутреннюю энергию тел. Пример: попадание пули в баллистический маятник.
Абсолютно упругим ударом называют столкновение, при котором сохранятся механическая энергия системы тел. Пример: центральный удар двух бильярдных шаров.
№2. Реальный газ. Уравнение Ван-дер-Ваальса
Реальный газ - газ, который не описывается уравнением состояния идеального газа Клапейрона – Менделеева. Молекулы в реальном газе взаимодействуют между собой и занимают определенный объем. Наиболее корректно описывает свойства реальных газов уравнение: 
a и b-постоянные Ван-дер-Ваальса; R*-индивидуальная газовая постоянная
Внутренняя энергия реального газа зависит не только от температуры, но и от объема газа. Это связанно с тем, что силы Ван-дер-Ваальса стремятся притянуть молекулы газа, т.е. уменьшить его объем, и тем самым уменьшить энергию системы.
Билет N10
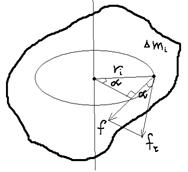
1) Рассмотрим вращение тв. тела под действием силы F:
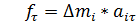
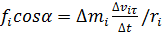
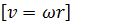
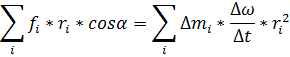
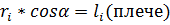

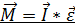
2) Термодинамика-раздел физики, в котором изучаются явления с энергетической точки зрения.Теплота-микроскопический способ передачи эн-ии.
1-ое начало термодинамики: тепло, полученное системой, идет на изменение его внутренней энергии
Тепло идет на изменение внутренней энергии системы и на совершение работы над телами

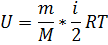
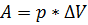
Невозможно построить вечный двигатель первого рода.(двигатель, который совершал бы работу большую, чем кол-во затраченного тепла)
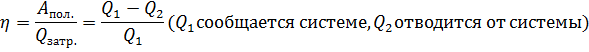
Теплоемкость системы-кол. теплоты, кот. нужно сообщить телу либо системе, чтобы его t изм. на 1 С.
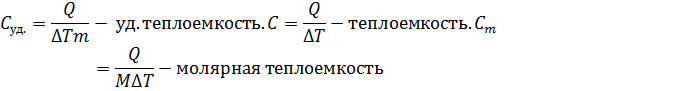
Билет N11
1. Кинетическая энергия тела, движущегося произвольным образом, равна сумме кинетических энергий всех n материальных точек па которые это тело можно разбить:
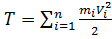 .
.
Если тело вращается вокруг неподвижной оси с угловой скоростью w, то линейная скорость i-ой точки равна
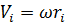 , где
, где 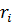 , - расстояние от этой точки до оси вращения.
, - расстояние от этой точки до оси вращения.
Следовательно: 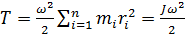 , где J- момент инерции тела относительно оси вращения. В общем случае движение твердого тела можно представить в виде суммы двух движений - поступательного со скоростью, равной скорости
, где J- момент инерции тела относительно оси вращения. В общем случае движение твердого тела можно представить в виде суммы двух движений - поступательного со скоростью, равной скорости 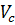 центра инерции тела, и вращения с угловой скоростью ω вокруг мгновенной оси, проходящей через центр инерции. При этом выражение для кинетической энергии тела преобразуется к виду
центра инерции тела, и вращения с угловой скоростью ω вокруг мгновенной оси, проходящей через центр инерции. При этом выражение для кинетической энергии тела преобразуется к виду
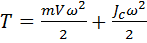 , где
, где 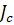 - момент инерции тела относительно мгновенной оси вращения, проходящей через центр инерции.
- момент инерции тела относительно мгновенной оси вращения, проходящей через центр инерции.
За время dt вращающееся тело совершит работу dA, равную произведению момента силы M на угол поворота 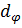 , сделанный радиусом этого тела, то есть dA=M
, сделанный радиусом этого тела, то есть dA=M 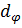 . Работу, совершенную вращающимся телом за единицу времени, называют мощностью вращающегося тела N, то есть
. Работу, совершенную вращающимся телом за единицу времени, называют мощностью вращающегося тела N, то есть 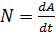 ,
, 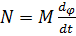 , где
, где 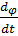 – мгновенное значение угловой скорости ω. Поэтому N=Mω.
– мгновенное значение угловой скорости ω. Поэтому N=Mω.
2.. Адиабатический процесс - это такое изменение состояний газа, при котором он не отдает и не поглощает извне теплоты. Следовательно, адиабатический процесс характеризуется отсутствием теплообмена газа с окружающей средой. Адиабатическими можно считать быстро протекающие процессы. Так как передачи теплоты при адиабатическом процессе не происходит, то уравнение I начала термодинамики принимает вид:
 ,
,
где ∆U-изменение внутренней энергии тела, A-работа, совершаемая системой. Внешняя работа газа может производиться вследствие изменения его внутренней энергии. Адиабатное расширение газа (dV>0) сопровождается положительной внешней работой, но при этом внутренняя энергия уменьшается и газ охлаждается (dT<0). Изменения энтропии S системы в обратимом адиабатическом процессе вследствие передачи тепла через границы системы не происходит:
 Здесь T-температура системы, δQ-теплота, полученная системой. Благодаря этому адиабатический процесс может быть составной частью обратимого цикла.Работа газа при адиабатическом процессе равна:
Здесь T-температура системы, δQ-теплота, полученная системой. Благодаря этому адиабатический процесс может быть составной частью обратимого цикла.Работа газа при адиабатическом процессе равна:  ,где p-давление газа, dV-малое приращение объема. Основное уравнение термодинамики примет вид: dU=-pdV. Уравнение Пуассона для идеального газа:
,где p-давление газа, dV-малое приращение объема. Основное уравнение термодинамики примет вид: dU=-pdV. Уравнение Пуассона для идеального газа:  ,где V-объем газа,
,где V-объем газа,  -показатель адиабаты,
-показатель адиабаты,  и
и  -теплоёмкости газа соответственно при постоянном давлении и постоянном объёме. С учётом уравнения состояния идеального газа уравнение адиабаты может быть преобразовано к виду:
-теплоёмкости газа соответственно при постоянном давлении и постоянном объёме. С учётом уравнения состояния идеального газа уравнение адиабаты может быть преобразовано к виду:  ,где T-абсолютная температура газа. Или к виду:
,где T-абсолютная температура газа. Или к виду:  . Поскольку k всегда больше 1, из последнего уравнения следует, что при адиабатическом сжатии (то есть при уменьшении V) газ нагревается (T возрастает), а при расширении — охлаждается, что всегда верно и для реальных газов. Нагревание при сжатии больше для того газа, у которого больше коэффициент k. При адиабатическом процессе показатель адиабаты равен
. Поскольку k всегда больше 1, из последнего уравнения следует, что при адиабатическом сжатии (то есть при уменьшении V) газ нагревается (T возрастает), а при расширении — охлаждается, что всегда верно и для реальных газов. Нагревание при сжатии больше для того газа, у которого больше коэффициент k. При адиабатическом процессе показатель адиабаты равен 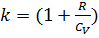 . 3.Задача:В закрытом сосуде находится 20г азота и 32г кислорода. Найти изменение внутренней энергии этой смеси при охлаждении её на 280.
. 3.Задача:В закрытом сосуде находится 20г азота и 32г кислорода. Найти изменение внутренней энергии этой смеси при охлаждении её на 280.
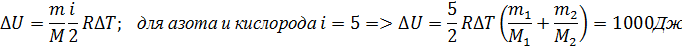
Билет N12
1) Дифференциальное уравнение гармонических колебаний и его решение. Энергия гармонического осциллятора.
Дифференциальное уравнение гармонических колебаний
(Любое нетривиальное решение этого дифференциального уравнения — есть гармоническое колебание с циклической частотой (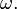 )
)
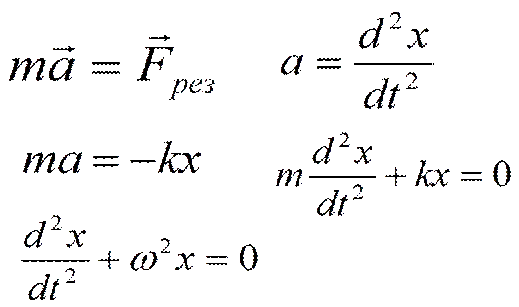
Энергия гармонического осциллятора
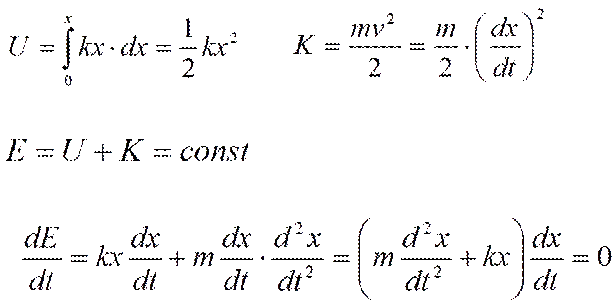
2) Применение первого начала термодинамики к изохорическому, изобарному, и изотермическому процессам.
Среди равновесных процессов, которые происходят с термодинамическими системами, отдельно рассматриваются изопроцессы, при которых один из основных параметров состояния остается постоянным.
Изохорный процесс (V=const). Диаграмма этого процесса (изохора) в координатах р, V изображается прямой, параллельной оси ординат (рис. 1), где процесс 1—2 есть изохорное нагревание, а 1—3 — изохорное охлаждение. При изохорном процессе газ не совершает работы над внешними телами, т. е.
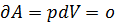
Из первого начала термодинамики (δQ=dU+δA) для изохорного процесса следует, что вся теплота, которая сообщается газу, идет на увеличение его внутренней энергии:
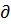 Q=dU
Q=dU
т.к. CV=dUm/dt,
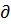 Q=dU
Q=dU
Тогда для произвольной массы газа получим
(1) 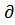 Q=dU=
Q=dU= 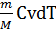
Изобарный процесс (p=const). Диаграмма этого процесса (изобара) в координатах р, V изображается прямой, которая параллельна оси V. При изобарном процессе работа газа при увеличения объема от V1 до V2 равна
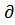 Q=dU=
Q=dU= 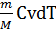 (2)
(2)
и равна площади заштрихованного прямоугольника (рис. 2). Если использовать уравнение Менделеева-Клапейрона для выбранных нами двух состояний, то
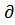 Q=dU=
Q=dU= 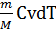 и pV2=
и pV2= 
откуда
V(2)-V(1)= 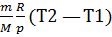
Тогда выражение (2) для работы изобарного расширения примет вид
A= 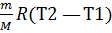 (3)
(3)
Из этого выражения вытекает физический смысл молярной газовой постоянной R: если T2 —T1 = 1К, то для 1 моль газа R=A, т. е. R численно равна работе изобарного расширения 1 моль идеального газа при нагревании его на 1 К.
В изобарном процессе при сообщении газу массой m количества теплоты
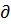 Q=
Q= 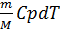
его внутренняя энергия возрастает на величину (т.к. CV=dUm/dt)
dU= 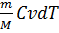
При этом газ совершит работу, определяемую выражением (3).
Изотермический процесс (T=const). Изотермический процесс описывается законом Бойля—Мариотта:
dU= 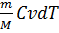
Диаграмма этого процесса (изотерма) в координатах р, V представляет собой гиперболу, которая расположена на диаграмме тем выше, чем выше температура, при которой происходит процесс.
Исходя из формул для работы газа и уравнения Менделеева-Клайперона найдем работу изотермического расширения газа:

Так как при Т=const внутренняя энергия идеального газа не изменяется:
dU= 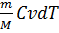 =0
=0
то из первого начала термодинамики (δQ=dU+δA) следует, что для изотермического процесса
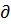 Q=
Q= 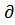 A
A
т. е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил:
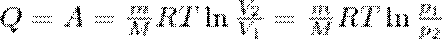 (4)
(4)
Значит, для того чтобы при расширении газа температура не становилась меньше, к газу в течение изотермического процесса необходимо подводить количество теплоты, равное внешней работе расширения.
Билет №13
 2018-01-08
2018-01-08 1466
1466

 -
-