Гибридизация атомных орбиталей
При определении геометрической формы частицы следует учитывать, что пары внешних электронов центрального атома располагаются в пространстве как можно дальше друг от друга.
При рассмотрении ковалентных связей нередко используют понятие о гибридизации орбиталей центрального атома - выравнивание их энергии и формы. Гибридизация является формальным приемом, применяемым для квантово-химического описания перестройки орбиталей в химических частицах по сравнению со свободными атомами. Сущность гибридизации атомных орбиталей состоит в том, что электрон вблизи ядра связанного атома характеризуется комбинацией атомных орбиталей с одинаковым главным квантовым числом. Такая комбинация называется гибридной (гибридизованной) орбиталью.
В результате гибридизации появляются новые гибридные орбитали, которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары/неспаренные электроны оказались максимально удаленными друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. Поэтому тип гибридизации определяет геометрию молекулы или иона.
ТИПЫ ГИБРИДИЗАЦИИ
| Тип гибридизации | Геометрическая форма | Угол между связями | Примеры |
| sp | линейная | 180o | BeCl2 |
| sp 2 | треугольная | 120o | BCl3 |
| sp 3 | тетраэдрическая | 109,28o | CH4 |
| СН4 |
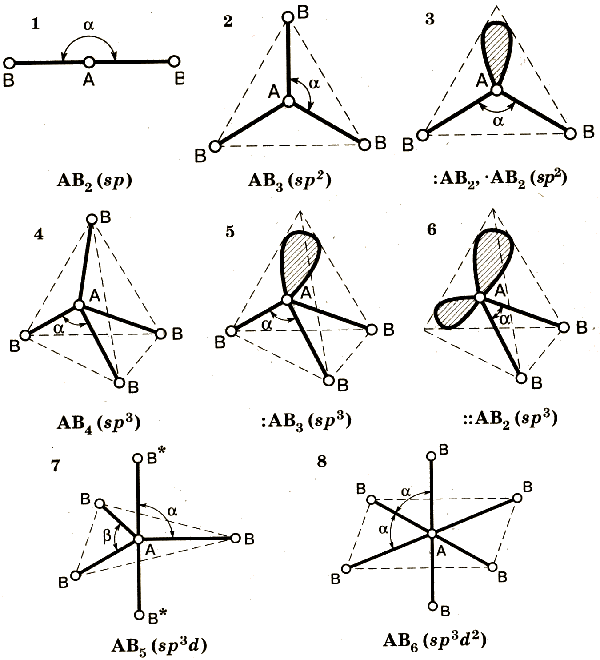
В гибридизации участвуют не только связывающие электроны, но и не поделенные электронные пары. Например, молекула воды содержит две ков связи между атомом кислорода и двумя атомами водорода.
 Помимо двух пар электронов, общих с атомами водорода, у атома кислорода имеются две пары внешних электронов, не участвующих в образовании неподеленные электронные пары. Все четыре пары электронов занимают определенные области в пространстве вокруг атома кислорода.
Помимо двух пар электронов, общих с атомами водорода, у атома кислорода имеются две пары внешних электронов, не участвующих в образовании неподеленные электронные пары. Все четыре пары электронов занимают определенные области в пространстве вокруг атома кислорода.
Поскольку электроны отталкиваются друг от друга, электронные облака располагаются на возможно большем расстоянии друг от друга. При этом в результате гибридизации меняется форма атомных орбиталей, они вытянуты и направлены к вершинам тетраэдра. Поэтому молекула воды имеет угловую форму, а угол между связями кислород-водород равен 104,5o.
Для предсказания типа гибридизации удобно использовать донорно-акцепторный механизм образования связи: происходит перекрывание пустых орбиталей менее электроотрицательного элемента и орбиталей более электроотрицательного элемента с находящимися на них парами электронов. При составлении электронных конфигураций атомов учитывают их степени окисления − число, характеризующее заряд атома в соединении, рассчитанный исходя из предположения ионного строения вещества.
Чтобы определить тип гибридизации и форму частицы:
находят центральный атом и определяют число σ-связей;
определяют степени окисления атомов в частице;
составляют электронную конфигурацию центрального атома в нужной степени окисления;
изображают схему распределения валентных электронов центрального атома по орбиталям, при этом, вопреки правилу Гунда, максимально спаривают электроны;
отмечают орбитали, участвующие в образовании связей с концевыми атомами;
определяют тип гибридизации;
по типу гибридизации определяют геометрию химической частицы.
Наличие π-связей не влияет на тип гибридизации. Однако наличие дополнительного связывания может привести к изменению валентных углов, поскольку электроны кратных связей сильнее отталкиваются друг от друга. По этой причине валентный угол в молекуле NO2 (sp 2) увеличивается  от 120o до 134o.
от 120o до 134o.
Кратность связи азот−кислород в этой молекуле равна 1,5, где единица отвечает одной σ-связи, а 0,5 равно отношению числа орбиталей атома азота, не участвующих в гибридизации (1) к числу оставшихся активных электронных пар у атома кислорода, образующих π-связи (2). Таким образом, наблюдается делокализация π-связей (делокализованные связи − ковалентные связи, кратность которых не может быть выражена целым числом).
 2018-01-21
2018-01-21 6057
6057
