Катализ. Положительный и отрицательный катализ. Гомогенный и гетерогенный катализ. Энергетический профиль каталитической реакции.


Гомогенный катализ - катализатор и реакционная смесь находятся в одной фазе. Скорость пропорциональна количеству катализатора(омыление сложных эфиров) H2О2 + I → H2О + IO; H2О2 + IO → H2О + О2 + I В гомогенном каталитических реакциях скорость пропорциональна числу катализатора, хотя его количество в системе невелико. Гомогенный катализ в растворах и биосредах может вызываться ионами водорода (кислотный катализ) и гидроксида (основный катализ).
Гетерогенный катализ - катализатор обычно твердый, а реакция протекает на его поверхности. Скорость зависит от площади и состояния катализатора, т.к. реакция проходит на активных центрах(водный раствор пероксида водорода взаимодействует с оксидом марганца 4).При гетерогенном катализе скорость реакции сильно зависит от площади и состояния поверхности катализатора, так как реакция происходит не на всей поверхности, а только на ее активных центрах.
Положительный катализ - скорость растет, отрицательный - снижается.


17.
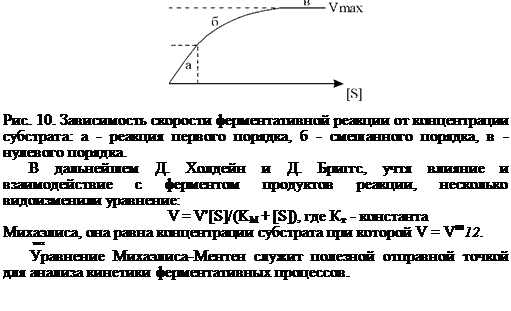
17. 17.Ферментативный катализ. Особенности каталитической активности ферментов. Уравнение Михаэлиса - Ментен и его анализ.



















Уравнение Михаэлиса-Ментен показывает, что при большей концентрации субстрата [S] и низком значении Ks скорость реакции будет равна максимальной скорости, т. е. V=Vmax, это в реакциях нулевого порядка; в случае малой концентрации субстрата скорость реакции будет прямо пропорциональна его концентрации в каждый данный момент (реакция первого порядка), т.е.: V=V'[S]/KS.
VA
Роль воды и растворов в жизнедеятельности. Физико-химические свойства воды, обусловливающие ее уникальную роль как единственного биорастворителя. Автопротолиз воды. Константа автопротолиза воды.





2.3. Автопротолиз воды
Все растворители условно можно разделить на две большие группы: апро-тонные и протолиты (или протонные растворители). Первые не обладают кислотно-основными свойствами (углеводороды, бензол, CS2, СС14 и др.), а вторые (Н О, С2Н5ОН, СН3СООН, HF, NH3, H2S04 и др.) - участники реакций протолиза.
Н20 - основной растворитель в биологических системах, является амфоли-том, способным самопроизвольно подвергаться слабой электролитической диссоциации или реакции автопротолиза:
н2о + н2о ирн- + н3о+
кис. осн. сопр. осн. сопр. кис.
Константа этого протолитического равновесия в соответствии с законом действующих масс равна:
Кс = [ОН-]-[Н30+]/[Н20]2. Равновесная концентрация растворителя [Н20] практически является величиной постоянной, т. к. концентрация молекул Н20, распавшихся на ионы, по сравнению с концентрацией недиссоциированных молекул, как правило, очень мала. Поэтому две константы Кс и [Н20] объединяют в одну константу Ks = Кс • [Н20]2, отсюда Ks = [ОН" ] • [Н30+]. Индекс "s" - первая буква английского слова solvent - растворитель, дляводы принят индекс "в" - вода.
Величину Ksназывают ионным произведением растворителя или константой автопротолиза растворителя.
Для воды = Ks = [ОН-] • [Н30+] = 1 • Ю-14 при t = 25°С. Автопротолиз воды процесс эндотермический.
I *
Н20 + Н20 Ц ОН" + Н30+; DH = 55,9 кДж/моль
кис. осн. сопр. осн. сопр. кис.
В обычных условиях (t=25°) Кв = 1 • Ю-14 (моль/л)2, а т. к. в чистой воде [ОН-] = [Н30+], то концентрация каждого из ионов при 25°С будет равна:
(Кв)1/2 = (10-14)1/2= Ю-7 моль/л
Следовательно, в чистой воде, где [ОН" ] = [Н30+] = 1*10"7моль/л, среда будет нейтральной. Исходя из этого ясно, что при:
[Н30+] > [ОН" ], т. е. 10~6... 10"1 моль, среда будет кислой.
[Н30+] < [ОН- ], т. е. 10~8... 10"14 моль, среда будет щелочной. Так как отрицательные степенные выражения неудобны в количественных расчетах, их заменяют логарифмическими функциями, которые называются показателями, таким образом:
рН - водородный показатель, это отрицательный десятичный логарифм концентрации ионов водорода:
PH=-lg[H+]
рОН - гидроксильный показатель, отрицательный десятичный логарифм концентрации гидроксид-ионов:
PH=-lg[OH-], рК^ - показатель ионного произведения воды.
Для чистой воды: рК^рН + рОН = 14 или рН = рОН =7 - среда нейтральная.
В кислых растворах: [Н30+] > Ю-7; рН < 7- среда кислая.
В щелочных растворах: [Н30+] < Ю-7; рН > 7- среда щелочная.
Автопротолиз – обратимый процесс образования равного числа катионов и анионов из незаряженных молекул жидкого индивидуального вещества за счет передачи протона от одной молекулы к другой.
H2O + H2O= H3O+ + OH–
Это Константа автопротолиза для воды обычно называется ионным произведением воды и обозначается как Kw. Ионное произведение численно равно произведению равновесных концентраций ионов гидроксония и гидроксид-анионов. Обычно используется упрощенная запись:
равновесие называется равновесием автопротолиза воды.

 19.Зависимость растворимости веществ в воде от соотношения гидрофильных и гидрофобных свойств; влияние внешних условий, на растворимость. Термодинамика растворения. Понятие об идеальном растворе.
19.Зависимость растворимости веществ в воде от соотношения гидрофильных и гидрофобных свойств; влияние внешних условий, на растворимость. Термодинамика растворения. Понятие об идеальном растворе.
Идеальными называются растворы, образование которых не сопровождается ни тепловыми, ни объемными изменениями системы (DH = 0, DV = 0). Свойства идеальных растворов не зависят от природы растворителя и растворенного вещества, а зависят только от количества частиц. При этом не имеют места какие-либо взаимодействия между частицами растворенного вещества и растворителя.

 Реальные растворы не являются идеальными и в своем поведении могут лишь приближаться к модели идеального раствора, например, разбавленные растворы неэлекролитов.
Реальные растворы не являются идеальными и в своем поведении могут лишь приближаться к модели идеального раствора, например, разбавленные растворы неэлекролитов.






Влияние внешних условий:
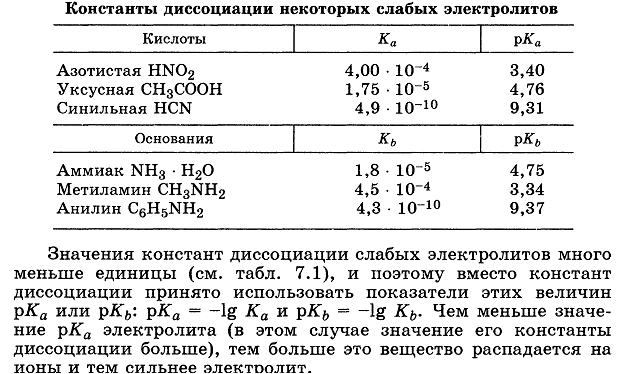
Элементы теории растворов электролитов. Сильные и слабые электролиты. Константы ионизации слабого электролита. Закон разбавления Оствальда.




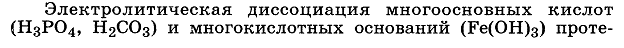




 21.Коллигативные свойства разбавленных растворов неэлектролитов. Закон Рауля и следствия из него: понижение температуры замерзания раствора, повышение температуры кипения раствора.
21.Коллигативные свойства разбавленных растворов неэлектролитов. Закон Рауля и следствия из него: понижение температуры замерзания раствора, повышение температуры кипения раствора.

Коллигаттивными свойствами разбавленных растворов являются: скоростть диффузии, осмотическое давление, давление насыщенного пара растворителя над раствором, температура кипения раствора, температура крист. Р-ра.

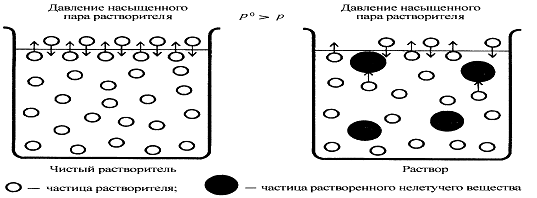

Этот закон соблюдается только в идеальных растворах. Растворы, компоненты которых существенно различаются по физическим и химическим свойствам, подчиняются закону Рауля лишь в области очень малых концентраций; при больших концентрациях наблюдаются отклонения от закона Рауля.
Второй закон Рауля(следствия) –
1) условием кристаллизации является равенство давления насыщенного пара растворителя над раствором давлению пара над твердым растворителем. Это будет достигаться только при более низких температурах, чем температура замерзания растворителя.
2 ) жидкость кипит при той температуре, при которой общее давление насыщенного пара становится равным внешнему давлению. Если вещество нелетучее, то давление должно быть равным парциальному давлению растворителя.

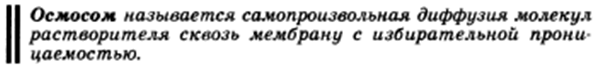 22.Осмос. Осмотическое
22.Осмос. Осмотическое
 2018-01-21
2018-01-21 2965
2965