Лекція 1.
Визначення:
Насичені вуглеводні мають загальну формулу CnH2n+2 , де n -1,2,3, і т.д. Мають закінчення –ан. Містять одинарні σ-зв’язки. Міжнародна назва насичених вуглеводнів – алкани, їх називають також парафіни .
Гомологічний ряд:
Метан СН4
Етан С2Н6
Пропан С3Н8
Характерна Sp3 гібридизація:
Всі атоми С в насичених вуглеводнях знаходяться у стані 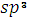 гібридизації.
гібридизації.
У збудженому стані атом Карбону має чотири неспарені валентні електрони.
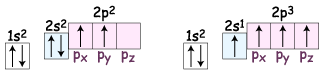
Фізичні властивості:
С1- С4 – гази
С5- С15 – рідини
Далі – тверді речовини
Не розчиняються у воді, але розчинні в органічних розчинниках.
Хімічні властивості:
1.Горіння
Підпалені на повітрі або в кисні алканигорять(реакція повного окиснення) з утворенням вуглекислого газу, води і виділенням теплоти. У разі нестачі кисню окиснення відбувається не повністю, частина речовини розкладається і утворюється Карбон у вигляді сажі та карбон(ІІ) оксид:

СН4 + О2 → СО2 + Н2О
2. Насичені вуглеводні стійкі до дії окисників, кислот, луг.
3. Насичені вуглеводні розкладаються при певній температурі на прості сполуки:
СН4 t = 1500 C C2H2 + 3H2
СН4 t > 1500 C C + 2H2
4. Реакція дегідрування(вiдщеплення Н2). Можливе для алканiв, починаючи з 2-ого вуглецю атома.
Внаслiдок реакції утворюються ненасиченi вуглеводнi(СnH2n).
С2H6 Cr2O3,t0 C2H4 + H2
СH3 – CH2 – CH3 Cr2O3,t0 CH2 = CH – CH3 + H2
Використовують ці реакції, як правило, у промисловості.
5. Крекiнг – це розщеплення молекул органiчних сполук пiд дією високих температур i за наявностi каталiзаторiв, яке супроводжується руйнуванням зв'язків C – C i утворенням речовин з меншою молекулярною масою(Можливий, починаючи з третього атома Карбону).
Умови: t = 450-500 oС, без доступу повiтря.
CH4 + CH2 = CH – CH3
СH3 – CH2 – CH2 – CH3
CH3 – CH3 + CH2 = CH2
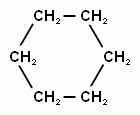 6. Пiролiз – це утворення циклічних сполук процесом розкладання органічних речовин без доступу повітря за високої температури.
6. Пiролiз – це утворення циклічних сполук процесом розкладання органічних речовин без доступу повітря за високої температури.
СH3 – CH2 – CH2 – CH2 – CH2 – CH3 Cr2O3,t0
7. Для насичених вуглеводнiв характерна реакцiя замiщення за гомолітичним(вiльнорадикальним механізмом):
а) При взаємодії з галогенами утворюються галогено-похiднi
CH4 + Cl2 hv CH3Cl + HCl;
CH3Cl + Cl2 hv CH2Cl2 + HCl;
CH2Cl2 + Cl2 hv CHCl3 + HCl;
CHCl3 + Cl2 hv CCl4 + HCl;
CH3Cl – хлористий метил;
CH2Cl2 – хлористий метилен;
CHCl3 – хлороформ;
CCl4 – чотирихлористий карбон.
Якщо в молекулi 3 атоми вуглецю, або бiльше, то реакцiя замiщення йде у друге положення.
CH3 – CH2 – CH3 + Сl2 hv CH3 – CH – CH3
|
Cl
Механізм:
Перша стадія: ініціювання реакції. Під дією енергії світла молекула хлору розщеплюється на атоми, що мають по одному неспареному електрону:
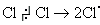
Ці частинки, які називають радикалами, дуже реакційноздатні.
Розривання ковалентного зв’язку, внаслідок якого утворюються частинки з неспареними електронами, називають гомолітичним.
Друга стадія: розвиток ланцюга. Унаслідок зіткнення з молекулою метану радикал відщеплює від неї атоми Гідрогену, при цьому утворюється новий радикал:
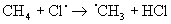
Стикаючись з молекулою хлору, вуглеводневий радикал відщеплює від неї атом Хлору й утворює молекулу хлорометану. Натомість утворюється радикал хлору:

Останній може атакувати молекулу хлорометану, внаслідок чого відбувається заміщення ще одного атома Гідрогену:
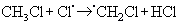
Ланцюг може розвиватися далі:

Третя стадія: обривання ланцюга. У разі зіткнення радикалів між собою настає обривання ланцюга:



Реакція припиняється, коли зникають усі вільні радикали.
б) Алкани взаємодіють з нітратною кислотою(HO – NO2 )
Реакцiя Коновалова
Реакцiя буде проходити при умовах: t = 140 0C,14% - нітратної кислоти.
CH4 + HO – NO2(14%) 140C CH3NO2 + H2O;
CH3 – CH2 – CH2 – CH3 + HO – NO2(14%) 140C CH3 - CH - CH3 + H2O
|
NO2
в) Реакція сульфоокиснення.
CH3 – CH2 – CH3 + SO2 Сr / hv CH3 – CH – CH3 + H2O
|
SO3H
г) Реакція сульфохлорування
CH3 – CH2 – CH3 + SO2 + Cl2 hv CH3 – CH – CH3 + HCl
|
SO2CL
8. Починаючи з четвертого атома вуглецю можлива iзомерiзацiя.
СH3 – CH2 – CH2 – CH3 AlCl3,t0 СH3 – CH – CH3
|
CH3
Добування:
1) Добування метану iз карбидiв алюмiнiя:
а) Аl4C3 + 12H2O t 3CH4 + 4Al(OH)3;
Al4C3 + 12HCl t 3CH4 + 4AlCl3;
б) CH3 – COONa + NaOH сплавл CH4 + Na2CO3.
2)Промисловi способи добування метану та гомологiв
nC + (n + 1)H2 t, Ni CnH2n + 2
C + 2H2 t, Ni CH4
CO + 3H2 t, Ni CH4 + H2O
3)Добування гомологiв iз солей карбонових кислот:
CH3 – CH2 – CH2 – COONa + NaOH сплавл CH3 – CH2 – CH3 + Na2CO3
4)За методом Фішера-Тропша
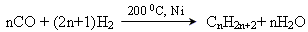
5)Реакція Вюрца
СH3Cl + 2Na + CH3Cl t CH3 – CH3 + 2NaCl
 СH3Cl + 2Na + CH3 – CH – CH3
СH3Cl + 2Na + CH3 – CH – CH3
| t CH3 – CH3
Cl
CH3 – CH – CH – CH3
| |
CH3 CH3
Застосування:
Насичені вуглеводні широко використовуються в органічному синтезі.
З них добувають багато органічних речовин: ненасичені вуглеводні, хлорпохідні, органічні кислоти.
Багато вуглеводнів входить до складу різних видів палива: горючого газу, бензину, гасу.
З вищіх алканів виготовляють такі речовини, як парафін і вазелін, мастила, електроізолятори.
Вищі алкани є сировиною для добування синтетичних мийних засобів.
Лекція 2.
Циклоалкани
Визначення:
Циклоалкани – насичены вуглеводні, молекули яких мають циклічну будову
Загальна формула: CnH2n
Sp3-гібридизація. Кути менші за 109028/, тільки у циклопентані більші.
Ізомерія: структурна. Також характерна просторова ізомерія, що зумовлена можливістю різного розміщення двох замісників, які належать різним атомам Карбону, відносно поверхні циклу. Такий вид ізомерії називають геометричною, або цис-транс-ізомерією.
Фізичні властивості:
Циклопропан і циклобутан – гази. Інші – рідини і тверді речовини.
Не розчиняються у воді, але розчинні в органічних розчинниках.
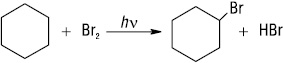 Хімічні властивості:
Хімічні властивості:
1.
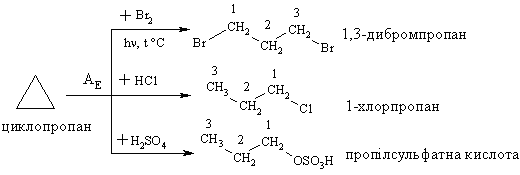 2.
2.
Добування:
1. 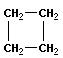 СН2-СН2-Cl
СН2-СН2-Cl
| + Zn + ZnC+ ZnCl2
СН2-СН2-Cl
Каталізатори: Cr2O3, Al2O3
*для цієї реакції використовують спиртовий розчин цинку

2.
Застосування:
Циклопропан використовують у медичній практиці як речовини для інгаляційного наркозу, циклопентанове кільце входить до складу простагландинів. Циклогексан — як розчинник для одержання капролактаму та адипінової кислоти, як екстрагент у фармацевтичній промисловості.
 2018-01-21
2018-01-21 956
956








