Лекція 1.
 Складні ефіри (естери)
Складні ефіри (естери)
Визначення:
Складні ефіри – продукт реакції етерифікації між спиртом і кислотою.
Фізичні властивості:
Естери з невисокими молекулярними масами є безбарвними рідинами з приємним запахом. Нерозчинні у воді, але розчиняються в органічних розчинниках. Температура кипіння менша, ніж у кислот, бо відсутні водневі зв’язки.
Хімічні властивості:
1. Реакція гідролізу або омилення.
Реакція гідролізу каталізує і лугами; в цьому випадку гідроліз незворотній:
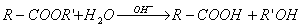
2. Реакція приєднання.
Складні ефіри, які мають у своєму складі ненасичених кислоту або спирт, здатні до реакцій приєднання.
3. Алкоголіз

4. Реакція утворення амідів.
Під дією аміаку на холоді складні ефіри перетворюються на аміди кислот і спирти:
R'-CO-OR" + NH3 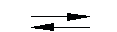 R'-CO-NH2 + R"OH.
R'-CO-NH2 + R"OH.
Добування:
· Етерифікація - взаємодія кислот і спиртів в умовах кислотного каталізу,наприклад отримання етилацетату з оцтової кислоти і етилового спирту:
o СН3COOH + C2H5OH = СН3COOC2H5 + H2O
· Взаємодія ангідридів або галогенангидридов карбонових кислот зі
· спиртами, наприклад отримання етилацетату з оцтового ангідриду і етилового спирту:
o (CH3CO)2O + 2 C2H5OH = 2 СН3COOC2H5 + H2O
· Взаємодія солей кислот з алкилгалогенидами
o RCOOMe + R'Hal = RCOOR' + MeHal
· Приєднання карбонових кислот до алкенам в умовах кислотного каталізу (у томучислі і кислотами Льюїса):
o RCOOH + R'CH=CHR'' = RCOOCHR'CH2R''
· Алкоголиз нітрилів в присутності кислот:
o RCN + H+ 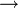 RC+=NH
RC+=NH
o RC+=NH + R’OH 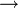 RC(OR')=N+H2
RC(OR')=N+H2
o RC(OR')=N+H2 + H2O  RCOOR' + +NH4
RCOOR' + +NH4
· Алкоголіз

Застосування:
Етилформіат та етилацетат використовуються як розчинники целюлозних лаків. Складні ефіри на основі нижчих спиртів і кислот використовують у харчовій промисловості при створенні фруктових есенцій, а на основі ароматичних спиртів — у парфумерній промисловості.
Воски входять до складу косметичних кремів і лікарських мазей. Тваринні жири і олії являють собою сировину для одержання вищих карбонових кислот, миючих засобів і гліцерину.
На основі рослинних олій виготовляють оліфи, що складають основу олійних фарб.
Нітрогліцерин — відомий лікарський препарат і вибухова речовина, основа динаміту.
Складні ефіри сірчаної кислоти використовують в органічному синтезі як алкілюючі реагенти, а фосфорної — як інсектициди.
Лекція 2.
Жири
Жири - складні ефіри, утворені вищими карбоксільними кислотами і гліцерином.
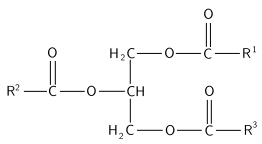 Загальна назва: тригліцериди
Загальна назва: тригліцериди
Загальна формула:
Фізичні властивості:
Тваринні жири, крім риб’ячого, є твердими речовинами, а рослинні – рідинами, окрім пальмової. Жири нерозчинні у воді, але добре розчиняються в бензині, бензині, дихлоретені.
Хімічні властивості:
1. Гідроліз
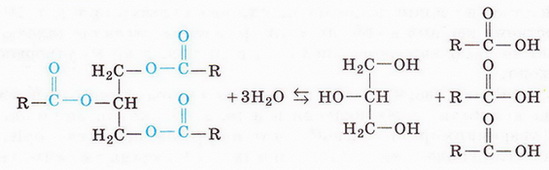
2. Омилення
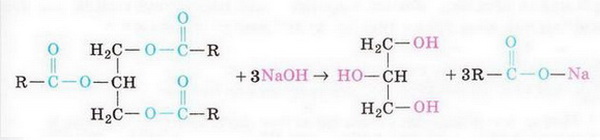
3. Гідрування (тільки для жирів ненасичених кислот)

Добування:
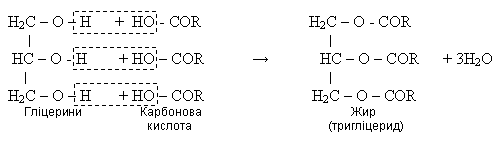
Застосування:
Жири - важливий продукт харчування людини. Жири становлять головний компонент таких продуктів харчування, як вершкове масло, рослинні олії, маргарин, смалець. Багато жирів містится у свинячому салі та у сирі.
Деякі жири (здебільшого рослинного походження) використовуються для виробництва мила.
Тема 7. Вуглеводи
 Вуглеводи – похідні вуглеводнів, у молекулах яких містяться гідроксильні групи, а також альдегідна чи кетонна група.
Вуглеводи – похідні вуглеводнів, у молекулах яких містяться гідроксильні групи, а також альдегідна чи кетонна група.
Загальна формула: Сn(H2O)m
Класифікація:
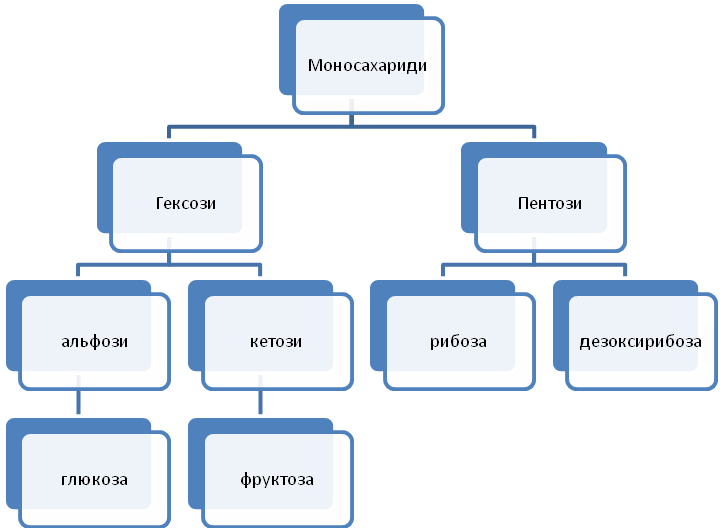
Лекція 1.
Глюкоза
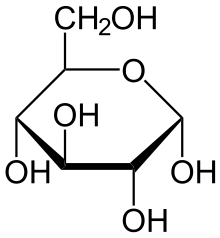
α-глюкоза
Альдегідна форма глюкози:
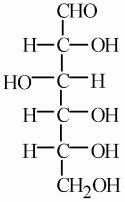
Фізичні властивості:
Глюкоза – безбарвна кристалічна речовина, добре розчинна у воді. Сполуки мають солодкий смак, фруктоза солодша за глюкозу.
У водному розчині існують усі види глюкози і між ними встановлюється хімічна речовина. Але кристалічна глюкоза складається тільки з α-форми і при розчині у Н2О переходить через альдегідну групу і у речовині переважає β-форма.
Поширення у природі: утворюється в процесі фотосинтезу:
6СО2 +6Н2О hV С6Н12О6 + 6О2
Хімічні властивості:
1. Реакція срібного дзеркала:
CH2OH(CHOH)4-COH + Ag2O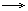 CH2OH(CHOH)4-COOH + 2Ag
CH2OH(CHOH)4-COOH + 2Ag
2. Гідрування (відновлення до 6-атомного спирту)
СН2ОН – (СНОН)4 – СОН + Н2 → СН2ОН – (СНОН)4 – СН2ОН
3. Взаємодія з Сu(ОН)2
СН2ОН–(СНОН)4–СОН + 2Сu(ОН)2 → СН2ОН–(СНОН)4–СООН + Сu2О + 2Н2О
4. Утворення естерів
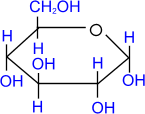

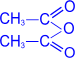
Спецефічні властивості:
А) Спиртове бродіння
С6Н12О6 → 2 С2Н5ОН + 2СО2
 2018-01-21
2018-01-21 1066
1066








