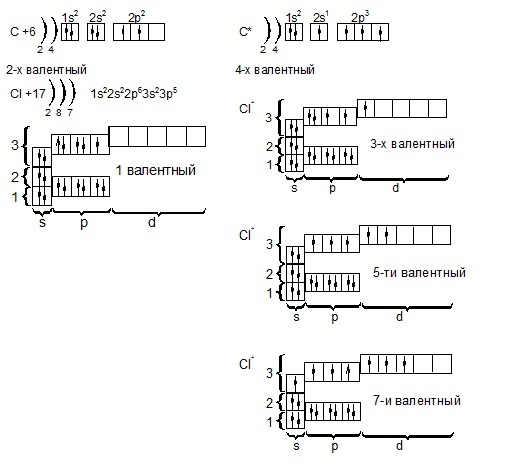
Задача 1. Составьте электронные формулы и представьте графически размещение электронов по квантовым ячейкам для элементов углерод и хлор. Проанализируйте возможности разъединения спаренных электронов при возбуждении атомов. Укажите валентность элементов в основном и возбужденном состояниях.
Решение:
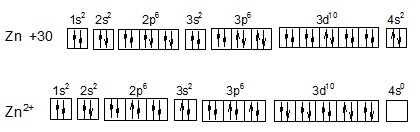
Задача 2. Представьте электронные формулы Zn+2; S+6.
Решение:
Zn0 – 2e = Zn2+
S0 – 6e = S6+
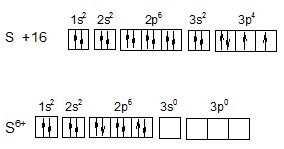
Задача 3. Укажите виды химической связи в следующих веществах: HBr, СаО, J2, Nа.
Решение:
HBr — ковалентная полярная связь. Ковалентная полярная связь возникает между атомами с близкими значениями электроотрицательностей, например между двумя неметаллами.
СаО – ионная связь. Ионные соединения образовываются, когда связываются атомы с большой разностью электроотрицательностей (более, чем 2,1). При соединении металлов с неметаллами, будет возникать соединение с ионной связью, т.к. их электроотрицательности очень различаются.
J2 – ковалентная неполярная связь. Если ковалентная связь в молекуле образована атомами с равной электроотрицательностью (чаще одинаковыми атомами), то такая связь не имеет полярности, т.е электронная плотность распределяется симметрично.
Nа – металл, в нем реализуется типичная для металлов металлическая связь.
Задача 4. Для гидросульфата натрия постройте графическую формулу и укажите виды химической связи в молекуле. Сколько σ- и π-связей имеет молекула?
Решение:
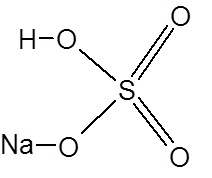
Связь O – Na – ионная
Связь O – S – ковалентная полярная
Связь O – H– ковалентная полярная
В молекулеNaHSО4 6 σ-связей и 2 π-связи.
Задача 5. Назовите приведенные соединения: а) [Ag(NH3)2]Cl, [Co (NH3)6](NO3)3, [Zn(H2O)4]SO4; б) K3[Fe(CN)6], K2[PtCl4]; в) [PdCl2(NH3)2].
Решение:
Расставим степени окисления: [Ag+(NH3)20]Cl-, [Co+3 (NH3)60]3+(NO3)3-, [Zn+2(H2O)40]2+SO42-, K3+[Fe+3(CN)6-]3-, K2+[Pt+4Cl4-]2-, [Pd+2Cl2-(NH3)20]0. С комплексным катионом а): хлорид диамминсеребра (I), нитрат гексамминкобальта (III), сульфат тетраквацинка (П). С комплексным анионом б): гексацианоферрат (III) калия, тетрахлороплатинат (II) калия. Комплекс — неэлектролит в): дихлородиамминпалладий.
Задача 6. Напишите формулы комплексных соединений по указанным названиям: а) хлорид тетраамминцинка (II), б) тетраиодокобальтат (III) натрия.
Решение:
а) хлорид тетраамминцинка (II) – [Zn(NH3)4]Cl2;
б) тетраиодокобальтат (III) натрия — Na[CoI4].
Задача 7. Эмпирическая формула соли CrCl3∙5H2O. Исходя из того, что координационное число хрома равно шести и вся вода связана внутрисферно, составьте координационную формулу соединения.
Решение:
CrCl3∙5H2O. Известно, что вся вода связана внутрисферно, а к.ч. = 6, поэтому формула соединения следующая: [Cr(H2O)5Cl]Cl2 – хлорид пентааквахлорохрома (III).
 2018-01-21
2018-01-21 2576
2576
