1) для сильной кислоты:
pH = -lg[H+] = -lgС, где С - концентрация кислоты, моль/л
2) для сильного основания:
рН = 14 – (-lg[OH-]) = 14 + lgС, где С - концентрация основания, моль/л
3) слабой кислоты:
рН= 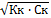 , где Кк – константа диссоциации слабой кислоты, Ск- концентрация кислоты, моль/л
, где Кк – константа диссоциации слабой кислоты, Ск- концентрация кислоты, моль/л
Если кислота многоосновная (Н2СО3, Н3РО4), то учитывается только диссоциация по первой стадии, так как диссоциация по остальным стадиям меньше и поставляет незначительное количество протонов.
4) cлабого основания:
рН = 14 – рОН = 14 – (-lg 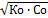 ) = 14+ lg
) = 14+ lg 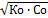 , где Ко – константа диссоциации слабой кислоты, Со- концентрация кислоты, моль/л
, где Ко – константа диссоциации слабой кислоты, Со- концентрация кислоты, моль/л
Гидролиз солей
Гидролиз солей – это обменное взаимодействие ионов соли с водой, которое приводит к образованию слабого электролита и как правило сопровождается изменением pH-среды.
Катионы сильных оснований и анионы сильных кислот не образуют слабых электролитов, поэтому гидролизу не подвергаются.
В зависимости от ионов, входящих в состав солей, в растворе могут устанавливаться следующие равновесия:
а) при гидролизе аниона (A¯) слабой кислоты:
А¯+ HOH = HA + OH¯
(образуются ионы OH¯, среда щелочная, pH>7);
б) при гидролизе катиона (B+) слабого основания:
B+ + HOH = BOH + H+
(образуются ионы Н+, среда кислая, pH<7);
в) при гидролизе катиона слабого основания и аниона слабой кислоты:
А¯ + НОН = НА + ОН¯, В+ + НОН = ВОН +Н+
Гидролиз солей, образованных многоосновными кислотами или многокислотными основаниями, протекает ступенчато, с образованием кислых или основных солей, преимущественно по первой ступени.
Особенность написания реакций гидролиза: сначала пишут ионные реакции, а затем молекулярное уравнение.
Таким образом, можно выделить три типа гидролиза:
1. гидролиз по аниону – такому гидролизу подвергаются соли, образованные катионом сильного основания и анионом слабой кислоты:
Na2CO3 + H2O =
2Na+ + CO32- + HOH = 2Na+ + HCO3¯ + OH¯
CO32- + HOH = HCO3¯ + OH¯ (pH > 7)
Na2CO3 + H2O = NaHCO3 + NaOH
2. гидролиз по катиону – подвергаются соли, образованные катионом слабого основания и анионом сильной кислоты:
CuSO4 + H2O =
Cu2+ + SO42- + HOH = CuOH+ + SO42- + H+
Cu2+ + HOH = CuOH+ + H+ (pH < 7)
2CuSO4 + 2H2O = (CuOH)2SO4 + H2SO4
3. гидролиз по катиону и аниону – подвергаются соли, образованные катионом слабого основания и анионом слабой кислоты:
CH3COONH4 + H2O =
CH3COO¯ + NH4+ + HOH = CH3COOH + NH4OH (pH≈7)
CH3COONH4 + H2O = CH3COOH + NH4OH
Если константы диссоциации образующихся слабых электролитов примерно равны, то pH≈7. В том случае, если К слабого основания больше, то среда – слабощелочная, в противном случае – слабокислая.
Гидролиз является обратимым процессом. В соответствии с принципом Ле Шателье введение дополнительного количества ионов H+ или OH+ в равновесную систему может усилить или подавить процесс гидролиза. Гидролиз является эндотермическим процессом, поэтому повышение температуры приводит к усилению гидролиза.
 2018-01-21
2018-01-21 1382
1382
