Электрод – это устройства которые состоят из проводника 1-го рода и ионного проводника, находящихся в контакте друг с другом. Бывают: металлические и газовые. К газовым относятся водородный и кислородный электроды.
Ур-ие Нернста для расчета потенциала водородного электрода:

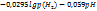
Для кислородного электрода:
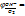
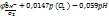
Гальванический элемент. Общие положения о гальвоническом элементе.ЭДС гальванического элемента.
ГЭ – называются ус-ва, в которых энергия хим. реакций преобразуется в электрическую. Состоит из двух полуэлементов, одним из которых является анод, а другой катод.
Система состоящая из металла погруженного в раствор собственной соли называется металлическим электродом. Величина потенциала выражается уравнением Нернста:
φ= 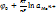
где 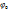 - стандартный потенциал данного электрода, Т=298К, R=8,31 Дж/моль*К
- стандартный потенциал данного электрода, Т=298К, R=8,31 Дж/моль*К
n-заряд ионов, F-число Фарадея = 96500Кл/моль, а – активность металла. После подстановки всех известных значении и переходи от натур логарифма к десятичному получаем:
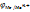 =
= 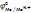 +
+ 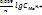
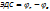 , для работающего ГЭ ЭДС всегда >0
, для работающего ГЭ ЭДС всегда >0
|
|
|
Напишите электронную конфигурацию атома хлора. Приведите его возможные валентные состояния.
 2018-01-21
2018-01-21 242
242






