КОВАЛЕНТНАЯ СВЯЗЬ - (от латинского «со» совместно и «vales» имеющий силу) (гомеополярная связь), химическая связь между двумя атомами, возникающая при обобществлении электронов, принадлежавших этим атомам. Ковалентной связью соединены атомы в молекулах простых газов. Связь, при которой имеется одна общая пара электронов, называется одинарной; существуют также двойные и тройные связи.
Поляризуемость–способность молекул поляризваться под влиянием внешнего электрического поля. Это может происходить и под влиянием поля, создаваемого приблизившейся полярной молекулой. Всегда важно учитывать полярность молекулы и ее электрический момент диполя. С последним связана реакционная способность веществ. Как правило, чем больше электрическиймомет диполя молекулы, тем выше реакционная способность вещества. С электрическим моментом диполя связана также растворимость вещества.
Насыщаемость - способность атома образовывать столько ковалентных связей сколько у него имеется энергетически доступных атомных орбиталей.
|
|
|
Направленность – определяет пространственную структуру молекул.Ковалентная связь направлена в сторону максимального перекрывания атомных орбиталей реагирующих атомов.
Метод валентных связей.
Метод валентных связей (МВС) иначе называют теорией локализованных электронных пар, поскольку в основе метода лежит предположение, что химическая связь между двумя атомами осуществляется с помощью одной или нескольких электронных пар, которые локализованы преимущественно между ними. В отличие от ММО, в котором простейшая химическая связь может быть как двух-, так и многоцентровой, в МВС она всегда двухэлектронная и обязательно двухцентровая. Число элементарных химических связей, которые способен образовывать атом или ион, равно его валентности. Так же, как и в ММО, в образовании химической связи принимают участие валентные электроны. Волновая функция, описывающая состояние электронов, образующих связь, называется локализованной орбиталью (ЛО).
Отметим, что электроны, описываемые ЛО, в соответствии с принципом Паули должны иметь противоположно направленные спины, то есть в МВС все спины спарены, и все молекулы должны быть диамагнитны. Следовательно, МВС принципиально не может объяснить магнитные свойства молекул.
Тем не менее, принцип локализованных связей имеет ряд важных преимуществ, одно из которых – его чрезвычайная наглядность. МВС достаточно хорошо, например, предсказывает валентные возможности атомов и геометрию образующейся молекулы. Последнее обстоятельство связано с так называемой гибридизацией АО. Она была введена для объяснения того факта, что двухэлектронные двухцентровые химические связи, образованные за счет АО в разных энергетических состояниях, имеют одинаковую энергию. Так, Be*(2 s 11 p 1), B*(2 s 12 p 2), C*(2 s 12 p 3) образуют за счет s - и p -орбиталей соответственно две, три и четыре связи, а потому одна из них должна быть прочнее других. Однако опыт показывает, что в BeH2, BCl3, CH4 все связи равноценны. У BeH2 угол связи равен 180°, у BCl3 – 120°, а у CH4 – 109°28'.
|
|
|
Донорно-акцепторный механизм образования ковалентной связи.
Существует и другой механизм, когда образование ковалентной связи происходит при взаимодействии одного атома или иона с заполненной атомной орбиталью с другим атомом или ионом имеющим вакантную орбиталь. Такой механизм образования ковалентной связи называется донорно-акцепторным.
Атом или ион, поставляющий электронную пару, называется донором, а атом или нон, ее принимающий, называется акцептором.
С точки зрения метода валентных схем по донорно-акцепторному механизму происходит перекрывание вакантной орбитали акцептора с заполненной орбиталью донора или донорной группы. Рассмотрим донорно-акцепторный механизм на примере образования иона аммония.

 Н Н
Н Н


 Н+ +: N – Н [
Н+ +: N – Н [  Н
Н  - N – Н ]+
- N – Н ]+
Н Н
В молекуле аммиака три неспаренных р - электрона атома азота образуют с тремя неспаренными электронами трех атомов водорода три ковалентные связи по обменному механизму. Неподеленная пара 2s – электронов атома азота взаимодействуют с вакантной орбиталью Н+. Образуется четвертая ковалентная связь по донорно-акцепторному механизму. Характеристики четвертой ковалентной связи такие, как у остальных.
Таким образом, валентность атомов элементов, согласно методу валентных схем, определяется как числом связей, образованных по обменному механизму, так и числом связей, образованных по донорно-акцепторному механизму.
Теория и типы гибридизации.
Угол между связями (валентный угол) является свойством двух связей одного общего атома и должен рассматриваться как свойство этого атома Согласно теории гибридизации Полинга - Слейтера валентный уголопределяется характером гибридных орбиталей для вр -гибридных он равен 109,5°, вр -гибридных — 120°, вр-гибридных— 180° И наоборот, по величине валентного угла можно судить
Sp-гибридизация

| Тип гибридизации | Число гибридных орбиталей | Геометрия | Структура | Примеры |
| sp | Линейная | 
| BeF2, CO2, NO2+ | |
| sp2 | Треугольная | 
| BF3, NO3-, CO32- | |
| sp3 | Тетраэдрическая | 
| CH4, ClO4-, SO42-, NH4+ | |
| dsp2 | Плоскоквадратная | 
| Ni(CO)4, [PdCl4]2- | |
| sp3d | Гексаэдрическая | 
| PCl5, AsF5 | |
| sp3d2, d2sp3 | Октаэдрическая | 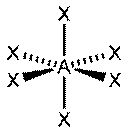
| SF6, Fe(CN)63-, CoF63- |
Происходит при смешивании одной s- и одной p-орбиталей. Образуются две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра центрального атома. Две оставшиеся негибридные p-орбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются неподелёнными парами электронов.
 2018-01-21
2018-01-21 848
848








