При увеличении концентрации исходных веществ равновесие смещается в сторону реакции, потребляющей эти вещества (вправо).
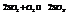
Влияние давления.
Увеличение давления смещает равновесие в сторону меньшего числа молей, т.е. в сторону падения давления.
Примечание. На реакцию, идущую без изменения числа молей, давление не влияет.
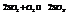

Скорость химической реакции. Закон действующих масс. Константа скорости.
Скорость гомогенной (однофазной) реакции зависит от природы реагирующих веществ, их концентрации и температуры.
Скорость гетерогенных (многофазных) процессов зависят от размеров и состояния поверхности раздела фаз.
Примечание. Гетерогенные – процессы, происходящие на поверхности раздела соприкасающихся фаз. (горение топлива, окисление металлом кислородом воздуха).
Закон действующих масс.
Справедлив для гомогенных реакций.
Формулировка: при постоянной температуре скорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Константа скорости обозначается как 
Пример. 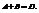

в квадратных скобках концентрации веществ.
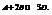


«к» не зависит от концентрации в каждый момент времени.
 2018-01-21
2018-01-21 551
551








