Гальванический элемент – любое устройство, дающее возможность получать электрический ток за счет проведения той или иной химической реакции.
Влияние природы реагирующих веществ.
Пусть протекает реакция:  Максимальная полезная работа:
Максимальная полезная работа: 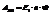


Реакция2: 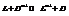
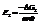
Вывод. В зависимости от природы веществ, ЭДС будет меняться.
Влияние температуры.
Согласно уравнению Гиббса-Гельмгольца, работа реакции. При наличии исходных термохимических данных можно рассчитать ЭДС. 2)Зависимость от температуры: 
Сделаем подстановки: 

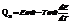
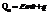
Qp – теплота реакции, которая выделяется или поглощается при ее необратимом проведении. Если реакция протекает обратимо, то часть энергии реакции превращается в работу А, а часть q остается в виде теплоты в элементе, q характеризует связанную энергию.
Определив градиент ЭДС, можно вычислить изменение энтропии для реакции.
Если q<0, 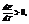 т.е. ЭДС уменьшается с ростом температуры.
т.е. ЭДС уменьшается с ростом температуры.
Если q>0,  т.е. ЭДС растет с ростом температуры.
т.е. ЭДС растет с ростом температуры.
Для гальванических элементов q подбирают малом, чтобы 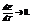
|
|
|
 2018-01-21
2018-01-21 1725
1725








