Пусть реакция 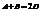
Изотерма реакции: 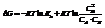
Преобразуем и получим: 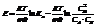
Обозначим первое слагаемое за 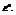
Это стандартная ЭДС, она отвечает случаю равенства единице концентраций всех участвующих веществ, т.е. стандартному изменению свободной энергии реакции 
Кислоты. Основные химические свойства.
Кислоты – это сложные вещества, содержащие атомы водорода, которые могут замещаться атомами металла.
Основность кислоты — это число атомов водорода, которые в молекуле кислоты могут замещаться атомами металла.
· Одноосновные, молекулы которых содержат один атом водорода
· Двухосновные, молекулы которых содержат два атома водорода и т. д.
· Бескислородные, молекулы которых не содержат атомов кислорода
· Кислородосодержащие, молекулы которых содержат атомы кислорода.
Химические свойства
Кислоты одинаково изменяют цвет индикатора.
Взаймодействуют
· С основаниями: Основание + Кислота = Соль + H2O
H3PO4 + 3NaOH = Na3PO4+ 3H2O
· С основными оксидами: Кислота + Основной оксид = Соль + H2O
2HCl + CaO = CaCl2 + H2O
· С амфотерными оксидами: Кислота + Амфотерный оксид = Соль + H2O
2HNO3 + ZnO = Zn(NO3)2 + H2O
· С амфотерными гидроксидами: Кислота + Амфотерный гидроксид = Соль + H2O
3HCl + Cr(OH)3 = CrCl3 + 3H2O
· С нормальными солями: Кислота + Соль = Соль + Кислота
HCl +AgNO3 = AgCl + HNO3
· С металлами 2HCl + Mg = MgCl2 + H2
 2018-01-21
2018-01-21 496
496








