Неэлектролиты - вещества, водные растворы и расплавы которых не проводят электрический ток, так как их молекулы не диссоциируют на ионы.
Осмос.Осмотическое давление.Пример: в стакан с водой залит слой р-ра сахарозы, спустя время концентрация р-ра во всем объеме одинакова. Между слоем воды и р-ра помещаем полупроницаемую перегородку (мембрану) она проницаема для мелких молекул воды и непроницаема для сахарозы. Процесс перехода молекул воды через мембрану наз-ся осмосом (односторонняя диффузия). Этот процесс прекращается когда к р-ру приложено осматическое давление.
Осматическое давление – давление, которое нужно приложить к р-ру, чтобы прекратился осмос, т.е. прекратилось проникновение мелких молекул в р-р через мембрану. Установили, что осматическое давление пропорц.концентрации раствор.в-ва.
Вант-Гофф вывел в виде закона: Pосм.=1000*Cm*R*T.
Давление пара над раствором. Первый закон Рауля.
жидкость↔ насыщенный пар,
т.е. число молекул жидкости, испаряющихся с поверхности, равно числу конденсирующихся молекул. Этому равновесию соответствует давление насыщенного пара растворителя над чистым растворителем 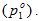 Нижний индекс (1) обозначает то, что свойство относится к растворителю; (2) – к растворенному веществу, а верхний индекс (о) указывает на то, что это свойство вещества в чистом состоянии; в данном случае это свойство чистого растворителя. В 1882 г. французский ученый Рауль сформулировал первый закон, названный его именем: относительное понижение давления насыщенного пара над раствором равняется мольной доле растворенного вещ-ва. ро-р/ро=Ni
Нижний индекс (1) обозначает то, что свойство относится к растворителю; (2) – к растворенному веществу, а верхний индекс (о) указывает на то, что это свойство вещества в чистом состоянии; в данном случае это свойство чистого растворителя. В 1882 г. французский ученый Рауль сформулировал первый закон, названный его именем: относительное понижение давления насыщенного пара над раствором равняется мольной доле растворенного вещ-ва. ро-р/ро=Ni
po – давл.насыщ.пара р-ля; р – давл.насыщ.пара над р-ом; ро-р – пониж.давл.н.п.р-ля над р-ом;
Ni-мольная доля (отношение числа молей растворенного в-ва к сумме числа молей всех компонентов р-ра)
Замерзание и кипение раствора. Второй закон Рауля.
Т.к. Рн.п. над р-ом < Рн.п. над р-ем, то t кипения р-ра > t кипения р-ля.
Раствор кипит при Рн.п. =Ратм.
Жидкость кристаллизуется, когда давление ее пара становится равным давлению насыщ.пара соответствующей твердой фазы (лед). Рн.п. льда достигается у р-ра при более низкой темпер.чем у р-ля.
2 закон Рауля: каждое чистое вещ-во характеризуется определенной температурой кипения или замерзания. У р-ов не так, t кипения,t кристаллизации р-ра зависит от давления насыщ.пара, от С р-ра.
 2018-01-21
2018-01-21 851
851








