История развития представлений о структуре атома. Теории Ломоносова и Дальтона. Модели атомов Томсона, Резерфорда, Бора.
Об атомах задумывались еще древние греки. В 18 веке Ломоносов сформулировал КОРПУСКУЛЯРНУЮ ТЕОРИЮ ст-ния в-ва. Открытие фун-х законов позволило вывест важнейшиии хим понятия, которые легли в основу анато-но мол-ного учения окогчательно признанного 1860 году.
Основ положения ат-ного учения:
1)Существуют вещества с мол-ным и немол-м ст-нием
2)Между мол-ми имеются промежутки,размеы которых зависят от тем и агр сост.
3)мол
….ТЕТРАДЬ
2.
Постулат Луи де Броля: он связал импульс движения материального объекта с длиной волны этого объекта через следующую величину.
L = h/p = h/mv, p = mv.
Функция 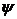 не является квантовым числом, а содержит эти квантовые числа.
не является квантовым числом, а содержит эти квантовые числа.
Принцип неопределённости де Броля: если частица имеет макроскопические размеры, то длина волны для этой частицы сравнительно мала.
m = 1г, v = 4 м/c, 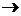
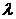 =10-21cм.
=10-21cм.
В качестве валентных выступают S и р подуровни.
3.
Правило Клечковского В.М.
Электрон заполн. Подуровень должен иметь минимально избыточной энергией по отношению к подуровню энергии.
Li 1822S1
Al18 1S22S22P63S23P63d0
K19 1S22S22P63S23P64S1
Правило Клечковского.
Заполнение идет от n+1 меньших к n+l больших
4S 3d
4+0 < 3+2 (сначала 4S, потом 3d)
2. Правило
Если суммы n+l равны друг другу, тозаполнение уровней и подуровней происходит в напр главного квантового числа k
4p 3 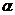
4+1 3+2 => сначала 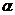 , потом 4p
, потом 4p
 2018-01-21
2018-01-21 570
570







