СH3COOH «CH3COO- + H+
Cu(OH)2 «[CuOH]+ + OH- (первая ступень)
[CuOH]+ «Cu2+ + OH- (вторая ступень)
H2CO3 «H+ + HCO- (первая ступень)
HCO3- «H+ + CO32- (вторая ступень)
Применим закон действия масс к равновесию между ионами и молекулами в растворе слабого электролита, например, уксусной кислоты:
CH3COOH 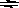 CH3COO- + H+
CH3COO- + H+ 
или синильной кислоты:
HCN 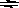 H+ + CN-
H+ + CN- 
Константы равновесия реакций диссоциации называются константами диссоциации. Константы диссоциации характеризуют диссоциацию слабых электролитов, чем меньше константа, тем меньше диссоциирует слабый электролит, тем он слабее. Так, например, поскольку КHCN =6,2×10-10<KCH3COOH = 1,8×10-5, то синильная кислота хуже диссоциирует и слабее, чем уксусная кислота.
Многоосновные кислоты диссоциируют ступенчато:
H3PO4 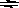 H+ + H2PO4-
H+ + H2PO4- 
H2PO4- 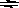 H+ + HPO42-
H+ + HPO42- 
HPO42- 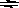 H+ + PO43-
H+ + PO43- 
Константа равновесия суммарной реакции диссоциации равна произведению констант отдельных стадий диссоциации:
H3PO4 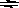 3H+ + PO43-
3H+ + PO43- 
Закон разбавления Оствальда:
При диссоциации слабого электролита, например, CH3COOH, молярная концентрация которого равна С, начальные и равновесные концентрации молекул и ионов равны:
CH3COOH 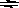 CH3COO- + H+
CH3COO- + H+
Снач С 0 0
Сравн С-Ca Ca Ca
где a - степень диссоциации.

Поскольку для слабых электролитов a<<1 и 1 - a» 1, имеем K=C×a2 или a =  .
.
Закон разбавления Оствальда: степень диссоциации слабого электролита увеличивается при уменьшении его концентрации, то есть при разбавлении.
 2018-01-21
2018-01-21 616
616








