Алкины
Алкины – это алифатические (ациклические), непредельные (ненасыщенные) углеводороды, с одной тройной углерод-углеродной связью С≡С в цепи и общей формулой СnH2n-2
Строение
Ацетилен – первый член гомологического ряда ацетиленовых углеводородов, или алкинов.
Молекулярная формула ацетилена C2H2
Структурная формула ацетилена H–C≡C–H
Электронная формула H: С ::: С: Н
Углеродные атомы ацетилена, связанные тройной связью, находятся в состоянии sp -гибридизации. При образовании молекулы ацетилена у каждого атома С гибридизуются по одной s - и p -орбитали. В результате этого каждый атом С приобретает по две гибридных орбитали, а две p -орбитали остаются негибридными. Две гибридных орбитали взаимно перекрываются, и между атомами С образуется σ-связь. Остальные две гибридных орбитали перекрываются с s -орбиталями атомов H, и между ними и атомами С тоже образуются σ -связи. Четыре негибридных p -орбитали размещены взаимно перпендикулярно и перпендикулярно направлениям σ-связей. В этих плоскостях p -орбитали взаимно перекрываются, и образуются две π -связи, которые относительно непрочные и в химических реакциях легко разрываются.
Таким образом, в молекуле ацетилена имеются три σ -связи (одна связь C–C и две связи C–H) и две π -связи между двумя С атомами. Тройная связь в алкинах – не утроенная простая, а комбинированная, состоящая из трех связей: одной σ - и двух π -связей.
Молекула ацетилена имеет линейное строение. Появление третьей связи вызывает дальнейшее сближение атомов С: расстояние между их центрами составляет 0,120 нм.

sp- Гибридные орбитали двух атомов углерода в состоянии,
предшествующем образованию тройной связи и связей C–H

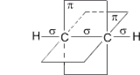
Схематическое изображение строения молекулы ацетилена (ядра атомов углерода и водорода на одной прямой, две p- связи между атомами углерода находятся в двух взаимно перпендикулярных плоскостях)
| Запомните! 1. Длина связи 0,120 нм 2. Угол связи 180° 3. Линейная молекула 4. Связи – σ и 2π 5. Sp- гибридизация |
Физические свойства
С2Н2 – Ацетилен – бесцветный газ, легче воздуха, мало растворим в воде, в чистом виде почти без запаха.
Свойства гомологов изменяются аналогично алкенам. По физическим свойствам алкины напоминают алкены и алканы. Температуры их плавления и кипения увеличиваются с ростом молекулярной массы. В обычных условиях алкины С2–С3 – газы, С4–С16 – жидкости, высшие алкины – твердые вещества. Наличие тройной связи в цепи приводит к повышению температуры кипения, плотности и растворимости их в воде по сравнению с олефинами и парафинами.
Изомерия и номенклатура
Структурная изомерия
1. Изомерия положения тройной связи (начиная с С4Н6):

2. 2. Изомерия углеродного скелета (начиная с С5Н8):
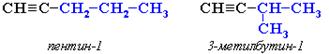
3. Межклассовая изомерия с алкадиенами и циклоалкенами, начиная с С4Н6:
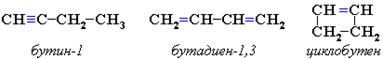
Пространственная изомерия относительно тройной связи в алкинах не проявляется, т.к. заместители могут располагаться только одним способом - вдоль линии связи.
 2017-11-01
2017-11-01 641
641







