Стехиометрический состав одноядерных карбонилов (без связи М−М) подчиняется так называемому правилу инертного (благородного) газа (или «правилу 18 электронов»). Согласно этому правилу число валентных электронов атома металла в сумме с числом электронов, предоставляемых атому металла координируемыми молекулами СО (по два электрона от каждой молекулы), должно быть равно 18, т.е. совпадать с числом электронов на внешних уровнях атома инертного газа в том же периоде. Другими словами, координация молекул СО должна приводить к возникновению у атома металла устойчивой конфигурации типа инертного газа (правило Сиджвика).
Состав электронной оболочки инертного газа (при n ≥ 3) может быть выражен формулой nd10+(n+1)s2+(n+1)р6. Таким образом, электронными парами должны быть заполнены 9 орбиталей, а для этого необходимо 18 электронов. Если считать, что в одноядерных мономерных карбонилах молекула СО координируется за счет предоставления металлу (на его пустые орбитали) одной пары электронов, то для переходных металлов с четным атомным номером можно составить следующие стехиометрические формулы.
| Металл | Электронная конфигурация металла | Число ē, необходимое для достижения М конфигурации благородного газа | Предполагаемая формула карбонила |
| Ti | 3d24s24p0 | Ti(CO)7 | |
| Cr | 3d44s24p0 | Cr(CO)6 | |
| Fe | 3d64s24p0 | Fe(CO)5 | |
| Ni | 3d84s24p0 | Ni(CO)4 |
Действительно, наиболее устойчивые одноядерные карбонилы хрома, железа, никеля имеют состав, согласующийся с правилом инертного газа.
Металлы с нечетным атомным номером, имеющие в наружной электронной оболочке нечетное число электронов, не могут таким же путем, как указанные выше металлы, сформировать электронную оболочку типа инертного газа. Поэтому «нечетные» переходные металлы, например марганец и кобальт, как правило, образуют полимерные (чаще димеризованные) карбонилы состава [Мn(СО)5]2, [Со(СО)4]2 и т.д. Полимеризация, как будет показано ниже, достигается за счет выполнения окисью углерода мостиковой функции, а также за счет связи М−М. Исключение в этом отношении составляет карбонил ванадия состава V(СО)6. Хотя атом ванадия содержит нечетное число электронов (3d34s24р0), его гексакарбонил имеет мономерное строение, поэтому 18-электронная конфигурация у ванадия в этом соединении не достигается. Полагают, что полимеризации препятствуют пространственные затруднения, возникающие из-за большого числа карбонильных групп, расположенных вокруг каждого атома ванадия, имеющего, как известно, относительно малые размеры.
Таким образом, правило инертного газа имеет ограниченную применимость и, как показано дальше, исходит из весьма упрощенных представлений о строении карбонилов. Однако для ориентировочной оценки стехиометрического состава карбонилов это правило полезно. Им можно пользоваться и для предсказания состава разнолигандных соединений переходных металлов, включающих в координационную сферу наряду с другими лигандами окись углерода. «Правило 18 электронов» в то же время не соблюдается, если синтез карбонилов проводится при низких температурах, например «на матрице» инертных газов. В этих условиях могут быть получены неустойчивые карбонилы необычного состава: Сr(СО)4, Со(СО)4 и т.д.
| Карбонил металла | Симметрия | Структура |
| Ni(CO)4 | Тетраэдр | 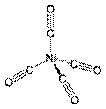 |
| Fe(CO)5 Ru(CO)5 Os(CO)5 | Тригональная бипирамида |  |
| V(CO)6 Cr(CO)6 Mo(CO)6 W(CO)6 | Октаэдр | 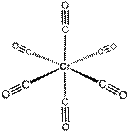 |
| Co2(CO)8 Rh2(CO)8 | Незеркальная тригональная бипирамида/мостиковый изомер |  |
| Mn2(CO)10 Tc2(CO)10 Re2(CO)10 | Незеркальный диоктаэдр | 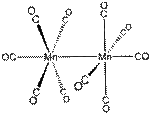 |
| Fe2(CO)9 | Структура «Фонарь» | 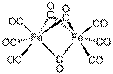 |
| Ru3(CO)12 Os3(CO)12 Fe3(CO)12 | Треугольный кластер | 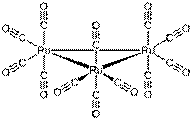 |
| Ir4(CO)12 Co4(CO)12 | Тетраэдрический кластер | 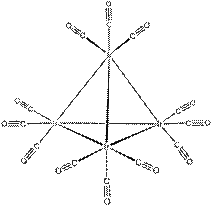 |
| Rh4(CO)12 | Тетраэдрический кластер | 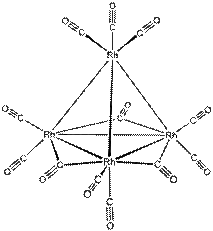 |
Карбонилы Ti, Zr, Hf, Nb, Ta неизвестны, карбонилы Pd, Pt, Cu, Ag, Au в виде нейтральных бинарных комплексов зафиксированы только в низкотемпературной инертной матрице.(Ozin, 1976).
 2017-11-01
2017-11-01 4327
4327








