Хлор находится в организме главным образом в ионизированной форме в виде хлорид анионов солей натрия, калия, кальция и магния.
Задания.
1. Написать электронную и электронно-графическую формулу строения аниона Сl- . Объяснить, отличие свойств анионов хлора от атомов хлора.
2. Осуществить превращение:
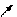 NaСl→NaNO3
NaСl→NaNO3
 Сl2→ΗСl
Сl2→ΗСl
Η2S →Na2S→PbS
Написать уравнения реакций в молекулярном и ионном виде.
3. Основные положения теории электролитической диссоциации. Степень и константа диссоциации.
Ситуационная задача №30
Вода является растворителем многих соединений, непосредственным компонентом ряда физико-химических и биохимических превращений, транспортером эндо- и экзогенных веществ.
Задания.
1. Почему вода является уникальным растворителем? (Объяснение дать на основании строения молекулы воды).
2. Даны вещества: СaС2; С2Η2; СΗ3СΗ=О; СaО; С6Η5NΗ2; СΗ3NΗ2; NΗ3. Какие из приведенных веществ будут реагировать с водой. Написать уравнения реакций.
3. Растворы. Растворимость веществ в воде. Диффузия. Осмос. Осмотическое давление.
Ситуационная задача №31
Сильные электролиты, NaСl, КСl, КΗ2PO4, К2ΗPO4, NaΗСO3 входят в состав жидких биологических сред.
Задания.
- К какому классу неорганических веществ относятся данные соединения? Написать схемы диссоциации данных электролитов.
- Осуществить превращения:
P→Η3PO4→Сa(Η2PO4)2→ Сa3(PO4)2→ P
- Соли, определения, классификация, номенклатура, свойства в свете теории электролитической диссоциации.
 2017-11-01
2017-11-01 745
745







