Диссоциация сильных электролитов настолько отличается от слабых, что была объяснена только через 40 лет после опубликования гипотезы Аррениуса.
Суть диссоциации сильных электролитов заключается в том, что они диссоциируют полностью, необратимо:
AB = A+ + B-.
Истинная степень диссоциации сильных электролитов равна всегда 100 % (1,0 доли ед.).
В растворах сильных электролитов ионов очень много (особенно при повышенных концентрациях). Отсюда две особенности растворов сильных электролитов:
· расстояния между ионами очень малы, иногда всего в 2-3 раза больше, чем в кристаллической решетке;
· количество ионов электролита соизмеримо с количеством молекул воды, и поэтому не все ионы могут быть гидратированы молекулами воды.
В силу этих двух особенностей каждый ион в растворе сильного электролита окружён ионами противоположного заряда, так называемой, " ионной атмосферой ".
Ионная атмосфера приводит к тому, что между ионами разных зарядов возникают силы притяжения, а между ионами одного заряда - силы отталкивания. Поскольку все ионы равноценны, то любой из них можно считать центральным в его ближайшем окружении, то – есть ионной атмосфере.
Понятием ионной атмосферы объясняют поведение ионов в растворе сильных электролитов. В растворах сильных электролитов ионы мешают друг другу принимать участие в физических и химических процессах. Кажущаяся степень диссоциации (αкаж.) отражает то количество активных ионов, которые принимают участие в химических и физических процессах. Поэтому αкаж. всегда меньше 100 % (1,0).
Под активностью понимается та часть ионов, которая приняла участие в физических и химических процессах, то - есть понятно, что активность всегда меньше концентрации. Поэтому αкаж< αист.
Активность и концентрация связаны между собой коэффициентом активности γ
a = γ .c.
Коэффициент активности - отношение экспериментальной величины к теоретической:
γ = экспериментальная величина/теоретическая величина.
Коэффициент активности некоторых электролитов в растворах приведены в табл. 2.
Таблица 2
| Концентрация раствора | Коэффициент активности | |
| NaCl | H2SO4 | |
| 0,001М | 0,965 | 0,830 |
| 0,01М | 0,874 | 0,544 |
| 0.1М | 0,778 | 0,265 |
| 1М | 0,657 | 0,138 |
В случае разбавленных растворов (для CB< 0,1М) коэффициент активности близок к единице, поэтому для разбавленных растворов сильных электролитов можно пользоваться понятием концентрации.
Если же растворы концентрированные, приходится пользоваться понятием активности.
Коэффициент активности раствора электролитов равен средней геометрической величине активности образовавших его ионов.
Так, для электролитов An Bm:
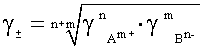 .
.
Кажущаяся степень диссоциации учитывает активные ионы, принявшие участие в физических и химических процессах.
Истинная степень диссоциации сильных электролитов всегда равна 1,0, кажущаяся степень диссоциации возрастает с повышением температуры раствора и понижением концентрации раствора.
Кажущаяся степень диссоциации связана с изотоническим коэффициентом соотношением
αкаж. = i-1 / n-1,
где n - количество ионов, на которые диссоциирует данный электролит.
 2014-01-31
2014-01-31 1455
1455
