При нормальных условиях (р=1 атм, Т=273 К) газы, входящие в состав атмосферы, мало отличаются по своему поведению от идеального газа. Поэтому для реальной атмосферы справедливо уравнение состояния идеального газа:
PV = ν RT, где
Р – давление;
V – объем газа;
ν – количество вещества;
R – универсальная газовая постоянная;
Т – температура.
Распределение давления в атмосфере по высоте Н описывается так называемой «барометрической формулой»:
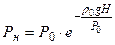 (2), где
(2), где
ρ0 и Р0 – плотность и давление при Н=0 (т.е. на уровне моря), причем Р0=101325 Па;
g – ускорение свободного падения.
Распределение концентрации составляющих атмосферу компонентов по высоте имеет вид:
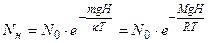 (3), где
(3), где
m – масса молекулы компонента;
M – молярная масса газа;
N0 – концентрация молекул на высоте Н=0 (на уровне моря);
κ – постоянная Больцмана;
R – универсальная газовая постоянная.
 2014-01-31
2014-01-31 759
759








