Оксиды подразделяются на солеобразующие и несолеобразующие.
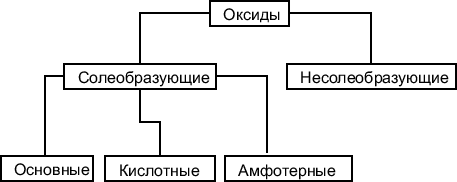
Солеобразующими называют такие оксиды, которые в результате химических реакций способны образовывать соли.
Несолеобразующие оксиды такой способностью не обладают. Примером несолеобразующих оксидов могут служить следующие вещества: CO, N2O, NO.
Солеобразующие оксиды, в свою очередь подразделяются на основные, кислотные и амфотерные.
Основными оксидами называются такие оксиды, которым в качестве гидратов (продуктов присоединения воды) соответствуют основания.
Например: Основные оксиды Соответствующая гидратная форма(основание)
Na2O → NaOH
BaO→ BaOH
СaO→ СaOH
Основные оксиды образуют металлы при проявлении ими невысокой валентности (обычно I или II).
Оксиды таких металлов, как Li,Na, K, Rb, Cs, Fr, Ca, Sr, Ba взаимодействуют с водой с образованием растворимых в воде оснований - щелочей. Другие основные оксиды непосредственно с водой не взаимодействуют, а соответствующие им основания получают из солей (косвенным путем).
Кислотными оксидами называются такие оксиды, которым в качестве гидратов соответствуют кислоты. Кислотные оксиды называют также ангидридами кислот.
Например: кислотные оксиды соответствующая гидратная форма (кислота)
SO3 → H2SO4
Р2О3→ H3РO4
СrО3→ H2CrO4
Кислотные оксиды образуют неметаллы и металлы при проявлений ими высокой валентности. Например, оксид марганца (VII) - кислотный оксид, так как в качестве гидрата ему соответствует кислота HMnO4 и это оксид металла с высокой валентностью.
Большинство кислотных оксидов могут взаимодействовать с водой непосредственно и при этом образовывать кислоты.
Например: СrО3 + H2O → H2CrO4
Р2О3 + H2O → H3РO4
SO3 + H2O → H2SO4
Некоторые оксиды непосредственно с водой не взаимодействуют. Такого типа оксиды сами могут быть получены из кислот. Например:
H2SiO3→ SiO2 + H2O (температура)
Это подтверждает названия кислотных оксидов - ангидриды, то есть "не содержащие воду".
Оксиды SO2 и CO2 реагирую с водой обратимо: СО2 + H2O ↔ H2CO3
SО2 + H2O ↔ H2SO3
Это подтверждает названия кислотных оксидов - ангидриды, то есть "не содержащие воду".
Амфотерные оксиды представляют собой оксиды, которые в зависимости от условий проявляют свойства как основных (в кислой среде), так и кислотных (в щелочной среде) оксидов.
К амфотерным оксидам относятся только оксиды некоторых металлов.
Например: BeO, Al2O3, PbO, SnO, ZnO, PbO2, SnO2, Сr2О3
PbO + 2HNO3→ Pb(NO3)2 + H2O
а) В кислой среде PbO (оксид свинца (II)) проявляет свойства основного оксида
б) в щелочной среде PbO проявляет свойства кислотного оксида.
t
PbO + 2NaOHтв → Na2 PbO2 + H2O
Амфотерные оксиды с водой непосредственно не взаимодействуют, следовательно, их гидратные формы получают косвенно - из солей. Несолеобразующие (индифферентные) оксиды - небольшая группа оксидов, не вступающая в химические реакции с образованием солей. К ним относятся: CO, N2O, NO, SiO2.
2. Получение оксидов.
1) окисление металлов: 2Cu + O2 = 2CuO
оксид меди (II) черный налет
Демонстрационный опыт - окисление меди кислородом в пламени спиртовки
2) окисление неметаллов: C + O2 = CO2
оксид углерода (IV)
3) разложение кислот: Н2SО4 = SО2 + Н2О
оксид серы (IV)
4) разложение солей: CaCО3 = CaО + CО2
оксид кальция (II)
5) разложение оснований: Fe(ОН)2 = FeО + Н2О
оксид железа (II)
7) горение сложных веществ: C2H5OH + 3О2 → 2CО2 + 3Н2О
Демонстрационный опыт – горение C2H5OH (этанол) в ложечке для сжигания веществ
3. Химические свойства оксидов.
1) Основные оксиды.
а) взаимодействие с кислотами: BaO + 2HCl = BaCl2 + H2O
оксид бария (II)
б) взаимодействие с водой: MgO + H2O = Mg(OH)2
оксид магния (II)
в) взаимодействие с кислотным оксидом: CaO + CO2 = CaCO3
оксид кальция (II)
г) взаимодействие с амфотерным оксидом: Na2O + ZnO = Na2ZnO2
цинкат натрия
2) Кислотные оксиды.
а) взаимодействие с водой: SO3 + H2O = H2SO4
оксид серы (VI)
б) взаимодействие с основанием: Ca(OH)2 + CO2 = CaCO3 + H2O
гидроксид кальция (II)
в) взаимодействие с основным оксидом: CO2 + CaO = CaCO3
карбонат кальция
3) Амфотерные оксиды.
а) взаимодействие с кислотами: ZnO + 2HCl = ZnCl2 + H2O
хлорид цинка
б) взаимодействие с основаниями: ZnO + 2NaOH = Na2ZnO2 + H2O
гидроксид натрия
 2020-05-12
2020-05-12 100
100






