1. Рассчитать потенциалы (Еоп) цинковых и медных электродов. При этом иметь в виду, что так как потенциал медного электрода более положителен, чем потенциал хлорсеребряного электрода, величина которого при 20°С составляет величину Ех-с = 0,201В, то измеренная в опыте разность потенциалов 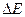 = ЕСu - Ех-с.. Для цинкового электрода:
= ЕСu - Ех-с.. Для цинкового электрода:  = Ех-с – ЕZn.
= Ех-с – ЕZn.
2. По формуле Нернста, используя табличные значения стандартных потенциалов медного и цинкового электродов, рассчитать теоретические значения потенциалов Етеор для электродов с разными концентрациями солей цинка и меди.
3. Рассчитать ЭДС элемента Якоби-Даниэля и сравнить ее с опытным значением измеренной разности потенциалов.
4. Полученные данные записать в таблицу и рассчитать % ошибки опытных результатов по сравнению с теоретическими.
| Схема гальванической цепи | ЭДС | Еоп | Етеор | Относительная ошибка, % |
5. Рассчитать ∆G0 реакции.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
1. Опишите механизм возникновения электродных потенциалов металлов. При каких условиях электродный потенциал называется стандартным (или нормальным)? Приведите формулу Нернста для расчетов потенциалов электродов 1-го и 2-го рода.
2. Рассчитайте величину электродного потенциала железа, погруженного в 0,01 М раствор соли FeS04, если кажущаяся степень диссоциации равна 40%.
3. Какова схема гальванического элемента, в котором протекает реакция
Cu + 2Ag+ = Сu+2 + 2Ag?
Рассчитайте ЭДС этого элемента и величину ∆G0.
4. Какие процессы происходят на электродах в гальваническом элементе:
(-} Mg|Mg(NO3)2||AgNO3|Ag (+)?
Определите ЭДС этого элемента.
Работа № 15. Электролиз и его практическое применение
 2020-05-12
2020-05-12 126
126








