Дисциплина: Химия
Группа: № 78
Урок № 35
Тема: Химические свойства карбоновых кислот.
Цель: Рассмотреть химические свойства карбоновых кислот
Литература: Рудзитис Г. Е. Химия. 10 класс: учеб. для общеобразоват. организаций с прил. на электрон. носителе базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – М.: Просвещение, 2014. – 224 с.
Материалы урока:
Повторить теоретический материал стр. 155-157
Упрочнение  -связи в карбонильной группе приводит к тому, что реакции присоединения для карбоновых кислот нехарактерны.
-связи в карбонильной группе приводит к тому, что реакции присоединения для карбоновых кислот нехарактерны.
1. Горение:
CH3COOH + 2O2 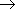 2CO2 + 2H2O
2CO2 + 2H2O
2. Кислотные свойства.
Из-за высокой полярности связи O-H карбоновые кислоты в водном растворе заметно диссоциируют (точнее, обратимо с ней реагируют):
HCOOH  HCOO- + H+ (точнее HCOOH + H2O
HCOO- + H+ (точнее HCOOH + H2O  HCOO- + H3O+)
HCOO- + H3O+)
Все карбоновые кислоты - слабые электролиты. С увеличением числа атомов углерода сила кислот убывает (из-за снижения полярности связи O-H); напротив, введение атомов галогена в углеводородный радикал приводит к возрастанию силы кислоты. Так, в ряду
HCOOH 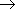 CH3COOH
CH3COOH 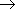 C2H5COOH
C2H5COOH
сила кислот снижается, а в ряду
| CH3COOH | 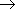
| CH2ClCOOH | 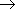
| CHCl2COOH | 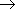
| CCl3COOH |
| уксусная кислота | монохлоруксусная кислота | дихлоруксусная кислота | трихлоруксусная кислота |
- возрастает.
Карбоновые кислоты проявляют все свойства, присущие слабым кислотам:
Mg + 2CH3COOH 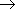 (CH3COO)2Mg + H2
(CH3COO)2Mg + H2 
CaO + 2CH3COOH 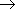 (CH3COO)2Ca + H2O
(CH3COO)2Ca + H2O
NaOH + CH3COOH 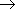 CH3COONa + H2O
CH3COONa + H2O
K2CO3 + 2CH3COOH 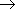 2CH3COOK + H2O + CO2
2CH3COOK + H2O + CO2 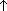
3. Этерификация (реакция карбоновых кислот со спиртами, приводящая к образованию сложного эфира):
|
| 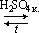
| 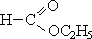
| + H2O | |
| муравьиная кислота | этанол | этиловый эфир муравьиной кислоты | ||
4.
В реакцию этерификации могут вступать и многоатомные спирты, например, глицерин. Сложные эфиры, образованные глицерином и высшими карбоновыми кислотами (жирными кислотами) - это жиры.
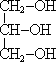
| + | 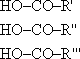
| 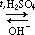
| 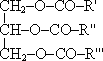
| + 3H2O |
| глицерин | карбоновые кислоты | триглицерид |
5.
Жиры представляют собой смеси триглицеридов. Предельные жирные кислоты (пальмитиновая C15H31COOH, стеариновая C17H35COOH) образуют твердые жиры животного происхождения, а непредельные (олеиновая C17H33COOH, линолевая C17H31COOH и др.) - жидкие жиры (масла) растительного происхождения.
6. Замещение в углеводородном радикале:
| CH3—CH2—COOH | + Cl2 | 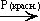
| CH3—CHCl—COOH | + HCl |
| пропионовая кислота |  -хлорпропионовая кислота -хлорпропионовая кислота
| |||
7.
Замещение протекает в  -положение.
-положение.
Особенность муравьиной кислоты HCOOH состоит в том, что это вещество - двуфункциональное соединение, оно одновременно является и карбоновой кислотой, и альдегидом:
8. 
9.
Поэтому муравьиная кислота кроме всего прочего реагирует и с аммиачным раствором оксида серебра (реакция серебряного зеркала; качественная реакция):
10. HCOOH + Ag2O(аммиачный раствор) 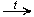 CO2 + H2O + 2Ag
CO2 + H2O + 2Ag
Домашнее задание.
Вопросы для самоконтроля:
1.Какие реакции характерны для карбоновых кислот?
2.Как горят карбоновые кислоты?
 2020-05-12
2020-05-12 127
127