| Понятие (см. стр. 12)
|
| Получение:
1) Взаимодействие металлов с азотной кислотой:
Zn + 4HNO3(конц.) → Zn(NO3)2 + 2NO2↑ + 2H2O
2) Взаимодействие оксидов металлов с азотной кислотой:
ZnO + 2HNO3 → Zn(NO3)2 + H2O
3)Взаимодействие гидроксидов металлов с азотной кислотой:
Zn(OH)2 + 2HNO3 → Zn(NO3)2 + 2H2O
4) Обменными реакциями двух солей (в результате реакции должен образовываться осадок): (NН4)2SO4 + Вa(NO3)2 → ВaSO4↓+ 2NH4NO3
Cu(NO3)2 + Na2S → 2NaNO3 + CuS↓
|
| Физические свойства:
Все нитраты – твердые кристаллические вещества. Окрашены в различные цвета. Все нитраты хорошо растворимы в воде.
|
Химические свойства:
1) С кислотами: NaNO3 + H2SO4 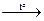 NaHSO4 + HNO3
2) Со щелочами: Mg(NO3)2 + 2NaOH → Mg(OH)2↓ + 2NaNO3
3) C другими солями: Zn(NO3)2 + Na2S → ZnS↓ + 2NaNO3
4) C более активными металлами: 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓
5) Разложение нитратов проходит по трем основным схемам, это зависит от активности металла:
а) если металл стоит в ряду активности до Mg(кроме Li):
MetNO3 NaHSO4 + HNO3
2) Со щелочами: Mg(NO3)2 + 2NaOH → Mg(OH)2↓ + 2NaNO3
3) C другими солями: Zn(NO3)2 + Na2S → ZnS↓ + 2NaNO3
4) C более активными металлами: 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓
5) Разложение нитратов проходит по трем основным схемам, это зависит от активности металла:
а) если металл стоит в ряду активности до Mg(кроме Li):
MetNO3 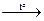 MetNO2 + О2↑
2NaNO3 MetNO2 + О2↑
2NaNO3 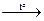 2NaNO2 + О2↑
б) если металл стоит в ряду активности от Mg до Cu и Li:
MetNO3 2NaNO2 + О2↑
б) если металл стоит в ряду активности от Mg до Cu и Li:
MetNO3 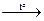 MetO + NO2↑ + О2↑
2Cu(NO3)2 MetO + NO2↑ + О2↑
2Cu(NO3)2 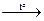 2CuO + 4NO2↑ + О2↑
4LiNO3 2CuO + 4NO2↑ + О2↑
4LiNO3 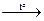 2Li2O + 4NO2↑ + О2↑
в) если металл стоит в ряду активности после Cu:
MetNO3 2Li2O + 4NO2↑ + О2↑
в) если металл стоит в ряду активности после Cu:
MetNO3 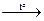 Met + NO2↑ + О2↑
2AgNO3 Met + NO2↑ + О2↑
2AgNO3 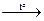 2Ag + 2NO2↑ + О2↑ 2Ag + 2NO2↑ + О2↑
|
| Применение:
1) Техническое название нитратов – селитры (см. стр. 12).
2) Многие нитраты являются минеральными удобрениями (см. стр. 13).
3) КNO3 – для получения черного пороха (в смеси с углем и серой).
4) AgNO3 («ляпис») – для получения серебра, а также в медицине.
|
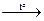 NaHSO4 + HNO3
2) Со щелочами: Mg(NO3)2 + 2NaOH → Mg(OH)2↓ + 2NaNO3
3) C другими солями: Zn(NO3)2 + Na2S → ZnS↓ + 2NaNO3
4) C более активными металлами: 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓
5) Разложение нитратов проходит по трем основным схемам, это зависит от активности металла:
а) если металл стоит в ряду активности до Mg(кроме Li):
MetNO3
NaHSO4 + HNO3
2) Со щелочами: Mg(NO3)2 + 2NaOH → Mg(OH)2↓ + 2NaNO3
3) C другими солями: Zn(NO3)2 + Na2S → ZnS↓ + 2NaNO3
4) C более активными металлами: 2AgNO3 + Cu → Cu(NO3)2 + 2Ag↓
5) Разложение нитратов проходит по трем основным схемам, это зависит от активности металла:
а) если металл стоит в ряду активности до Mg(кроме Li):
MetNO3 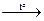 MetNO2 + О2↑
2NaNO3
MetNO2 + О2↑
2NaNO3 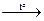 2NaNO2 + О2↑
б) если металл стоит в ряду активности от Mg до Cu и Li:
MetNO3
2NaNO2 + О2↑
б) если металл стоит в ряду активности от Mg до Cu и Li:
MetNO3 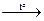 MetO + NO2↑ + О2↑
2Cu(NO3)2
MetO + NO2↑ + О2↑
2Cu(NO3)2 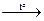 2CuO + 4NO2↑ + О2↑
4LiNO3
2CuO + 4NO2↑ + О2↑
4LiNO3 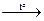 2Li2O + 4NO2↑ + О2↑
в) если металл стоит в ряду активности после Cu:
MetNO3
2Li2O + 4NO2↑ + О2↑
в) если металл стоит в ряду активности после Cu:
MetNO3 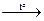 Met + NO2↑ + О2↑
2AgNO3
Met + NO2↑ + О2↑
2AgNO3 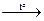 2Ag + 2NO2↑ + О2↑
2Ag + 2NO2↑ + О2↑
 2020-05-13
2020-05-13 112
112








