Виды химической связи
Химическая связь
В природе не существуют одиночные атомы. Все они находятся в составе простых и сложных соединений, где их объединение в молекулы обеспечивается образованием химических связей друг с другом.
Образование химических связей между атомами – естественный, самопроизвольный процесс, так как при этом происходит понижение энергии молекулярной системы, т.е. энергия молекулярной системы меньше суммарной энергии изолированных атомов. Это движущая сила образования химической связи.
Природа химических связей – электростатическая, т.к. атомы есть совокупность заряженных частиц, между которыми действуют силы притяжения и отталкивания, которые приходят в равновесие.
В образовании связей участвуют неспаренные электроны, находящиеся на внешних атомных орбиталях (или готовые электронные пары) – валентные электроны. Говорят, что при образовании связей происходит перекрывание электронных облаков, в результате чего между ядрами атомов возникает область, где вероятность нахождения электронов обоих атомов максимальна.
Химическая связь - это взаимодействие атомов, осуществляемое путем обмена электронами. При образовании химической связи атомы стремятся приобрести устойчивую восьмиэлектронную (или двухэлектронную – Н, Не) внешнюю оболочку, соответствующую строению атома ближайшего инертного газа, т.е. завершить свой внешний уровень. |
Классификация химических связей.
1. По механизму образования химической связи.
а) обменный, когда оба атома, образующие связь, предоставляют для неё неспаренные электроны.
Например, образование молекул водорода Н2 и хлора Cl2:
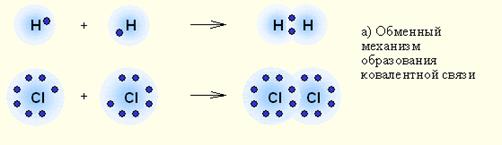
б) донорно – акцепторный, когда один из атомов предоставляет для образования связи готовую пару электронов (донор), а второй атом – пустую свободную орбиталь.
Например, образование иона аммония (NH4)+ (заряженная частица):
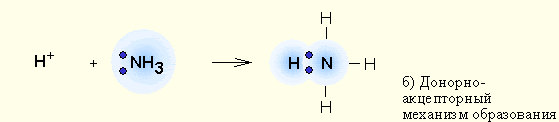
2. По способу перекрывания электронных орбиталей.
а) σ- связь (сигма), когда максимум перекрывания лежит на линии, соединяющей центры атомов.
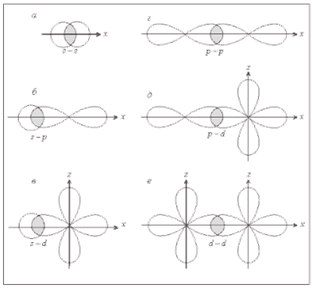
Например,
H2 σ(s-s)
Cl2 σ(p-p)
HCl σ(s-p)
б) π- связи (пи), если максимум перекрывания не лежит на линии, соединяющей центры атомов.
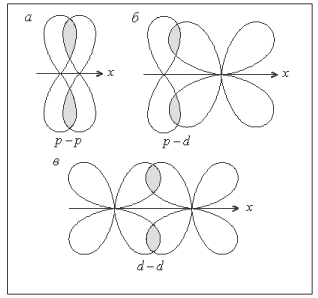
3. По способу достижения завершенной электронной оболочки.
Каждый атом стремится завершить свою внешнюю электронную оболочку, при этом способов достижения такого состояния может быть несколько.
| Признак сравнения | Ковалентная | Ионная | Металлическая | |
| неполярная | полярная | |||
| Как достигается завершенная электронная оболочка? | Обобществление электронов | Обобществление электронов | Полная передача электронов, образование ионов (заряженных частиц). | Обобществление электронов всеми атомами в крист. решетке |
| Какие атомы участвуют? | немет – немет ЭО = ЭО | 1) Немет-Немет1 2)Мет–немет ЭО < ЭО | мет +[немет]- ЭО << ЭО | В узлах находятся катионы и атомы металла. Связь осуществляют свободно перемещающиеся в межузловом пространстве электроны. |
| ∆c= ЭО1 – ЭО2 | 0 | < 1,7 | > 1,7 | 0 |
| Примеры | простые вещества – неметаллы. | кислоты, оксиды | соли, щелочи, оксиды щелочных металлов. | простые вещества – металлы. Связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке. |
Задания для закрепления
№1. Определите виды химических связей в молекулах следующих веществ:
H2S, KCl, O2, Na2S, Na2O, N2, NH3, CH4, BaF2, LiCl, O3, CO2, SO3, CCl4, F2.
№2. Напишите механизм образования молекул H2S, KCl, O2, Na2S, Na2O, N2, NH3, CH4, BaF2, LiCl, CCl4, F2. В случае ковалентной связи определите тип перекрывания электронных облаков (π или σ), а так же механизм образования (обменный или донорно-акцепторный)
 2020-05-11
2020-05-11 170
170






