1. Рассчитывают начальную ЭДС коррозионного элемента, равновесные анодные и катодные потенциалы, принимая концентрацию ионов металлов в растворах (например, [Аl3+] и др.) равной 10 моль/л и учитывая, что кислотный показатель среды рН = 7 (в тех опытах, в которых он не замерялся).
Расчеты равновесных потенциалов металлов проводят по формуле
φм+/м = φо + RT/nF • 2,3 lg[M+].
Расчет равновесного потенциала водородного электрода проводят по формуле
φН+/H = φо + RT/nF • 2,3 lg аH+ / Рн2,
где φн - равновесный потенциал водородного электрода, В;
φо=0 - стандартный потенциал нормального водородного электрода (при а =1 и р =1), В;
ан - активность ионов водорода в растворе, моль/л;
Рн2 – относительное парциальное давление водорода над раствором;
n - число электронов, участвующих в реакции восстановления ионов водорода.
Н30+ + е = 1/2Н2 + Н20.
При 25°С и парциальном давлении водорода в атмосфере воздуха (рн= 5 • 108 равновесный потенциал водородного электрода
φ = 0,215-0,059 рН,
где рН = -lg ан+ - кислотный показатель среды.
2.Строят полную коррозионную поляризационную диаграмму изученной системы в координатах ток (i) -потенциал ( φ ) типа представленной на рисунке 2.
|
|
|
|
|
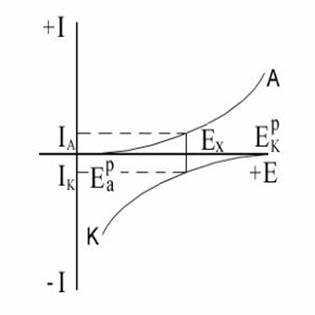
Рисунок.2 - Упрощенный вид поляризационной диаграммы
При этом:
а) используют расчетные значения равновесных потенциалов железа, меди и других металлов, водорода и кислорода в качестве исходных точек для построения соответствующих анодных и катодных кривых;
б) при построении катодных кривых для всех металлов учитывают перенапряжение водорода (определяющее наклон катодных кривых, см. таблица 1), полагая, например, что оно на меди в полтора раза выше, чем на железе, т.е.
ηСu =1,5 η Fe.
3. Подробно описывают протекание опыта. Оценивая газовыделение, можно применять условные показатели: "отсутствует", "очень слабое", "слабое", "среднее", "сильное", "очень сильное".
Т а б л и ц а 2- Перенапряжения водорода (ηн) и ионизация кислорода (ηо) на различных металлах
| Металл | ηн,в | ηо,в |
| Платина | 0,02 | 0,71 |
| Железо | 0,35 | 1,08 |
| Никель | 0,25-0,37 | 1,09 |
| Медь | 0,48 | 1,05 |
| Серебро | 0,57 | 0,97 |
| Алюминий | 0,58 | - |
| Цинк | 0,72 | 1,75 |
| Олово | 0,7-0,86 | 1,22 |
| Свинец | 1,16 | 1,45 |
Контрольные вопросы к работе № 1
1Типы коррозии. Классификация видов коррозии
2 Электрохимическая коррозия.
3 Термодинамика электрохимических систем и электродных процессов. Условная водородная шкала. Правило знаков ЭДС и электродных потенциалов
4. Электрохимический потенциал. Электрохимические равновесия.
5 Равновесные диаграммы потенциал-pH (диаграммы Пурбе или диаграммы электрохимического равновесия). Принципы построения. Использование диаграмм Пурбе
6Диаграмма равновесия воды
7 Коррозионно-поляризационные диаграммы.
8. Механизм и скорость электродной реакции. Равновесный и стационарный потенциалы. Ток обмена.
9 Простые и смешанные электроды. Поляризация и перенапряжение. Их типы
10Поляризационные диаграммы потенциал – pH
Лабораторная работа №2 Определение скорости коррозии металла объемным методом
Цель работы: ознакомиться с количественными методами оценки скорости коррозии
Теоретическая часть
Показатели коррозии
Прямые показатели коррозии
- убыль (увеличение) массы на единицу поверхности, г/(м2час);
- глубина коррозионного разрушения (проницаемость), мм/год;
- доля поверхности, занятая продуктами коррозии
- время, необходимое для появления коррозии на определенной части поверхности (10 или 50%);
- объем выделившегося газообразного продукта коррозии;
- время появления первого коррозионного разрушения;
- количество очагов коррозии на единицу поверхности.
- время до появления коррозионной трещины или полного разрушения образца;
Косвенные показатели:
- величина тока коррозии;
- изменение физико-механических свойств металла (предела прочности при испытаниях на сжатие и разрыв, относительного удлинения, отражательной способности и др.);
- электрическое сопротивление.
Скорость коррозии вычисляют либо в весовых единицах, отнесенных к единице поверхности (см2, м2) в единицу времени (час, сутки, год), либо в усредненном уменьшении толщины образца в микронах, миллиметрах или сантиметрах в год. При равномерной коррозии эта величина представляет большой интерес для конструкторов, так как дает оценку долговечности изделия.
Скорость коррозии
Скорость коррозии - коррозионные потери металла с единицы поверхности за единицу времени. Определение применяется для случаев сплошной, равномерной, неравномерной, местной, подповерхностной коррозии. Скорость коррозии. может быть выражена в А/м2 или г/(м2-ч) и по глубине проникновения - в мм/год. Всеэти показатели эквивалентны и могут быть пересчитаны один в другой. Основным показателем разрушения магистральных газопроводов является глубина проникновения.
Чаще всего скорость коррозий металлов оценивают количественно по убыли массы единицы поверхности металла в единицу времени - весовой показатель скорости коррозии. Его используют при равномерной коррозии, например при коррозии в кислотах, при коррозии малоуглеродистой стали и меди в атмосферных условиях.
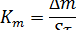
где Km - скорость коррозии, г/(м2час);
Δm- изменение массы металла за промежуток времени т на поверхности металла S.
Этот показатель может быть отрицательным, если масса металла за время испытания и после удаления продуктов коррозии уменьшилась. Он может быть и положительным, если масса образца за время испытаний увеличилась.
Если известен состав продуктов коррозии металла, то можно сделать пересчет положительного показателя изменения массы в отрицательный по формуле:
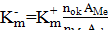
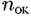 — валентность окислителя.
— валентность окислителя.
А – атомная масса
Отметим, что весовой показатель не всегда удобен, особенно если сравнивается коррозия металлов разной плотности. В таких случаях лучше пользоваться глубинным показателем коррозии, т.е. средней глубиной проникновения коррозионного разрушения в металл. Для листового металла и обечаек также применяют глубинный показатель коррозии Кп, или δ мм/год:
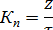
где z - глубина проникновения коррозионного разрушения в тело металла за время т.
Между этими двумя показателями существует простая взаимосвязь:
δ = Кп =8,76(К m/d) = 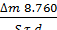
где d-плотность металла. кг/м3
Глубинный показатель удобен для конструкторов, которые, зная регламент на время эксплуатации изделия, рассчитывают припуск на коррозию.
По величине средней скорости коррозии находят балл, характеристику устойчивости металла и коррозионную активность среды
Независимо от вида агрессивной среды и характера коррозионного разрушения для оценки скорости. используют различные шкалы коррозионной устойчивости металлов и сплавов (таблица 3) и оценки степени коррозионной опасности (таблица 4).
При относительно равномерной коррозии с помощью глубины коррозионного проникновения определяют потери массы металла по формуле:
δ = Кп =8,76(К m/d),
Сопоставление величины максимального коррозионного разрушения, найденного по глубине самых глубоких каверн (мм), с величиной среднего коррозионного разрушения позволяет оценить степень неравномерности коррозии. Этот фактор необходимо учитывать при определении срока службы магистрального газопровода и др. объектов, поскольку неравномерная коррозия приводит к резкому понижению остаточной прочности и живучести участков трубопроводов и оборудования, пораженных ею.
Т а б л и ц а 3 - Шкала коррозионной стойкости металлов и сплавов
| Группы стойкости | Скорость коррозии, мм/год | Балл |
| Совершенно стойкие | 0,001 | 1 |
| Весьма стойкие | 0,001-0,005 | 2 |
| 0,005-0,01 | 3 | |
| Стойкие | 0,01-0,05 | 4 |
| 0,05-0,1 | 5 | |
| Пониженной стойкости | 0,1-0,5 | 6 |
| 0,5-1,0 | 7 | |
| Малостойкие | 1-5 | 8 |
| 5-10 | 9 | |
| Нестойкие | >10 | 10 |
Т а б л и ц а 4 Шкала коррозионной опасности магистральных газопроводов
| Степень опасности | Максимальная скорость коррозии, мм/год |
| Высокая | св. 0,3 |
| Повышенная | 0,1-0,3 |
| Умеренная | 0,01-0,1 |
Для определения скорости коррозии используются: ультразвуковая и виутритрубная дефектоскопия, инструментальное обследование коррозионных повреждений в шурфах; гравиметрический метод; электрохимический метод с помощью поляризационных кривых; группа методов, основанных на измерении электрических параметров сенсорных устройств, работающих в системах коррозионного мониторинга контролируемых объектов, и др. методы.
 2020-06-12
2020-06-12 138
138








