Пример 6. При взаимодействии 5,6 л газообразного амина с равным объемом хлороводорода (все н.у.) образовалась соль массой 20,375 г. Определите молекулярную формулу амина, напишите уравнение реакции с хлороводородом.
Запишем реакцию в общем виде:
С х Н у N + HCl = (С х Н у NH)+Cl–
Реакции аминов с кислотой – это реакции присоединения: 1 моль амина реагирует с 1 моль кислоты и образуется 1 моль соли. По условию, амин и соль взяты в стехиометрическом соотношении – т.е. в соответствующем коэффициентам реакции:

Число моль соли также равно 0,25 моль:

Найдем молярную массу соли:

Молекулярную массу исходного амина найдем по формуле:

Газообразные амины – это H3C–NH2, CH3–NH–CH3, N(CH3)3, молекулярную массу 45 г/моль имеет диметиламин. Запишем реакцию его взаимодействия с хлороводородом:

Пример 7. В результате реакции предельного двухатомного спирта массой 7,6 г с избытком металлического натрия выделился газ, объемом 2,24 л (н.у.). Установите молекулярную и структурную формулу спирта, если известно, что он не реагирует со свежеосажденным Cu(OH)2.
|
|
|
Предельные двухатомные спирты имеют общую формулу С n Н2 n +2О2 или, выделяя функциональные группы ОН: С n Н2 n (ОН)2. В реакции с избытком металлического натрия водород заместится в обеих гидроксильных группах, запишем реакцию в общем виде:
С n Н2 n (ОН)2 + 2Na = С n Н2 n (ОNa)2 + Н2
Число моль вступившего в реакцию спирта равно числу моль образовавшегося водорода:

Найдем молярную массу спирта:

Найдем n из уравнения
12 n + 2 n + 2×(16+1) = 76
n = 3
Молекулярная формула предельного двухатомного спирта С3Н6(ОН)2, запишем обе возможные структурные формулы:

Пропандиол-1,2 содержит группы –ОН у соседних атомов углерода, он реагирует со свежеосажденным Cu(OH)2 (подобно этиленгликолю, глицерину, глюкозе). А в пропандиоле-1,3 группы –ОН разнесены достаточно далеко, его свойства больше похожи на свойства одноатомных спиртов, которые не взаимодействуют со свежеосажденным Cu(OH)2. Искомая структурная формула:

Выше очень подробно рассмотрены все возможные варианты расчетов в задачах 35. Ниже разберем 4 примера задачи 35 формата ЕГЭ 2019–2020 с минимумом необходимых объяснений – так, как надо представить решение в бланке 2.
Пример 8. При сжигании дипептида природного происхождения массой 4,8 г получено 7,93 г углекислого газа, 0,83 г азота и 3,24 мл воды. При гидролизе дипептида в присутствии соляной кислоты образуется только одна соль.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу дипептида;
|
|
|
2) составьте возможную структурную формулу этого дипептида, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции гидролиза дипептида в присутствии соляной кислоты.
Решение:












Молекулярная формула С6Н12О3N2.
Так как при гидролизе образуется только одна соль – дипептид составлен из двух молекул одной и той же аминокислоты. Указано, что дипептид природного происхождения – это a-аминокислота:

Структурная формула дипептида:

Реакция гидролиза:

Пример 9. При сгорании 8,1 г органического вещества получили 11,76 л углекислого газа и 5,4 г воды. Известно, что это вещество реагирует с раствором гидроксида калия, а в реакции с бромной водой образуется трибромпроизводное этого вещества.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите реакцию взаимодействия этого вещества с бромной водой.
Решение:

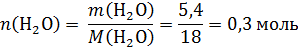

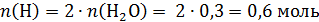

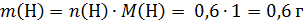



Молекулярная формула С7Н8О1.
Это ароматическое соединение. Оно относится к фенолам, так как реагирует с раствором гидроксида калия. Углерода не 6, а 7, т.е. с бензольным кольцом соединена не только группа –ОН, но и –СН3, причем они находятся друг от друга через один атом углерода – иначе не образуется трибромпроизводное при реакции с бромной водой.
Структурная формула:

реакция с бромной водой:

Пример 10. При полном сгорании органического вещества массой 38,85 г образовалось 69,3 г углекислого газа и 28,35 г воды. Относительная плотность паров этого вещества по воздуху равна 2,552. Установлено, что оно не реагирует с гидрокарбонатом натрия, но взаимодействует со щелочами и даёт реакцию «серебряного зеркала».
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите реакцию взаимодействия этого вещества с гидроксидом натрия.
Решение:









Простейшая формула С3Н6О2.
Найдем молекулярную массу искомого вещества:

Простейшая формула и является истинной, M (С3Н6О2) = 74 г/ моль. Молекулярная формула С3Н6О2. Это вещество с общей формулой С n H2 n O2 – или карбоновая кислота, или сложный эфир. Вещество не реагирует с гидрокарбонатом натрия – значит это не кислота. Это сложный эфир муравьиной кислоты – иначе не будет реакции «серебряного зеркала».
Структурная формула:

Реакция с гидроксидом натрия:

Пример 11. При окислении углеводорода С5Н8 перманганатом калия в сернокислой среде было получено органическое вещество А, содержащее по массе 61,54 % кислорода, 34,62 % углерода и 3,84 % водорода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте возможную структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А окислением углеводорода С5Н8 перманганатом калия в сернокислой среде.
|
|
|
Решение:
Убедимся, что сумма процентов равна 100:

Вещество А содержит только углерод, кислород и водород.



Молекулярная формула: С3Н4О4. 4 кислорода указывает на двухосновную кислоту, структурная формула:

В кислоте 3 углерода, в исходном углеводороде – 5, единственно возможный углеводород – пентадиен-1,4 (окисление будет идти с разрывом цепи по двойной связи, на обоих концах образуется карбоксильная группа).
Запишем реакцию окисления:

Д/З
1. При сгорании некоторого органического вещества массой 7,02 г получили 6,72 л углекислого газа (н.у.), 672 мл азота (н.у.) и 5,94 г воды. При нагревании с раствором гидроксида натрия данное вещество подвергается гидролизу, продуктами которого являются соль природной аминокислоты и вторичный спирт.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции гидролиза этого вещества в присутствии гидроксида натрия.
2. Органическое вещество содержит по массе 46,60 % углерода, 13,59 % азота и 31,07 % кислорода. При обработке этого вещества соляной кислотой образуется этанол и соль. Найдите формулу вещества и напишите реакцию взаимодействия с соляной кислотой.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите реакцию взаимодействия этого вещества с соляной кислотой.
3. При сгорании 5,3 г органического вещества получили 8,96 л углекислого газа (н.у.) и 4,5 г воды. Известно, что при окислении этого вещества сернокислым раствором перманганата калия образуется одноосновная кислота и выделяется углекислый газ.
|
|
|
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте возможную структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите реакцию взаимодействия этого вещества с сернокислым раствором перманганата калия.
 2020-06-29
2020-06-29 145
145







