Алифатические предельные одноосновные кислоты:
НСООН муравьиная
СН3СООН уксусная
С2Н5СООН пропионовая
С3Н7СООН масляная
С5Н11СООН валериановая
С6Н13СООН капроновая
С15Н31СООН пальмитиновая
С17Н35СООН стеариновая
Непредельные кислоты:
СН2=СН-СООН акриловая
СН3-(СН2)7-СН=СН-(СН2)7-СООН олеиновая
Ароматические кислоты:
С6Н5COOH бензойная
Двухосновные кислоты:
НООС-СООН щавелевая
НООС-СН2-СООН малоновая
Физические свойства
Водородные связи (прочнее, чем у молекул спиртов!)
1. температуры кипения и плавления карбоновых кислот намного выше, не только чем у соответствующих углеводородов, но и чем у спиртов;
2. хорошая растворимость в воде (с увеличением углеводородного радикала уменьшается).
Водородные связи в карбоновых кислотах настолько сильны, что эти вещества образуют димеры:
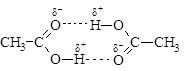
Почему водородные связи между молекулами карбоновых кислот прочнее, чем между молекулами спиртов?
Потому что в карбоксильной группе выше положительный заряд на атоме водорода в гидроксиле: электроотрицательный атом кислорода карбонильной группы стягивает электронную плотность с гидроксильной группы.
 2020-06-29
2020-06-29 226
226








