Лекции по неорганической химии
Для студентов очного отделения
факультета лесного хозяйства
План лекций
1. Скорость химической реакции. Химическое равновесие.
2. Растворы. Протолитические процессы и равновесия.
2.1 Классификация растворов. Тепловые и объемные эффекты.
2.2 Электролитическая диссоциация. Сильные и слабые электролиты.
2.3 Сильные электролиты. Теория Дебая - Хюккеля.
2.4 Теория кислот и оснований по Бренстеду – Лоури.
2.5 Ионное произведение воды. Водородный и гидроксильный показатель.
2.6 Буферные растворы
2.7 Гидролиз солей
3. Строение атома. Периодический закон
4. Химическая связь
5. Комплексные соединения
6. Окислительно - восстановительные реакции.
7.Редокспотенциалы и направление протекания окислительно- восстановительных реакций.
8.Химия биогенных элементов и их соединений.
8.1 Химия элементов VI группы. Халькогены.
8.2 Химия элементов V группы.
Скорость химической реакции. Химическое равновесие
Раздел химии, изучающий скорость химических реакций и механизмы их протекания называется химической кинетикой. Все реакции протекают во времени. Одни идут очень быстро (взрывы, горение), другие медленно (формирование горных пород). Но все реакции подчиняются общим законам.
|
|
|
Все реакции можно разделить на две группы:
1. Гомогенные – реагирующие вещества находятся в одной фазе – газообразной или жидкой.
N2 + 3H2 → 2NH3
2. Гетерогенные – реагирующие вещества находятся в разных фазах
Газ – твердое тело
Жидкость – Твердое тело
Газ – жидкость
С + O2 → CO2
Рассмотрим в общем виде химическую реакцию и изменение концентраций реагирующих веществ со временем:
А + В → C + D
Где: A и В – исходные вещества, С и D – продукты.
За скоростью реакции можно следить по изменению концентрации любого вещества, как по исходному, так и по продуктам.
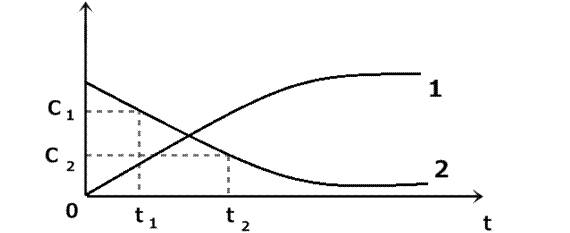
Рис. 1 Зависимость изменения концентрации продуктов (1) и исходных веществ (2) от времени.
Допустим, мы следим за скоростью реакции по исходному веществу. В какой - то момент времени t1 ему будет соответствовать концентрация С1, а моменту времени t2 будет соответствовать концентрация С2. Тогда средняя скорость реакции будет описываться уравнением:
Vср = - С2 - С1/ t2-t1 или: Vср = - ∆С/∆t
« -», еслирасчет ведется по исходным веществам;
«+», расчет ведется по продуктам реакции.
Истинная скорость реакции: Vист = - dC/dt
Скорость химической реакции – это изменение концентрации реагирующих веществ в единицу времени.
Скорость гомогенной реакции – это количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени в единице объёма системы:
|
|
|
Vгомог=  ;
;
Размерность скорости гомогенной реакции: моль/ л ∙ с
Скоростью гетерогенной реакции - это количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице поверхности раздела (или массы, объёма твердой фазы, когда затруднительно определение величины поверхности твёрдого тела):
Vгетерог = 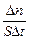
Размерность скорости гетерогенной реакции: моль/ м2∙с
Факторы, влияющие на скорость реакции:
1. Природа вещества
2. Концентрация
3. Температура
4. Наличие катализаторов и ингибиторов
 2020-09-24
2020-09-24 125
125







