Лекция № 2
1. Молярная концентрация или молярность [С(В) или СВ] моль/л – показывает сколько моль вещества В содержится в 1 литре раствора.
С(В)=m(г)/(Мр.в. ·Vр-ра)
Моль- это количество вещества системы, которое содержит столько определенных структурных элементов (молекул, атомов, ионов, электронов и т.д.) сколько атомов содержится в 0,012 кг углерода-12. (6,02×1023)
2. Молярная концентрация эквивалента или нормальность [C(fэкв(B)B)] моль×экв/л - показывает сколько моль эквивалента вещества В содержится в 1 литре раствора.
C(fэкв(B)B)= m(г)/(Э ·Vр-ра)
Эквивалент вещества В [ЭВ]- реальная или условная частица этого вещества, эквивалентная одному иону водорода в реакциях кислотно–основного взаимодействия или одному электрону в реакциях окисления-восстановления.
Фактор эквивалентности [fэкв(В)] – безразмерная величина, равная или меньше единицы. Рассчитывается на основании стехиометрии реакции:
Молярная масса эквивалента вещества В:
[M(fэкв(B)B)]= fэкв(B)×M(B)
Массовая доля или процентная концентрация- отношение массы (г) данного вещества в растворе к массе всего раствора.
3. Титр рабочего раствора В по рабочему веществу В [T(B) или ТВ] г/мл – число граммов растворенного вещества В в 1 мл раствора
Т(В) = m/V, или через концентрацию
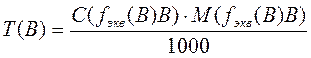
4. Титр рабочего раствора В по определяемому веществу А или условный титр [ТВ/А или Т(В/А)] г/мл - число граммов определяемого вещества А, эквивалентное 1 мл рабочего раствора В.
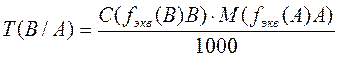
или через титр раствора
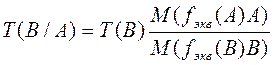 |
 2014-02-02
2014-02-02 5017
5017








