Жесткость воды показывает количество миллиэквивалентов (мэ/л) растворимых солей кальция и магния, содержащихся в одном литре воды. Ж (Н2О) (мэ/л).
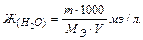
Самостоятельно: виды жесткости воды и способы ее устранения (см. учебник
гл. XIX, § 212, c. 596-599, задачник гл. XI, § 8, с. 232).
Задача 1. Чему равна жесткость воды, в 100 л которой содержится 14,63 г Mg (HCO3)2?
Для решения задачи используем формулу для определения жесткости воды.
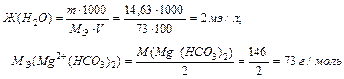
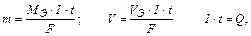
m – масса вещества (г), V – объем вещества(л);
I – сила тока, А;
t– время, с.
F = 96500 Кл/моль (F = 26,8 А∙ч/моль) (Кл = Кулон);
Q – количество электричества (А . с; А . ч).
КВАНТОВОМЕХАНИЧЕСКОЕ ПРЕДСТАВЛЕНИЕ О СТРОЕНИИ АТОМА. ПРАВИЛА И ПОРЯДОК ЗАПОЛНЕНИЯ АТОМНЫХ ОРБИТАЛЕЙ.
План:
1. Различные теории о строении атома.
2. Квантовые числа, их физический смысл.
3. Принципы заполнения атомных орбиталей.
Литература:
1. Фролов В.В. Химия. Гл.V, §51-56.
2. Лучинский Г.П. Курс химии. Гл.V, §8-12, гл. VI, §13-18
3. Ахметов Н.С. Общая и неорганическая химия. Раздел V, гл.3,4.
4. Общая химия под ред. Соколовской Е.М. и др. Гл.6, §1-11.
Научные основы атомно-молекулярного учения были заложены в работах русского ученого М.В.Ломоносова, французских химиков Лавуазье и Пруста, английского химика Дальтона и т.д. Однако до начала двадцатого века, атом считался единым и не делимым. Лишь только серия открытий 1896 – 1898 гг естественной радиоактивности Анри Беккерелем (1896 г - радиоактивность урана), Марией Склодовской-Кюри и Пьером Кюри, позволила изменить представления о неделимости атома.
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов (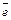 ), вращающихся вокруг него. Ядра атомов имеют сложное строение и состоят из нуклонов (протонов (
), вращающихся вокруг него. Ядра атомов имеют сложное строение и состоят из нуклонов (протонов (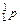 ) и нейтронов (
) и нейтронов (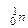 )).
)).
 2014-02-02
2014-02-02 893
893








